Eritrociták metabolizmusa
Az aerob sejtek energiát kapnak molekuláris oxigén formájában. Ugyanakkor a toxikus anyagok folyamatosan kisebb mennyiségben jelennek meg az O2-ból. az úgynevezett aktív oxigénformák [ROS (angol a reaktív oxigénfajokhoz)]. Ezek a vegyületek erős oxidáló szerek vagy erősen reaktív szabad gyökök (lásd 20. oldal), amelyek elpusztítják a sejtszerkezeteket és a funkcionális molekulákat. Különösen hajlamos ROS-károsodásra a vörösvérsejtek, amelyek szállítási funkciójuk miatt magas oxigén koncentráció jellemzi.
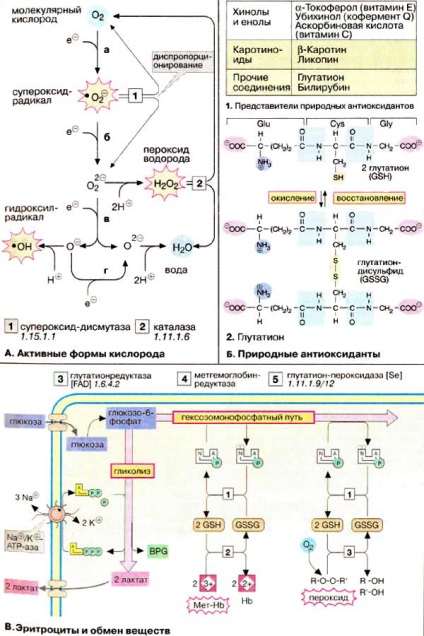
Az oxigénmolekula (O2) két párosítatlan elektront tartalmaz. így egy biradikális. Azonban a párosított elektronok úgy vannak elrendezve, hogy az O2 molekula viszonylag stabil maradjon. Mindazonáltal, ha a molekula tartalmaz egy extra elektron (a) lépés formák igen reakcióképes szuperoxid gyök (• O 2 -) következő redukciós lépésben (b) lépésben vezet peroxid anion (• O 2 2-), amely könnyen és ezáltal kötődik protonok ezt hidrogén-peroxiddá (H2O2) alakítjuk át. A harmadik elektron hozzáadása (c) lépés a molekula O 2 és O-ionokká történő felosztásához vezet. Míg az O2 - két proton hozzáadásával vizet képez. az O protonálása - egy különösen veszélyes hidroxilgyökhöz vezet (• OH). A negyedik elektron hozzáadása és az O - végek végső protonálása víz képződésével.
A ROS képződése például vasionokat katalizál. A ROS-ot folyamatosan az O2 és az FMN (FMN) vagy a FAD (FAD) közötti interakció hozza létre (lásd 108. oldal). Ezzel szemben a helyreállítási O2 citokróm c-oxidáz semmi bonyolult (folyik nélkül felhalmozódása ROS), mivel ez az enzim nem mentesíti közbenső szerdán. Az antioxidánsokkal együtt (B reakcióvázlat) vannak enzimek. amelyek szintén akadályozzák a szabad ROS kialakulását. Például, a szuperoxid-diszmutáz [1] két szuperoxid gyökök aránytalanságát okozza O2 és kevésbé veszélyes H2O2 alkalmazásával. Ez utóbbit ismét hem-tartalmú katalázzal O2 és H2O aránytalansága aránytalanná teszi [2].
A ROS és más gyökök elleni védelem érdekében minden sejt tartalmaz antioxidánsokat. Az utóbbiak restaurátorok. amelyek könnyen reagálnak oxidáló anyagokkal, és ennek eredményeként megvédik a fontosabb molekulákat az oxidációtól. A biológiai antioxidánsokhoz C és C vitaminok tartoznak # 917; (lásd a 352-355. oldalt), a Q koenzim (lásd 142 oldalt) és néhány karotinoidot (lásd: 58. 352. A hem megsemmisítése során keletkező bilirubin (lásd 196. oldal) szintén védelmet nyújt az oxidációval szemben. Különösen fontos a glutation. a Glu-Cys-Gly tripeptid, amely szinte minden sejtben nagy koncentrációban található. A glutation az atipikus # 947; -link a Glu és a Cys között. A redukálószer itt a cisztein maradék tiolcsoportja. A redukált forma két molekulája (GSH., A fenti ábrán) diszulfidot képez az oxidáció során (GSSG., Az alábbi ábrán).
A vörösvértestek is van egy rendszer (szuperoxid-dizmutáz, kataláz, GSH), amely képes inaktiválni ROS és megszünteti az okozott kár őket. Ehhez anyagokra van szükség. biztosítva a normális metabolizmus fenntartását az eritrocitákban. Anyagcsere eritrocitákban lényegében csak anaerob glikolízist (lásd. P. 148), és a hexóz-monofoszfát [GMP (HMW)] (lásd. P. 154).
A glikolízis során kialakult ATP elsősorban a Na + / K + -ATPáz szubsztrátja, amely támogatja a vörösvérsejtek membránpotenciálját. A glikolízis során 2,3-DPG effektor is létrejön (lásd 276. oldal). Az NMPH + H + a GMF-ben van kialakítva. amely biztosítja a H + regenerálására redukált glutation (GSH) a glutation-diszulfid (GSSG) keresztül glutation-reduktáz [3]. Az elkészített glutation a vörösvérsejtek legfontosabb antioxidáns. a funkcionálisan aktív hemoglobinban a methemoglobin visszanyerésében (lásd 274. oldal) koenzimként szolgál [4]. Fontos védőenzim a szelén tartalmú glutation-peroxidáz [5].
A csökkent glutation hatására a H2O2 detoxifikációra kerül sor. valamint a hidroperoxidok, amelyek a ROS reakciója során a vörösvérsejt-membrán telítetlen zsírsavjaival jönnek létre.
