Galvanikus cella a ph elem mérésére - a vegyész referenciakirálya 21
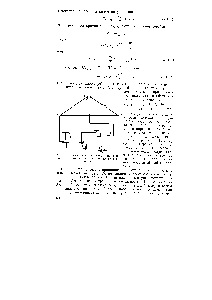
Ábra. 29. A telepítés elektromos ábrája az emf. stb. galván sejtek
A standard potenciálok az oxidációs-redukciós kémiai reakciók lehetséges irányáról gondoskodnak. Valóban azonban ez az irány a következő okok miatt eltérő lehet. Oxidáció-csökkentő rendszerek. a reakciósebességtől függően. amelyek az elektródákon áramlanak, reverzibilis és visszafordíthatatlan részekre oszthatók. A reverzibilis rendszerek standard potenciálját közvetlenül a fent leírt módszerrel mérjük, míg az irreverzibilis rendszerek standard potenciálját a legtöbb esetben a termodinamikai számítások találják. Ennek következtében a gyakorlatban az értékeik eltérőek, mivel számos tényező befolyásolja őket. Például az irreverzibilis rendszerek esetében a potenciálban a rendszer összetevőinek koncentrációjának változása szerint nincs rendszeres változás a potenciálban. és a standard oxidációs potenciál és komponenskoncentrációk alkalmazásával végzett számításokat. sokkal illusztráltabbak, mint azok a tényleges adatoknak. Ezért az oxidációs-redukciós rendszerek formális (valós) potenciálja sokkal gyakorlatiasabb. Formális potenciálokat (φ) találunk az emf. stb. galván sejt. amelyben az oxid alkotórészeinek kezdeti koncentrációi [c.350]
A kifejezés (V.5) lehetővé teszi az e. stb. galvanikus elem a folyamatok termodinamikai vizsgálatához. áramlik az elektródákon. A komplexitás E vizsgálatok, hogy közvetlen kapcsolatot létesít az elektrokémiai cella hagyományos mérőműszer (voltmérő) termodinamikai egyensúly a rendszer nem működik. Ez - amint korábban bemutattuk - az eredmények torzulását eredményezi, mivel nem mérjük e. stb. E elem, és az elektródák elektrosztatikus potenciáljának különbsége. A mérések során a szabályokat az alkalmazott mérőeszközzel együtt kell működtetni. Mérje meg az oldatok hőmérsékletét. [C.165]
A DC-forrást (lásd 28. ábra) be kell kapcsolni a P-kapcsolóval, majd a K-gomb a normál elemre vagy a cellára kapcsol. e. stb. amelyet mérünk. Kapcsolja ki fordított sorrendben. Ha az e. stb. minden potenciométer nélküli fizetés, megfelelő összeszerelés ellenőrzése a mérőberendezés séma szerint (lásd. ábra. 28), beleértve a pole a vizsgált elem és áramforrás. valamint a kapcsolatokat. A párhuzamos mérésekben fellépő oszcillációk rossz kapcsolatot jeleznek a főáramkörben (áramforrás áramkör). Ha az oldalsó áramkörben nincs áram, ellenőrizze az érintkezőket és a vezetők állapotát. Lehetséges, hogy az üvegszelvényekben légbuborékok kerülnek érintkezésbe és az elektrolitikus hídba. Az elektródák fémlemezén lévő csatlakozók nem érinthetik a megoldásokat. Szükséges az áramforrás feszültségének szisztematikus ellenőrzése és a potenciométer kalibrálása. Csatlakoztassa a tesztkamrát és a normál elemet a potenciométerrel a kulcsot csak az emitter mérési idejére. stb. és nagyon rövid időközönként kizárják a polarizációs jelenségeket és az ionok koncentrációját a megoldásokban az elem működtetése miatt. Az ionok diffúziójának csökkentése egyik félcellából a másikba elektrolitikus hídhoz kötődnek, csak az emf mérése előtt. stb. A hidakat telített sóoldatban tárolják. Az elektródákat és a galvánsejteket üvegedényekben gyűjtjük össze. amelyek formáit a munkák írják le. [C.142]
Az ilyen galvanikus elemeket centrális elemeknek nevezik. Gyakorlatilag ezek az elemek nem használhatók áram megszerzésére. de a mérés elmélete és módszertana szempontjából érdekes. Például az e. stb., egy ilyen elem meghatározhatjuk az ismeretlen számunkra a koncentrációt. [C.165]
Az 1. ábrán. A 129. ábra mutatja az emf mérésének irinzipial skálait. stb. galván sejt. A kompenzáló áramkör magában foglalja az aktuális forrás NZ - az akkumulátor 1, a feszültség, amely szállított slidewire AB, 2 galvanométer érzékeny elem 10, és a vizsgálati elem Weston nerek nochatelya 4 5 6 megszakító és a mozgatható érintkező C. A módszer alapja pas, hogy mért e. stb. kiegyensúlyozott (kompenzált). stb. akkumulátort. [C.298]
Lásd azokat a lapokat, amelyeken a "pH mérésére szolgáló galváncellás" kifejezés szerepel. [C.268] [c.424] [c.195] [c.126] [c.138] [c.309] [c.304] pH meghatározása Theory and Practice (1968) - [C.0]