Apoptózis - programozott sejtvesztés - biológia
Bővebben: STAGE - Nucleált kromatin-nukleázokra és / vagy kondenzációs enzimekre kifejtett hatások
A többsejtű élőlények - állatok, növények és gombák - genetikailag beépített program sejthalál. Morfogenetikai folyamatok egyedfejlődés, pozitív és negatív szelekció a T és B limfociták állatokban túlérzékeny növényi válasz patogén invázió, őszi lombhullás - csak néhány példa a programozott sejthalál (PKS). PKC és segít megőrizni a sorrendben a normális működését a biológiai rendszerek, tisztító a gazdátlan, a betegek, akik az életciklusuk vagy vrezultate mutációk jelentek meg a potenciálisan káros sejteket.
Az a tény, hogy az ontogénség genetikai kontroll alatt áll, alig tudott meglepni bárkit még a 20. század távoli 70. évében. Ez volt az irányítás, és megtalálta őt Brenner. Két másik "Nobel-ember" fedezte fel a "halál génjeit".
Régóta világos, hogy az ontogénség lehetetlen anélkül, hogy az egyes sejtek, szöveti helyek, sőt egész szervek megszűnnének, amelyek az egyéni fejlődés egyes szakaszaiban felmerülnek, így eltűnhet a felnőtt szervezet kialakulása után. Nem volt világos, hogy az ilyen elimináció fág-citoszin vagy valamilyen más, még nem ismert módon alakul-e ki.
A tudósok kísérleteiket a Caenorhabditis elegans fonálférgében végezték el
a) nagyon kicsi (körülbelül 1 mm hosszú)
c) az élő csak egy pár hétig. Ezen ez egyszerűen nyomon követni a sorsát minden alkotó 959 a megtermékenyített petesejt, amíg felnőtt osobi.Brenner használt mutagén (metiletansulfonat) és kapott mutációk, hogy megáll a fejlődés az egyes szakaszait az egyedfejlődés, és az azonosított gének felelősek értük.
Salston felhívta a figyelmet arra a tényre, hogy egy felnőtt nematódának 1090l-ből kell állnia. de nem 959 vagy 131 sejtből. az ontogenitás során meghal, figyelembe véve a programozott halál (apoptózis) útját. Sal-ben azonosította a sejtes öngyilkosság-nuc-1 első génjét, amely a DNS-degradációhoz szükséges egy haldokló sejtben. Ugyanabban a 70-es években Horwitz folytatta a Brenner tanulmányát, felfedezte a ced-3 és ced-4 géneket, amelyek szükségesek a sejtes öngyilkossághoz. Ezt követően Horwitz is opisol gént ced-9, tartja a sejt apoptózis, amíg ideje volt, és a megfelelő géneket talált magasabb rendű állatokban és emberekben.
Az apoptózis és a nekrózis a sejtpusztulás két változata
Az állatokban kétféle sejthalál létezik: apoptózis és nekrózis.
apoptózis Festés állatok - az átmenet a foszfatidilszerin a belső monoréteg a citoplazma membránon a külső egyrétegű, csökkentése sejttérfogat, zsugorodása a citoplazma membránon, a nucleus kondenzációs (karyorrhexis és karyopyknosis: karyorrhexis-marginatsiya heterokromatin és a kialakulását gyűrűk egyedi csomók; Pyknosis kompressziós sejtmagok), szünetek a nukleáris DNS-szálak és az azt követő bomlását a sejtmag részekre, fragmentáció sejteket membránvezikulák intracelluláris tartalmát (apoptotikus sejtek), sejtek és makrofágok fagocitáiják E szomszédok. Ugyanez a sors felfogja cellában, amikor az bekövetkezett mutáció, ami oda vezethet, hogy a tumorszövet proliferációját, amikor szükségtelenné válik a testben, például, során ontogenic fejlesztés, illetve alkalmazása a limfociták, a végső szakaszában a fertőzés, ha a szervezet már nem igényeinek a további antitestek termelését [5-7].
A sejtvesztés másik - kóros formája - a nekrózis. Ez a halál után jön egy ketrecben, amikor a T-gyilkos nem azonnal elrendelte a sorsa a fertőzött sejt, miután letette a apoptózis. Egy vírus vagy más parazita, amely egy sejtben megszorozódik, elpusztítja: a sejt lysezi, tartalmát kifelé, az intercelluláris térbe. Néhány intracelluláris paraziták, köztük protozoon Toxoplasma gondii (toxoplazmózis kórokozó), amely képes gátolni az apoptózis. A paraziták új generációja rohant a szomszédos sejtekbe, és egyre több kárt okoz a szervezetben. Gyulladásos folyamat kezdődik, amelynek kimenetele lehet mind a szervezet helyreállítása, mind a szervezet halála. A nekrotikus halál is okozhat fizikai vagy kémiai károsodás, mint például égések, vagy fagyás, szerves oldószerek, hipoxia, mérgezés, és más hipotóniás sokk.
A gyulladás jelenlétét vagy hiányát az állatokban olyan jelként használják, amely megkülönbözteti az apoptózist a nekrózistól.
Nekrózis jellemzi törés és citoplazmás membránokat, ami lebomlását organellumok, felszabadulását lizoszomális enzimek és a kimenet a citoplazma tartalmának az extracelluláris térben (ábra. 1). Amikor apoptózis konzervált membrán integritásának, organellumok jelennek morfológiailag érintetlen, és a sejtek hasítási termékek, az apoptotikus sejtek (vagy vezikula) képviselnek fragmensek, egy membrán veszi körül (ábra. 1).
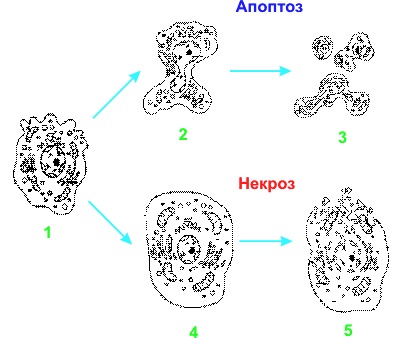
Ábra. 1. Változások a ultrastruktúráját állati sejt nekrózis és apoptózis. 1 - a sejtek normális, 2 - zsugorodása apoptotikus sejtek alkotnak hólyagos outgrowths 3 - fragmentálódása apoptotikus sejtek alkotnak vezikulumokat, 4 - duzzanat sejtelhalás, és 5 - nekrotikus sejt szétesés
A legtöbb tudós egyetért abban, hogy az apoptózis a sejtmagban lévő kromatin enzimatikus bomlása eredményeképpen következik be, és az endonukleáz sejtek kezdik a DNS molekulát a mono- és oligomerek létrehozására. A nukleáz elleni támadás nemcsak euchromás. hanem a mag spirális kondenzált heterokromatikus régiói is. Ennek a folyamatnak a megkezdéséhez a sejtnek enzimeket - nukleázot kell termelnie, és ennek érdekében a transzkripció folyamata (RNS bioszintézis) és a transzláció (fehérje bioszintézis) fokozódik a sejtben. Vannak adatok arról, hogy a fehérjeszintézis gátlói - a ciklohexamid és a puromicin - megakadályozzák a kromatin enzimatikus bomlását, és megakadályozhatják vagy késleltethetik az apoptózis folyamatát. Jelenleg számos módja van az apoptózisnak.
Először is ez a módja az internukleozomális terek enzimes emésztésének és a 200 nukleotid fragmensek
2) másodszor, kromatin hetero-kromatizálás DNS-vágás nélkül
Bővebben: STAGE - Nucleált kromatin-nukleázokra és / vagy kondenzációs enzimekre kifejtett hatások
Információ az "Apoptózis - programozott sejthalál" munkájáról