Miért nem egyezik meg mindig a valence számszerű értéke az elektronok számával a külsővel?
a kémiai kötések kialakulása az atomban lévő párosított elektronok jelenlétében lehetséges. sok elemnél nem minden elektronikus elektron elektron szintje párosul.
például az oxigén és a kén atomjai, hat elektron a külső szinten, de közülük csak kettő párosul:
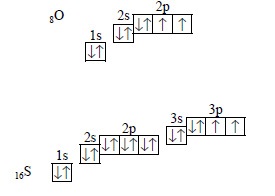
Azonban a külső elektron szintjén még mindig vannak üres 3d orbitálok a kénatomban, amelyhez a 3s és 3p pályák elhaladhatnak, így a kén atom hat párosított elektron lesz:
ezért a kén maximális hatékonysága hat, vagyis egybeesik az elektronikus elektronok számával. a második szinten lévő oxigénatomban nincsenek d-orbitálok, ezért nincs lehetőség az elektronok párosításra, és az oxigénérték nem lehet kettőnél, vagyis nem egyenlő az elektronok számával a külső szinten.
A probléma a fejezet 2. fejezet Periodikus törvény és rendszeres rendszer I. Mendeleyev alapján az elmélet az atom szerkezetét. (problémákat az §1-3-ig) a kémiai témáról a Chemistry 11, Rudzitis, Feldman (11. fokozat)
Ha nincs megoldás erre a problémára, ne aggódjon. Rendszergazdák megpróbálják kiegészíteni a webhelyet azokkal a feladatokkal és feladatokkal kapcsolatos megoldásokkal, amelyekre szükség van, és amelyeket nem adnak át a GDZ-ben végrehajtott remake-ekben és gyűjteményekben. Kérjük, próbálkozzon újra később. Valószínűleg megtalálja, amit keresett :)
Örülünk, hogy minden korosztályú oktatási intézmény hallgatóit örömmel fogadjuk honlapunkon! Itt találsz remastereket és problémamegoldást ingyen, regisztráció nélkül.
davay5.com