Az etilén sorozat telítetlen szénhidrogének, az összetétel általános képlete
Az etilén sorozat telítetlen szénhidrogének. vagy alkének, a CnH2n általános képletű szénhidrogének. amelyek molekulái egy kettős kötést tartalmaznak. C kettős kötés a sp 2-hibridizációs állapotban van, a kettős kötés a -and-kötések kombinációja. Természetéből - a kapcsolat drasztikusan különbözik a kapcsolódástól; - a kapcsolat kevésbé erős, mivel az elektronikus felhők átlapolódnak a molekula síkján kívül.
A legegyszerűbb alkén etilén. Az etilén szerkezeti és elektronikus formái a következők:
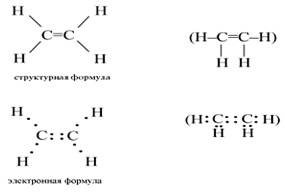
Az etilénmolekulában hibridizálódnak az egy és két p-orbitális C atomok (sp2-hibridizáció). Így minden C atomnak három hibrid pályája és egy nem hibrid p-orbitálisja van. A C atomok hibrid pályái közül kettő átfedésben van, és C-kötést képez az atomok között. A C-atomok fennmaradó négy hibrid pályája ugyanazon a síkon átfedő négy H-atom-orbitálissal, és négy kötést is képez.
A két nem hibrid P-orbitális C-atom átlapol egy olyan síkban, amely merőleges a kötés síkjára, azaz az egyik alakul ki. A reagensek hatására a kötés könnyen megtörik.
Az etilén a homérosz alkén-sorozat első tagja.
De a buténmolekula -2 lehet két térbeli formában - cisz- és transz-:
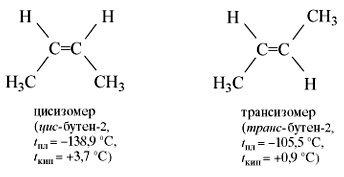
A cisz- és transz-izomerek, amelyek különböző térbeli atomrendezéssel rendelkeznek, számos fizikai és kémiai tulajdonságban különböznek egymástól. Így kétféle szerkezeti izomerizmus lehetséges az alkének számára. a szénlánc izomerizmusa és a kettős kötés helyzete izomerizmusa. Geometriai izomerizmus is lehetséges. Az etilén (eten) színtelen gáz, nagyon gyenge édes illatú, enyhén könnyebb a levegőnél, kevéssé oldódik vízben.
Kémiai tulajdonságai szerint az etilén élesen különbözik az etántól, amely molekulájának elektronikus szerkezete miatt következik be. Miután a molekulában egy kettős kötés kötődik-és-kötésekből áll, az etilén képes két monovalens atomot vagy gyököket összekapcsolni a szakadási kötés miatt.
Az addíciós reakciók képessége minden alkénre jellemző.
Ha bróm (brómvíz formájában) adunk az alkénhez, a bróm barna szín gyorsan eltűnik. Ez a reakció minőségi kettős kötés esetén.
Ha az eredeti alkén aszimmetrikus, akkor a reakció a Markovnikov-szabály szerint folytatódik.
A hidrogén-halogenidek telítetlen vegyületekhez történő hozzáadása egy ionos mechanizmussal történik.
4. Víz hozzáadása (hidratációs reakció):
Ezt a reakciót etil-alkohol előállítására használják az iparban.
Az alkánokat oxidációs reakció jellemzi:
1. Az etilén könnyen oxidálható már szokásos hőmérsékleten, például kálium-permanganát hatására. Ha az etilént átvezetik KMnO4 kálium-permanganát vizes oldatán. akkor az utóbbi jellegzetes ibolyaszínűsége eltűnik, etilén oxidációja kálium-permanganáttal (kvalitatív reakció kettős kötésre):
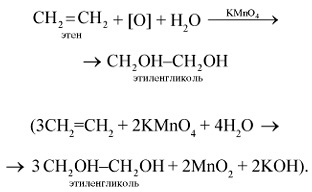
2. Az etilén éghető fényes lánggal, hogy szén-monoxidot (IV) és vizet képezzen:
3. Az etilén részleges oxidációja levegő oxigénnel nagy ipari jelentőséggel bír:
Az etilén esetében, mint minden telítetlen szénhidrogén esetében, a polimerizációs reakciók jellemzőek. Ezek magas hőmérsékleten, nyomáson és katalizátorok jelenlétében fordulnak elő:
A polimerizáció az azonos molekulák szekvenciális kombinációja nagyobbakká.
Így az etilént és homológjait az adagolás, oxidáció és polimerizációs reakció jellemzi.