III
§ 6. aminosavak szerkezeti blokkok fehérjék
Aminosavak az élő szervezetekben előforduló elsősorban a készítményben a fehérjék. A fehérjék épülnek elsősorban a húsz standard aminosav. Ezek az a-aminosavak és a különböző struktúrája oldalcsoportok (gyökök), által kijelölt R betű:
A különböző aminosav oldalán gyökök kulcsszerepet játszik a kialakulását a térszerkezet a fehérjék működését az aktív centrum az enzimek.
A szerkezet a szokásos aminosavak utalnak, hogy a végén a szakasz a 3. táblázatban. Természetes aminosavak triviális nevek működnek felvételei fehérje szerkezetének kényelmetlen. Ezért bevezették a hárombetűs és egybetűs elnevezések, amelyek szintén a 3. táblázat mutatja.
Minden aminosav, kivéve a glicint, egy-szénatom királis, azaz jellemzi őket optikai izomerek. Táblázat. 3 királis szénatom csillaggal jelölt. Például, az alanin mindkét izomerre Fischer projekciós a következőképpen:
Azok jelölésére, mint a szénhidrátok, melyeket a D, L-nómenklatúra. A fehérjék szerkezete tartalmaznak csak L-amino-savakat.
L- és D-izomerek kölcsönösen egymásba alakíthatók. Ezt a folyamatot nevezik racemizálódást.
Aminosavak tartalmaznak az amino- és karboxil-csoportokat. Emiatt, mutatnak amfoter tulajdonságokkal, azaz, tulajdonságok, és a savak és bázisok.
Amikor vízben oldjuk aminosavak, például glicin, a karboxicsoportja disszociál alkotnak hidrogén-ion. Ezután egy hidrogénion csatlakozik miatt nem megosztott elektronpárt a nitrogénatomon az aminocsoport. Ion képződik, amely egyszerre van jelen a pozitív és negatív töltések, úgynevezett kettős ion:
Ilyen aminosavak a túlsúlyban formában egy semleges oldat. Az aminosav közegben csatolásával, a hidrogénion, kation formák:
Lúgos környezetben képződik anion:
Így attól függően, pH aminosav lehet pozitív töltésű, negatív töltésű és elektromosan semleges (azonos pozitív és negatív töltések). A pH, amelyen a nettó töltése az aminosav nulla, az úgynevezett izoelektromos pontja az aminosav. Sok aminosavak az izoelektromos pont pH = 6 Például, az izoelektromos pontot a glicin és alanin van értékek 5,97 és 6,02 volt.
Két aminosavak egymással reagálnak, miáltal a víz molekula lehasad, és a termék kialakítása, amely az úgynevezett egy dipeptid.
Bond összekötő két aminosav az úgynevezett peptid-kötés. Ha szó jelölést az aminosavak, a kialakulása egy dipeptid sematikusan az alábbiak szerint:
Hasonlóképpen, tripeptidekből tetrapeptidek, stb.:
H2 N - Lys - Ala - Gly - COOH - tripeptid
H2 N - TRP - GIS - ala - ala - COOH - tetrapeptid
H2 N - Tyr - Lys - Gly - Ala - Leu - Gly - TRP - COOH - heptapeptid
Peptideket tartalmaznak, amelyek egy kis számú aminosav-maradékok, oligopeptidek van egy közös név.
Érdekes tudni! Sok oligopeptidek nagy biológiai aktivitását. Ezek közé tartozik számos hormon, például az oxitocin (nanopeptid) stimulálja a méh-összehúzódások, bradikinin (nanopeptid) gátolja a gyulladásos folyamatok a szövetekben. Antibiotikum gramicidin S, (gyűrűs dekapeptid) adja a szabályozása ionáteresztő képesség a membránban a baktériumok, és ezáltal elpusztítja azokat. Gombás toxinok amanitin (oktapeptid) blokkolásával a fehérje szintézisét, okozhat súlyos mérgezést emberben. Széles körben ismert, Aszpartám - aspartylphenylalanine-metil-észter. Az aszpartám édes ízű, és használják édes ízt a különböző élelmiszerek és italok.
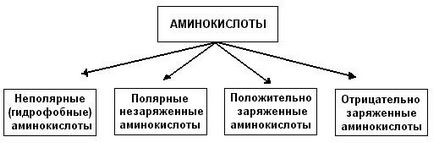
Számos megközelítés, hogy a besorolás a aminosavak, de a legelőnyösebb egy olyan alapuló osztályozás szerkezete a gyökök. Vannak négy osztályát tartalmazó aminosavak a gyökök a következő típusú; 1) a nem-poláros (vagy hidrofób); 2) poláros töltetlen; 3) negatív töltésű, és 4) pozitív töltésű:
A nem poláros (hidrofób) aminosavak közé tartozik az alifás apoláros (alanin, valin, leucin, izoleucin) és aromás (fenil-alanin és a triptofán) R-csoportok és egy kénatomot tartalmazó aminosavat - metionin.
Töltés nélküli poláros aminosavak képest nempoláros jobban oldódnak vízben, több hidrofil, mivel a funkciós csoportok hidrogénkötéseket képeznek vízmolekulák. Ezek közé tartoznak az aminosavak, amelyeknél poláros HO-csoportot (szerin, treonin és tirozin), HS-csoport (cisztein), amidot (glutamin, aszparagin) és glicin (R-csoport glicin, látva egy hidrogénatom túl kicsi ahhoz, hogy kompenzálni erősen poláros egy-amino- és a-karboxil-csoport).
Aszparaginsav és glutaminsav negatív töltésű aminosav. Ezek két karbonsav és egy aminocsoport, így ionizált állapotban a molekula lesz a nettó negatív töltése:
Tartozik a pozitív töltésű aminosavak a lizin, hisztidin és az arginin az ionizált formában, hogy van egy pozitív töltéssel:
Jellegétől függően a gyökök természetes aminosavak is sorolják semleges, savas vagy bázikus. Alkalmazásához semleges apoláros és poláros töltetlen, savanyú - negatív töltésű, a fő - a pozitív töltésű.
Tíz a 20 aminosav alkotó fehérjéket megszintetizálhatjuk az emberi szervezetben. A többi között kell szerepelnie ételeinket. Ezek közé tartozik az arginin, valin, izoleucin, leucin, lizin, metionin, treonin, triptofán, fenil-alanin és a hisztidin. Ezek az aminosavak az úgynevezett esszenciális. Az esszenciális aminosavak gyakran az élelmiszer-adalékanyagok, a gyógyszerként felhasznált.
Érdekes tudni! A döntő szerepe van az erőviszonyok az emberi aminosavakat. A hiánya az esszenciális aminosavak a diéta a szervezet megsemmisíti önmagát. Ebben az esetben, az első szenvednek az agy, ami a különböző betegségek, a központi idegrendszer, a mentális zavarok. Különösen veszélyeztetett fiatal növekedési szervek. Például, megsértve a szintézise tirozin származó fenilalanin gyermekek fejlődő betegség súlyosabb finilpirovinogradnaya mentális retardáció, hogy okoz súlyos mentális retardáció vagy halált a gyermek.