oxidáció mértékét
lecke Célok
- tovább tanulmányozza a vegyérték, megtudja, a szerzett ismeretek alapján a atomok elektronszerkezete és kémiai kötéssel, hogyan megkomponált képletek anyagok.
lecke célkitűzések
• Képzés: továbbra is tanulmányozzák a vegyérték hogy mit oxidáció mértéke, hogy fontolja meg álláspontját, valamint megtanulják, hogyan kell meghatározni az oxidációs foka az atom vegyület;
• iskolai: tanítani előállítási eljárására és összehasonlítása, a készségek fejlesztése önálló munka, hozzájárulnak a logikus gondolkodás;
• Oktatási: létrehozni egyfajta tolerancia.
Fontos kifejezések
- Az oxidáció mértéke - a töltés kondicionált atomok jellemző száma teljesen vagy részlegesen eltolódott elektronpár vagy elektronok az egyik atom egy másik kémiai vegyületek.
- Kémiai képlet - jelképe anyagok szerkezetét és kémiai összetétele révén kisegítő és numerikus karakterek és szimbólumok a kémiai elemek.
Ellenőrzés házi
1., amelyben van egy nem-poláris molekulái kovalens kötés?
2) Egy molekula képződését kovalensen - apoláros kötések alkotják az hármas kötést?
• D) az időszak számát.
oxidáció mértékét
Először is, ne felejtsük el, amit a vegyérték.
Az oxidációs állapot - fontos jellemzője az állam egy atom a molekulában. Vegyértékét száma határozza meg a párosítatlan elektronok az atom csak a gerjesztési egy atom. Magasabb vegyértékű elem, általában egyenlő a csoport szám. A vegyületek oxidációja különböző kémiai kötések képződött egyenlőtlenül.
Az oxidációs a molekulák különböző kémiai kötéseket a következőképpen alakult:
1. A vegyületek az ionos kötés oxidációs elemek az ion töltése. Ennek egy példája látható az 1. ábrán.
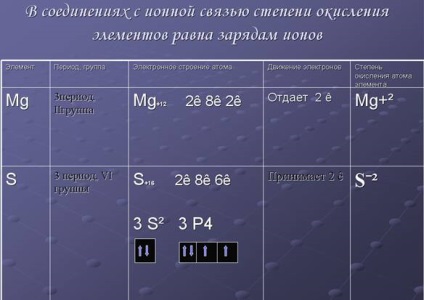
1. ábra. Illusztráció Az oxidáció mértékét az elemek a vegyületek ionos kötésekkel.
2. A vegyületek a nem-poláros kovalens kötés (a molekulák egyszerű anyagok) oxidációs állapota 0 elemek.
H20, SI20, F20, S0, AI0
3. Az oxidáció mértéke a molekulák kovalensen kötődni poláris molekulák határozzák meg a hasonló ionos kémiai kötéssel.
Az oxidáció mértéke az elem - ez kondicionált díjat tartalmaz a molekulában, ha azt feltételezzük, hogy a molekula áll ionok.
A mértéke az oxidációs, ellentétben vegyérték van egy jel. Ez lehet pozitív, negatív és zérus. A 2. ábra a típusú oxidáció.
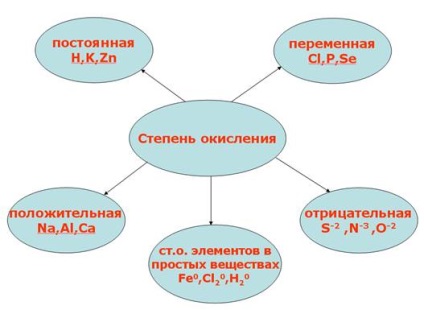
Ábra. 2. Az oxidáció mértéke.
Valcncy által kijelölt római számokkal felső elem szimbólum, és az oxidáció mértékét jelzi arab számok a díjat az elem szimbólum (3. ábra).

Ábra. 3. rendeltetése vegyérték és oxidációs állapota.
Egy és ugyanaz az elem lehet különböző oxidációs fokú. Így, A 4. ábra a fokát kén oxidációs.

Ábra. 4. A mértéke kén oxidációs.
Most nézzük meg a meghatározását az oxidáció mértékét az oxidok:
A pozitív oxidációs állapotú az elektronok száma. amelyek adott adatok atom. Atom adhat az összes vegyérték elektronok csoportnak megfelelő a számát, amelyben az elem, ezáltal mutatva magasabb oxidációs fok (kivétel OF2).
Negatív oxidációs számát egyenlő az elektronok száma, amelyek szerint vett atom (az ábrákon csak a nemfémek). Nemfémes atomok kapcsolódnak az elektronok száma, amely addig, amíg a befejezése a külső réteg hiányzik, így mutató negatív erő.
Az 5. ábrán példaként a magasabb és az alacsonyabb oxidációs fokú.

Ábra. 5. A magasabb és alacsonyabb oxidációs fok.
Oxidációs közötti érték magasabb és alacsonyabb oxidációs fok nevezett közvetítők (6. ábra):

Ábra. 6. A köztes oxidációs állapotban.
A vegyületek nem-poláros kovalens kötés (a molekulák egyszerű anyagok) oxidációs állapotban van 0 elemek: H20, SI20, F20, S0, AI0
Annak meghatározására, az oxidáció mértékét az atom a vegyületben kell vizsgálni számos pozíciót (7. ábra).

Ábra. 7. A rendelkezések figyelembe kell venni, hogy meghatározzuk az oxidáció mértékét az atom a vegyületben.
Nagyon hamar, akkor fogják bevezetni, hogy az oxidációs-redukciós reakciók:
Előállítása A általános képletű vegyület
Számos módszer előállítására a általános képletű vegyület oxidációját, de kezdetben figyelmét az algoritmus, és általában ezek előállítása (8. ábra):

8. ábra. Az algoritmus rajz kémiai képletek oxidációt.
Lássuk, hogyan kell előállítani oxidok képlet:
Az első módszer kidolgozásának általános képletű:
1. Az első helyen az elem van írva egy kisebb eiektronegativitás a második egy nagyobb elektronegativitási.
2. tétel írva az első helyen van egy pozitív töltés, „+”, a második negatív töltés „-”.
3. Határozza meg az egyes elemek oxidációs állapotban van.
4. Keresse közös többszöröse az érték az oxidációs fokú.
5. Osszuk a legkisebb közös többszöröse az érték a oxidáció mértékét, és kapott indexek tulajdonítható, hogy a jobb alsó után a szimbólum a megfelelő elem. A 9. ábra egy példát mutat be az elem:
Ábra. 9. példa 5 bekezdés összeállítása képletek.
6. Ha az oxidáció mértékét egy még - páratlan, ezek az ikon mellett a jobb alsó kereszt - bölcs anélkül, hogy a „+” és „-”. Példa, hogyan kell végrehajtani az elem, a 10. ábrán látható.
Ábra. 10. példa 6, bekezdés összeállítása képletek.
7. Ha az oxidáció mértékét egy még értéke, először meg kell csökkenteni a legkisebb értékét az oxidáció mértékét, és tegye kasul - át anélkül, hogy a „+” és „-”: C + 4 O 2. Egy példa arra, hogyan kell felhívni ilyen vegyületek adják a 11. ábrán.
Ábra. 11. példa 7, bekezdés összeállítása képletek.
A második módszer a készítmény a képlet:
1. Jelöljük oxidációs állapot N keresztül X, jelzik az oxidáció mértékének O: N2x O3-2
2. Határozzuk meg a mennyiségét negatív töltések, az oxidációs foka oxigén többszörösen oxigén-index: 3 • (-2) = -6
3. A elektromosan semleges molekula volt szükség, hogy meghatározzuk a mennyiségét pozitív töltések: X2 = 2X
4.Sostavit algebrai egyenlet (12. ábra).
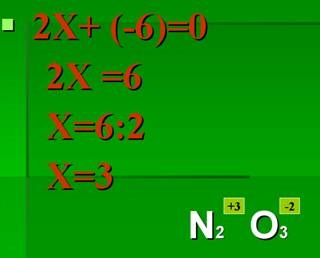
12. ábra. Elkészítése egy algebrai egyenlet.
1. Oxidációs töltés feltételesen kémiai elem atomok a vegyület, amelynek kiszámítása azon a feltételezésen, hogy a csatlakozások kizárólag az alábbiak ionok.
2. oxidációs lehet pozitív, negatív vagy nulla értékek, amelyeket általában fölött elhelyezett, a tetején a szimbólum elem.
3. A pozitív oxidációs állapotban egyenlő az elektronok száma, hogy megadott adatok atom.
4. A negatív oxidációs számát egyenlő az elektronok száma, amelyek szerint vett atom (az ábrákon csak a nemfémek).
Az ellenőrző egység
1. Mi az oxidáció mértéke?
2. Milyen típusú oxidáció?
3. Mi egy köztes oxidációs állapotban?
4. Hogyan hozzunk létre egy képletet az ízületek?
házi feladat
Adja meg a nevét a következő bináris vegyületek. Cl2O7, Cl2O, ClO2, FeCl2, FeCl3 MnS, MnO2, MnO, MnCl4, Cu 2O, Mg2Si, Na3N, Fez.
Írja képletű anyagok, amelyek az alábbi elemeket tartalmazza:
1. F és G
2. N és H
3. Zn és Cl
A szabályok meghatározására oxidáció mértéke
Ennek feladata a tanulság az, hogy vezessenek be egy témát, mint az oxidáció mértékét. Nézzük Összefoglalva magával, és ismét felidézni a meghatározása az oxidáció mértékét.
Azt már tudjuk, hogy az oxidációs állapotot nevezik feltételes atomot és egy kisegítő felelős a kémiai elem a vegyület, amely ki volt számítva egy ilyen javaslat, amelyben az összes ionos és kovalens - poláros vegyületek állhatnak csupán ionok.
A ítélete az oxidáció mértékét a különböző elemek hasznos lehet:
• Először is, az elrendezés a vegyi anyagok osztályozásának;
• másodszor, a leírását vegyi anyagok sajátosságait;
• Harmadszor, a vegyületek előállítására képletek vegyi anyagok és ezek nómenklatúrája;
• Negyedszer, az oxidáció mértékét, és elég gyakran használják, ha dolgozik az oxidációs - redukciós reakciókat.
A legtöbb esetben, az oxidáció mértékét az atomok anyagok a bonyolult szerkezetű eredetileg által kijelölt jel, majd egy számot. Rendeltetése számok lehetnek a +1, +2, -2 és mások.
Ha feltételezzük elképzelhető, hogy a vegyület van az ion töltése, ebben az esetben meg kell adni a számot először, majd aláírja.
De ahhoz, hogy megtalálják az oxidáció mértékét, vannak bizonyos szabályok. Vessünk egy közelebbi pillantást ezeket a szabályokat.
Így mértékének meghatározására oxidációs az atomok szükséges betartani a következő szabályokat:
• Először, egy egyszerű anyagok atomok oxidációs fokú nullával egyenlő;
• Másodszor, az algebrai összege oxidációs állapotok a semleges molekula is nulla. De az ionok egyenlő az algebrai összege felelős ion.
• Harmadszor, gyakorlatilag az összes vegyületek hidrogén lesz egy oxidáció mértéke, amely egyenlő 1, azzal az eltéréssel, hidridek aktív fémek. Ezek CO lesz egyenlő -1.
• Negyedszer, ha figyelembe vesszük, az oxigén atomot tartalmaz a CO = -2 vegyületek. Ezután kivétel OF2 és peroxidok a fémek és ennek megfelelően ebben az esetben az oxigén CO egyenlő +2 és -1.
• Ötödször, ha komplex vegyületek, jelezzük a központi atom.
• A következő szabály alkálifém. Ha az előírtnál az elemek az első csoport a fő csoport, a CO = 1. De a terméket a második csoport, amelyek magukban foglalják az alkáliföldfémek a vegyület lesz egy oxidációs állapotú +2. Alumínium SB = 3, A = -1 fluoratom.
• Ha tekinteni kovalens vegyület, a elektronegatívabb atom mindig jelzi az oxidáció mértékét a „-” jel. De vegyületek kevésbé elektronegatív atom egy „+” jel.
• Ha figyelembe vesszük az egyszerű ionos vegyületek, ezek oxidációs foka és egyenlő nagyságú és jele az a tény, hogy van egy elektromos töltés.
Most egy közelebbi pillantást a szabályok köztes oxidációs állapotok:

De meg kell jegyezni, hogy ezeket a szabályokat kell követni, ha van dolgunk állandó oxidációs állapotban van. Abban az esetben, ha egy kémiai elem egy változó, általában függ a sorrendben és típusú atomok ez a vegyület.
Esettanulmány
1. Ön mivel a képlet a kémiai elemek. Határozzuk meg az oxidáció mértékét a fenti általános képleteknek.
2. Ebben a feladatot kell meghatározni az oxidációs állapotban bemutatott mielőtt kémiai elemek a bináris általános képletű vegyület.

3. Itt kerülnek bemutatásra képleteket. Mik azok kapcsolatok:

4. A nevek ezen anyagok szükséges ahhoz, hogy a képlet:
