alumínium-nitrát képlet Chemistry
alumínium-nitrát normál körülmények fehér színű szilárd anyag formájában (ábra. 1), amely hevítés hatására elbomlik.
Igen jól oldódik vízben (hidrolízisét a kation). Ez feloldjuk salétromsavban. Ez reagál bázisokkal, ammóniával hidrát.

Ábra. 1. Nitrát alumínium. Megjelenés.
A kémiai képlete az alumínium-nitrát
A kémiai képlete alumínium-nitrát Al (NO3) 3. Ez azt mutatja, hogy a szerkezet a molekula tartalmaz egy alumínium-atom (Ar = 27 amu), három nitrogénatom (Ar = 14 amu) és kilenc oxigénatomokat (Ar = 16 AU m.). Szerint a kémiai képlet számított molekulatömege alumínium-nitrát:
Úr (Al (NO3) 3) + 3 = 27 × 14 + 9 × 16 = 27 + 42 + 144 = 213.
Grafikus (szerkezeti) általános képletű alumínium-nitrát
Structure (grafikus) általános képletű alumínium-nitrát több intuitív. Ez azt mutatja, hogy az atomok vannak csatlakoztatva egymáshoz a molekulán belül:
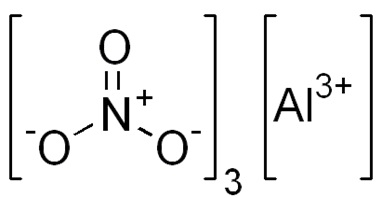
ionos képletű
Alumínium-nitrát egy elektrolit, amely disszociál ionokra vizes oldatban az alábbi reakcióegyenlet:
Példák problémák megoldása
Korlátozásával neutralizáló 25,5 g egybázisú sav feleslegét különítettek 5,6 l (STP) gázt nátrium-hidrogén-karbonát-oldattal. Határozza meg a molekula képletét a sav.
Az egyenlet semlegesítés korlátozó monosav feleslegben alkalmazott nátrium-karbonát-oldattal, egy általános formája:
Kiszámítjuk a anyagmennyiség a reakció során felszabaduló szén-dioxid:
n (CO2) = 5,6 / 22,4 = 0,25 mól.
Kiszámítjuk a móltömeg korlátozó egybázisú sav:
Definiáljuk a szénatomok száma a molekulában korlátozó egybázisú sav (értékei a relatív atomi tömegeket vett Mendeleev Periódusos Táblázat egész számra kerekítve: 12 - a szén-dioxid, 1-16 hidrogén és oxigén):
M (CnH2n + 1 COOH) = 12N + 2n + 1 + 12 + 16 + 16 + 1 = 14n + 46;
14n + 46 = 102 g / mol;
Ez azt jelenti, molekuláris képlete korlátozó egybázisú sav C4 H9 COOH.