Colloid mint gyógyszer - stadopedia
Az ilyen idegen hangzású "kolloid" szó a görög "cola" - ragasztóanyagból származik. A kolloidok más néven ismertek minket. Tehát a szervezetben lévő nagy fehérjék, poliszacharidok és nukleinsavak molekulái nem más, mint a kolloidok.
"A vér, a bőr és a többek a kolloid rendszerek" - magyarázza Marcus Antonietti professzor a Colloids és a határfelületek tanulmányozásával foglalkozó Max Planck Intézet munkatársa. - Magától értetődik, hogy a természet mint modell, amikor kolloidokat hozunk létre. Közben különböző molekulákkal tudunk működni. "
A polimerek kémiai területén új szintézis módszerek váltak lehetővé, amelyek segítségével a kémiai rendszert részecskékké vághatjuk, amelyek méretei a nanometer tartományban vannak. Így a tudósok polisztirolból készült kolloid gyöngyöket állíthatnak fel, amelyeken több ezer csápszerû akceptort csatolnak. A sztirolból és vinil-piridinből álló blokk polimer ilyen csapdái lehetővé teszik például, hogy "higanyhúzzák" a vérből a higanyt mérgezés során. Az így kialakított kolloidok rendkívül reaktívak. A nehézfém-ionokat tömegük legfeljebb 16% -ában képes megkötni.
Jelenleg az úgynevezett liposzómákat már használják az orvostudományban. A liposzómák olyanok, mint a kiskapszulák. Ezek egy burkoló membránból és egy belső üregből állnak, amely egy vízben vagy olajban oldható hatóanyaggal van feltöltve. Mivel a liposzóma membrán szerkezetét sejtmembránok tekintik a saját, kisebb járműveket kapszula kevesebb problémát leküzdésében a bőr természetes gáton, mint a „csomagolatlan” hatóanyagok. A felső bőr mély rétegeiben a liposzómáknak meg kell adniuk a hatóanyag terhelését a sejtekhez, és meg kell erősíteniük az intercelluláris térüket az üres héjjal.
A liposzómák vagy a lipid vezikulumok hosszú időn át ismertek, és valószínűleg mindenki ismeri egymást: nagyon hasonlítanak hozzájuk azok a cseppecskék, amelyek bejutnak a vízbe, de természetesen tisztán külső. A liposzómák zárt vizes buborékok, amelyeket egy vagy több lipidréteg vesz körül. A liposzómák mérete és alakja számos tényezőtől függ: a táptalaj savasságától, a sók jelenlététől és hasonlókatól. Az angol kutató Alec Bangem és munkatársai először 1965-ben felhívták a figyelmet rájuk. Észrevették, hogy a liposzómák (ez a név három évvel később született) nagyon emlékeztetnek a sejtmembránokra. Ezekben az években már ismert volt, hogy a sejtmembránok számos funkciót teljesítenek, és a liposzómák azonnal a vizsgálatuk fontos eszközévé váltak. A membránok modelljeként a liposzómák lehetővé tették számos tulajdonságuk vizsgálatát: elektromos ellenállóképesség, vízmolekulák, ionok és egyéb töltött részecskék permeabilitása, valamint a sejtek tartalma. A liposzómákat ezenkívül a vitaminok, hormonok, antibiotikumok és más gyógyszerek membránjának hatására tanulmányozzák. Ez a szempont a kutatók legnagyobb figyelmet szentelte, mivel kiderült, hogy a liposzómák jól szembesülnek a kábítószer hordozók szerepével.
A liposzómák lehetnek egyrétegűek (átmérő: 250-300 angström) és többrétegű (5,50 mikrométer). Árnyékos hangok - a víz, a fény - bimolekuláris lipidréteg elhelyezkedése, az alkotó molekuláinak "farka" fordított a rétegben.
Milyen tulajdonságai vannak a liposzómáknak előnyben részesítve őket a kábítószerek más hordozóihoz képest? Először is ez a természetes sejtmembránokhoz való kötődés a kémiai összetétel szempontjából. Ismeretes, hogy a membránokat tartalmazó lipidek tömegük 20-80% -át foglalják el. Ezért a liposzóma komponensek megfelelő megválasztásával a szervezetbe való beadása nem okoz negatív reakciókat.
A liposzómák második fontos tulajdonsága az egyetemesség. A félszintetikus jelleg miatt a méretük, jellemzőik és felületi összetételük széles körben változatos lehet. Ez lehetővé teszi a liposzómák számára a farmakológiailag aktív anyagok széles körének átvitelét: tumorellenes szerek és antimikrobiális szerek, hormonok, enzimek, vakcinák, valamint a sejt, genetikai anyag további energiaforrásai.
Harmadszor, a liposzómák viszonylag könnyen bomlanak le a szervezetben, hogy kiadja az anyagot szállítani, de az utat maguknak a liposzómáknak mentes antigén tulajdonságokkal, megbízható kikötő és a rakomány való érintkezéstől az immunrendszert, és ezért nem okoz a védő és az allergiás reakciók.
Fontos szerepet játszik a liposzómák sejtekkel való kölcsönhatásának természete is. Sokféle formát ölthet: a legegyszerűbb - a liposzómák adszorbeálódnak (csatolva) a sejtfelszínhez. Az eset véget érhet, és továbbhaladhat: a sejt elnyeli a liposzómát (ezt a lenyelés folyamatát endocitózisnak nevezik), és vele együtt a leadott anyagok belépnek a sejtbe. Végül a liposzómák egyesülhetnek a sejtmembránokkal és részévé válhatnak. Ebben az esetben a sejtmembránok tulajdonságai megváltozhatnak: például viszkozitása és permeabilitása, az elektromos töltés nagysága. A membránokon áthaladó csatornák számát növelheti vagy csökkentheti. Így a liposzómáknak köszönhetően megjelenik a sejt célzásának új módja, amelyet "membrántechnikának" nevezhetünk.
Interakciók a liposzómák a sejtmembránnal: liposzóma növelheti a permeabilitása a membrán - okoz a formáció további csatornák (I); köthető az adszorbeált (II) membránhoz; fontos formája a kölcsönhatás - a liposzóma-felvétel a sejt által, ebben az esetben egy anyag hozta liposzóma esik közvetlenül egy cella (III); néha a sejtmembrán és a kicserélt liposzóma lipidek (IV), és más esetekben, a liposzóma membrán és a sejt biztosíték (V) hivatkozva hordozók liposzóma hatóanyag-legszélesebb körben használt kísérleti onkológiában. A lényeg az, hogy számos olyan gyógyszer van, amelyek nagyon hatékonyak a rosszindulatú sejtek elpusztításában vagy növekedésük gátlásában. Azonban terápiás célokra való alkalmazásuk nem mindig lehetséges, mivel nagy a toxicitása vagy rossz vízben való oldhatósága. A liposzómák használatával ezek a nehézségek megoldhatók. Ily módon egy laboratóriumi egereket beadhatók liposzómákkal, leukémia, keverhető készítmények és a növekedés visszamaradását észlelték a rosszindulatú sejtek számát. Más kutatók töltött liposzómákat antraciklin: ezek az anyagok az aktív széles választékával szemben a rosszindulatú daganatok, de nagymértékben toxikus az egyéb szövetekben, különösen a szívizmot, - és a káros hatások a fenti vegyületek jelentősen csökkent, ami ennek eredményeként jelentősen növelheti a dózist.
A liposzómák a fertőző betegségek leküzdésére is felhasználhatók. A gyakori leishmaniasist antimon gyógyszerekkel kezelik, amelyek nagyon toxikusak. De amikor beléptek a kísérleti állatok liposzómák alkalmazásával, majd kezdték, hogy elnyomja a szorzás a kórokozók a májsejtekben százszor hatékonyabb, mint a szokásos, és a toxikus hatások a szív és a vese jelentősen csökkent, ami lehetővé tette, hogy növelje az adagot a gyógyszer. Hasonló eredményeket értek el a leishmaniasishoz hasonló gombás betegségek - cryptococcosis és histoplasmosis kezelésében.
Amikor mikroorganizmusok - patogének „rejtett” a sejteken belül, így védve vannak mind az immunrendszer (antitestek), és a gyógyszerek hatásának. Néha a makrofágok, a patogén baktériumok felfogása után, nem képesek megemészteni őket. Minden ilyen esetben, a betegség egyre elhúzódó, krónikus lefolyású, és akkor van szükség, hogy a korrekciós intézkedések be tud hatolni a fertőzött sejtekben, és a kívánt koncentrációban a kezelés. A kísérletek eredményei egy csoport amerikai kutatók, akik dolgoztak makrofágokkal fertőzött egerek baktérium egér tífusz, kimutatták, hogy a liposzóma és a sokkal növekedése a kezelés hatékonyságát: hoztak makrofágok antibiotikum cefalotin, és a baktériumok számát a sejtek belsejében sokkal nagyobb mértékben csökkent, mint a feldolgozás az azonos sejtek tiszta antibiotikum. Ugyanakkor nagyon magas koncentrációt értek el a sejteken belül, azaz pontosan ott, ahol a kórokozók találhatók.
A liposzómákba ágyazott gentamicin antibiotikumot használó egyéb kutatók ugyanolyan eredményeket értek el a brucellózis kórokozók ellen, mind a sejttenyészetben, mind pedig a tengerimalac állatokon végzett kísérletekben.
Így a liposzómák segítenek fenntartani a vérben és a sejtekben a kábítószerek magas koncentrációját, és segítenek abban, hogy behatoljanak olyan területekre, ahol liposzómák nélkül nem képesek.
Interakciók a liposzómák és a sejtek, nagyrészt képesek leküzdeni néhány anatómiai korlátok a test, különösen a falak, a gyomor-bél traktus. Ezt a körülményt a cukorbetegség kezelésére használták azáltal, hogy az inzulint preorálisan liposzómákban adták be. A kísérleteket patkányokon, amelyek korábban mesterségesen előidézett diabétesz, és azt találtuk, hogy a bevezetése inzulin liposzómákba csökkenését okozta vércukorszint az állatokban, mivel a liposzómák megvédje a hormon a pusztulástól emésztőrendszerben. Jelenleg az ebben az irányban folytatott kutatás folytatódik. Céljuk -, hogy elérjék azt a lehetőséget cukorbetegség inzulin injekcióval a szájon keresztül, akkor lesz egy nagy áldás a betegek ezt a súlyos betegséget.
Kísérleteket tettek más anyagok ezen módszerrel történő bevezetésére. Nem mindig voltak sikeresek, de egyes esetekben kétségtelen sikereket értek el. Így állatokon végzett kísérletekben az interferon termelés aktivátorai bejuthatnak a liposzómába a gasztrointesztinális traktuson keresztül, amely trombita területet, K-vitamint és más anyagokat elpusztít. Számos gyógyszer bejuttatása a szervezetbe nagyon ígéretes, különösen azokban az esetekben, amikor az injekciók kevésbé kívánatosak vagy akár lehetetlenek. De még nem tisztázott, hogy a liposzómák bizonyos anyagai miért mennek keresztül a bélfalon, míg mások nem. A jelenség mechanizmusát jelenleg vizsgálják.
A liposzómák pontos, célzott gyógyszeradagoláshoz azonban bizonyos korlátozások vannak. Bevétele után a legtöbb liposzóma által abszorbeált sejtek a retikuloendoteliális rendszer, főleg a makrofágok, amelyek képes a vér és elpusztítani idegen anyagok (megemészteni) annak szükségességét, hogy fenntartsák a állandóságának a belső környezet. Ezeknek a sejteknek a legnagyobb felhalmozódása a májban, a lépben, a csontvelőben, a nyirokcsomókban és a véráramban van. Ezért, ha a cél a bevezetése a liposzómák rejlik érintkezik a sejtek a retikuloendoteliális rendszer a probléma alig merül fel: hogy liposzómák (kórokozói a fertőző betegségek, amelynek kezelése beszéltünk fent megtalálhatók ezekben a sejtekben). Ha szükséges, hogy a liposzómák szállítsák tartalmukat más helyekre, akkor nehezebb ezt elérni.
Az utóbbi években végzett tanulmányok azonban lehetővé teszik számunkra, hogy a közeljövőben reménykedjünk ezen akadály leküzdésében.
Az All-Union Kardiológiai Kutatóközpontban, a V.P. Torchilinnal a liposzómák irányított szállítását végeztük a kísérletes myocardialis infarktus zónájába. Ezt a miozint, a szívizom proteint tartalmazó antitestekkel végezték. Az antitestek kémiailag kapcsolódtak a liposzómák felületéhez. A liposzómák mind az infarktus zónában, mind a normál szívszövetben (azaz myosinban) felhalmozódtak, bár ezek jelentős része még mindig a májsejtekben lokalizálódott.
Nagyon hatásos volt a liposzómák intravénás bejuttatása. Ebben az esetben a máj és a lép többszörös liposzómákat kap, mint a peritoneumon keresztül, különösen a bőr alá.
Így a beadás módjainak kombinálásával reménykedhet a sikeres liposzómás kezelés és azoknak a betegségeknek, amelyek kevéssé kapcsolódnak a retikuloendotheliális rendszer sejtjeihez.
A közelmúltban végzett vizsgálatok kimutatták, hogy a makrofág rendszer fontos szerepet játszik a szervezet különböző fertőzésekből és daganatokból történő védelmében. A makrofágok mind a tumorsejteket, mind a vírusok által érintett sejteket elpusztíthatják anélkül, hogy befolyásolnák a normál, egészséges sejteket. De ezek a makrofágok csak aktivált állapotban vannak. Lymphocyták aktiválódnak, amelyek erre a célra különleges anyagokat - a limfokineket - szelektálnak.
1981-ben megállapították, hogy a limfokinek és a muramil-dipeptid makrofágok aktiválására való képesség jelentősen megnő, ha ezeket az anyagokat liposzómákká viszik be. Ebben az esetben a hatásuk időtartamának növekedését figyeljük meg, néha akár több napig is. Az is fontos, hogy sokszor csökkentsék dózisukat anélkül, hogy feláldoznák a hatékonyságot. Érdekes megjegyezni, hogy mindkét hatóanyag, ugyanabba a liposzómába zárva, aktiválás közben aktiválta egymást.
A liposzómákban a muramilpeptid nagyon hatásos volt a herpeszvírussal szemben, és egy gyógyszerrel, például glukantinnal kombinálva, és a már említett leishmaniasis ellen.
Így a gyakorlati alkalmazása liposzómák kezelésére néhány betegség egy nagyon ígéretes Avenue farmakológia, alapuló eredmények a tanulmány tulajdonságainak a kolloid anyagokkal, különösen bilipidnyh rétegek.
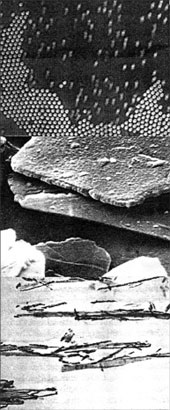
Golyók, botok, lemezek - a kolloid részecskék különböző formái
De a kolloidok az orvostudományban természetesen képesek többet. A kolloid részecskék polimereit tartalmazó gélek reagálnak külső tényezőkre, például a pH, a hőmérséklet vagy az elektromos térerősség változására. A gyomor savas környezetében egy ilyen gél koagulál, és gyengén savas környezetben a bélben, ellenkezőleg, duzzad. A gélek ideális eszköz lehet olyan gyógyszerhez, amely csak a belekben működik.
Kétségtelen, hogy van egy egész palettája az innováció lehetséges gyógyszerek. Például az endoszkópia egy üvegszálas kábelszondát takar, kolloid gélt tartalmaz. Ezután a gél megduzzad, majd újracsökkent, amikor váltakozó feszültséget alkalmaznak. Ennek eredményeképpen a kábel továbbhalad. Most Japán kísérleteket tesz ilyen mesterséges robotok - "földigiliszták" bevezetésére a műtét során a minimális beavatkozás a szervezetbe. A módszer nagy előnye, hogy nem szükséges az endoszkópot erõs erõin keresztül nyomni, ez utat nyit magának.
Amikor a kémikus Wolfgang Ostwald először mikroszkópos kolloidokat látott a 20. század húszas éveiben. rájött a hatalmas potenciálra: "A jelenlegi természettudományok egyik területéről sem tudok, amelyek egyik vagy másik módon nem érintenék olyan sok és sokféle érdekes területet. Természetesen az atomok és a radioaktivitás elmélete mindenkinek érdekes. De ezek az inspirált finomságok hasonlóak a kolloidok kémiájához, amelyek sok területen fontos kenyérként szükségesek. "
Mindazonáltal több mint hetven év telt el a felfedezés előtt, új életet kapott.
Kolloid diszperziók (diszperziók) - microheterogeneous képződését, amelyben egy finomszemcsés anyag - a nemfolytonos fázis - egyenletesen elosztott (diszpergált) a másik fázisban - diszpergáló közeg. A kolloid rendszerekben a diszpergált fázis részecskemérete 10 -9 -10 -7 m, azaz kb. a nanometerektől a mikrométerek frakcióiig terjed. Ez a régió nagyobb, mint egy tipikus kis molekula mérete, de kisebb, mint az objektum mérete egy hagyományos optikai mikroszkópban.
Minden természet - állatok és növények, a hidroszféra és az atmoszféra, a földkéreg és az altalaj - olyan összetett gyűjtemény sok változatos és különböző típusú durva és kolloid diszperziók. A diszpergált állapot teljesen univerzális, és megfelelő körülmények között bármely test beléphet. Ez határozza meg a sajátos helyzetét kolloidkémia - a tudomány foglalkozik a tanulmány a kolloid rendszerek és a felszíni jelenségek, amelyek fejlesztését végzik közvetlen kapcsolatot és kölcsönhatást számos gyakran egymáshoz nem kapcsolódó tudomány, az ipar, az orvostudomány és a mezőgazdaság.
A kolloidok globális szerepe abban rejlik, hogy ezek az élő biológiai szervezetek fő összetevői. Az emberi test összes anyaga kolloid rendszer.
A kolloidok táplálék formájában kerülnek be a szervezetbe, és az emésztési folyamatban a szervezetre jellemző specifikus kolloidokká alakulnak.
Az ember kolloid-kémiai fiziológiája egy tudományág, amely tanulmányozza az emberi testrendszerek működését, amelyek kolloid vegyületeket alkotnak. Elmondható, hogy az egész emberi test egy komplex kolloid rendszer, amely kapcsolatban áll a felszíni jelenségekkel.