Az ionizációs energia
A ionizációs energia - az energia egy kommunikációs, vagy ahogy néha nevezik, az első ionizációs potenciál (I1), a legalacsonyabb szükséges energia egy elektront távolítanak el egy szabad atom a legalacsonyabb energia (őrölt) állapotban végtelenre.
Az ionizációs energia az egyik fő jellemzője az atom. ahonnan nagymértékben függ a jellege és erőssége a kémiai kötések által alkotott atom. Atomi ionizációs energiák is jelentősen függ redukáló tulajdonsága a megfelelő egyszerű anyag.
Vannak még fogalmak a második multi-elektron atomok, harmadik és így tovább. D. Ionizációs potenciál képviselő elektron energia eltávolítását a szabad gerjesztett kation a díjakat az +1, +2, és így tovább. D. Ezek ionizációs potenciál, általában kevésbé fontos, hogy a jellemzők kémiai elem.
Az ionizációs energia mindig endoenergeticheskoe érték (világos, hogy tépje le az elektron az atom, a szükséges energiát, hogy csatolja spontán ez nem történhet meg).
Az atomi ionizációs energia a legnagyobb mértékben befolyásolják a következő tényezők:
- A hatékony nukleáris töltés, egy olyan funkció az elektronok száma az atom árnyékoló mag és elhelyezkedik mélyebben fekvő belső pályák;
- a sugárirányú távolság a mag a külső maximális töltéssűrűség, a legtöbb gyengén kötött, hogy az atom, és hagyja a ionizációs egy elektron;
- intézkedés a átható ereje az elektron;
- elektron-elektron taszítás között a külső (vegyérték) elektron.
A ionizációs energia is befolyásolja kevésbé jelentős tényező, mint például a kvantummechanikai kicserélődési kölcsönhatás. spin és töltés korrelációs et al.
Ionizációs energia elemek mérik eV egyetlen atom vagy joule per mól.
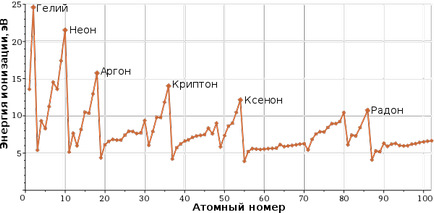
A ionizációs energia az elemek.