Nedvesítő jelenségek - studopediya
Adszorpciós elektrolitok jellegétől függ az adszorbens. Ionok képesek polarizált adszorbeált csak a felülete a poláris molekulák vagy ionok. A nagyobb ion sugara adszorbeátum ugyanabban díj, annál jobban adszorbeálódik. Ez annak köszönhető, hogy a nagyobb polarizálhatóságot és hidratálást nagy ionok. A képesség, hogy adszorbeálja képezhet a következő sorozat:
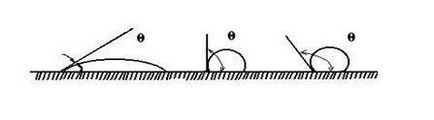
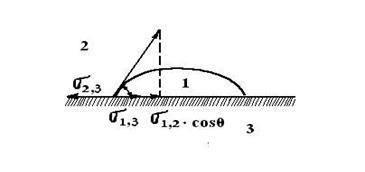
li + mg 2+ cl - K + < Az Exchange adszorpció esetében megfigyelt már adszorbeált ionok a felületen az adszorbens. Akkor nem lehet közötti csere elektromos kettős réteg az adszorbens és a környezet. Ioncserélő így fordul elő ekvivalens mennyiségű. Cseréjére adszorpció megy végbe számos funkcióval. 1. csere adszorpciós specifikus: a csere csak bizonyos ionok. Megkülönböztetése savas és bázikus adszorbensek. Savas oldatok adszorbensekkel kationok kicserélésére, és a fő - anionok. Vannak amfoter adszorbens képes megosztás mindkét típusú ionok. 2. A csere adszorpció nem mindig visszafordítható. 3. A csere adszorpciós lassabb, mint a molekuláris adszorpció. 4. csere adszorpciós megváltoztathatja közeg pH-ja. adszorbens - H + + Na + + Cl - ® adszorbens - Na + + H + + Cl -; adszorbens + OH - + Na + + Cl - ® adszorbens + Cl - + Na + + OH -. A csere adszorpció nagy jelentősége van a biológiában, a mezőgazdaság, a mérnöki. A talaj elnyeli a kálium, ammónium-iont kibocsátások kalcium, magnézium, alig nyel-klorid, nitrát, szulfát ionok. Megvan az a képessége, hogy elnyelje a keveréket finomra őröljük oldhatatlan alumínium-szilikátok. Vízkezelő, ioncserélő gyanta oldatok koncentrációja széles körben használják. Az Exchange szorpciós figyelhető meg a sarokban, bár ő nem rendelkezik polaritás. Megmagyarázni ezt a tényt, Frumkin javasolta a következő terv. Szén adszorbeálja hidrogén molekula, ha érintkezésbe kerül az adszorbens képez hidrogén-ion: ugolH2 ® szén 2- 2H + Ez a komplex képes ioncserélő: Szén - H + + Na + + Cl - ® szén - Na + + H + + Cl -. ugolO2 ® szén 4+ 2O 2-, szén 2+ O 2 + H 2O ® szén 2+ 2OH -, Szén + OH - + Na + + Cl - ® szén + Cl - + Na + + OH -. Nedvesítő intenzitása határozza meg a kölcsönhatás a molekulák között a különböző anyagok, és ebben az értelemben, egy jelenség, közel adszorpciós. Upon nedvesítése a szilárd testfolyadék megfigyelhető terjedő felülete mentén a csepp, amíg a kialakulását egy egyrétegű. Nedvesítése nem mindig teljes, ebben az esetben a csepp és a felület egy úgynevezett érintkezési szög. Ennek értéke lehet nagyobb vagy kisebb, mint 0. 90 ábrán bemutatott. 4.2. Ez hozott mérésére az érintkezési szög a folyadék fázistól. Ábra. 4.2. A nedvesítési szöge folyadékok különböző jellegű A nedvesítő folyadékot lehet tekinteni egy szilárd test, mint egy az intézkedés következtében a felületi feszültség erők. Vegyük a részleges nedvesítő-, ábrán látható 4.3. Kerülete cseppecske kölcsönhatás határ három környezetben: folyadékok 1, 2 és kívül a szilárd test 3. Ábra. 4.3. A függőség a érintkezési szög a felületi feszültség különböző interfészek: 1 - folyadék; 2 - a levegő.; 3 - szilárd Az az egyensúlyi állapotot fejez ki Young egyenlet: Nedvesítő csökkenése kíséri a felületi energia Ha a felület érintkezik a poláris, vízzel és a nem-poláris szénhidrogén szelektív nedvesítő figyelhető meg. Ebben az esetben az érintkezési szög kisebb, mint 0. 90, és ez a felület az úgynevezett hidrofil. Ha a testet jobban nedvesíti a nem-poláros oldószerben, a víz érintkezési szög nagyobb, mint 90, és 0. nevezett hidrofil felületi. A szelektív víz nedvesítő figyelhető meg, ha a polaritás a különbség a víz és a szilárd anyag kisebb, mint a nem-poláris szénhidrogén és szilárd. Anyagok hidrofil felületi például szilícium-, alumínium-, gipsz, fém-oxidok és -hidroxidok, cellulóz. Nempoláris szénhidrogént szelektív nedvesítő figyelhető meg, ha a polaritás közötti különbség a szénhidrogén és a szilárd anyagot kisebb, mint az anyag és a víz. A hidrofób anyagok közé tartoznak a szénhidrogének, szulfidok nehézfémek, talkum, grafit, kén. Az érintkezési szög mérési eredmények, bár van számos nehézséggel. Nagysága a szög befolyásolja nyomait felületi szennyeződésektől, a jelenléte a oxidfilm, adszorbeált levegő, felületi érdesség, felületi állapota kialakulásának. Nedvesítő fontos szerepet játszik a gyártási folyamatokban, például flotációs. A módszer azon alapul, a használata különbségek nedvesíthetőség különválasztott részecskéket vízzel. Nézzük meg a viselkedését a kis hidrofób és hidrofil részecskék a felületen a víz-levegő, víz-olaj. Hidrofil részecskék mind határokat állít a vízbe és elsüllyedt. Hidrofób részecske marad a felület azzal a megkötéssel, hogy nem nagyon nehéz. Kénvegyületek több hidrofób, mint a meddőkőzet (szilícium-dioxid). A nagyobb hatékonyság a bevezetett levegő a szuszpenziót (habos flotációs). Amikor lebegő buborékok által összegyűjtött részecskék a felületén, amelyen a víz képez nagy érintkezési szöget. Mivel a cellulóz a felületen mineralizált hab, amelyet eltávolítunk a koncentrátum. Az optimális méret a ásványi szemcsék a flotációs a 0,15-0,01 mm-es. Ahhoz, hogy a hatékonyság növelése a flotációs gyűjtők használják. Ez amfifil szerves vegyületek, amelyek felületén adszorbeálódik az ásványi úgy, hogy a poláros rész felé néző az adszorbenshez, és a radikális kifelé. A hidrofobicitás a részecskék a növekedést. Gyakran használhatók e célokra xantátok - ROCS2 M, ahol M - alkálifém. Közel a jelenségek tapadási nedvesítő és az adszorpció. Ez a jelenség akkor fordul elő, ha két kölcsönösen oldhatatlan, folyadék vagy egy folyadék és egy szilárd vagy két szilárd anyagot érintkezésbe hozzuk, és egymáshoz tapadnak, az intézkedés alapján az intermolekuláris erők. Az adhéziós munka a két folyadék határozza meg Dupre egyenlet. folyadék rendszer - szilárd Továbbá még megkülönböztetni tapadás kohézióját: ragadt a két réteg ugyanazon anyag.
Kapcsolódó cikkek