Alapvető színpadi heterogén eljárások
Kinetikája heterogén eljárások.
4.4.1 típusai heterogén eljárások
Heterogén reakciók, ellentétben a homogén, akkor jelentkeznek, amikor a reagensek több mint egy fázisból állnak. Elválasztó felület az egyik fázis a másik, az úgynevezett a felület felszínén, vagy interfész. Keresztül a reagensek felszíne kell szállítani. Fázis felület, vagy interfész a fázisok közötti határ. Például, a reakciók „szilárd-gáz” felület a külső felülete a szilárd anyag, amely érintkezik a gáz. Az interfész két nem elegyedő folyadék felületi érintkezés a két folyadékot.
Heterogén folyamatok jellemzően uchsatii következő lépéseket:
1. Közlekedési reagenseket a felületen.
2. szorpciós reagensek a határfelületen.
3. A kémiai reakció a határfelületen fazyu
4. A deszorpciós reakció termékek AKF interfész.
5. Közlekedési a reakció termékek a mélység a folytonos fázis
A teljes sebességgel a folyamat egymásra egyes fordulatszám-fokozatok.
Szállítás a reagensek a határfelületi anyagátadási alkalmazásával ismertetjük mintákat.
Az alapvető egyenletet leírására az anyagátadási sebesség a következő:
- tömegáram, hogy az interfész felületen, kmol / min
- anyagátadási együttható, m / min
- érintkező felülete, m 2
- reaktáns koncentrációja a felületen, kmol / m 3
- reaktáns koncentrációja az ömlesztett folytonos fázisban. kmol / m 3
2. a felületen szorpciós sebességű interfész Henry-törvény bude koncentrációjával arányos a határfelületen a fázisok, az arányossági tényező - Henry-állandó függ az anyag természetétől és a hőmérséklet. Ez a folyamat általában elegendően gyors, és a felületi koncentráció felírható a következőképpen:
A reakció sebessége a felületen egyenlő lesz a termék a reakció sebességi állandója a reaktáns koncentrációja a határfelületen.
Hiányában a reagens tárolási határfelületi anyagáram szállítják a felület miatt anyagátadási egyenlő a forrasztószer, amely belép a kémiai reakció. Egyenlővé ezek a folyamatok, megkapjuk az anyagmérleg egyenlet.
Egyenlet segítségével koncentrációja a határfelületen. Kapunk egy kifejezés:
Behelyettesítve ezt a kifejezést az egyenlet a sebessége a heterogén reakcióelegyet a felület (4.4.3), kapjuk egyenletet a sebessége a heterogén reakcióelegyet, kifejezett térfogat Reagens koncentráció a folytonos fázisban:
Egyenlet (4.4.7) fejezi additivitás ellenállásokat egyes fokozatokban heterogén eljárás. Ha a kémiai ellenállás sokkal nagyobb, mint az ellenállás anyagátadási és anyagátadási sebességet, hogy a felület korlátozza a teljes sebességgel a folyamatot. Ebben az esetben azt mondjuk, hogy a folyamat játszódik le a diffúziós régióban. Feltéve, hogy mikor. anyagátadási sebesség sokkal nagyobb, mint a reakció sebessége a határfelületen, és a folyamat játszódik le a kinetikus régióban. Ha az egyes szakaszait a sebességi állandó összemérhető. folyamat
bevételt a vegyes diffúziós-kinetikus régióban.
4.4.3.Opredelenie áramlási mező
FIELD heterogén eljárással lehet meghatározni függően hatékony aránya a folyamatot a folyamat feltételei.
· A folyamat a megfigyelt arány a relatív mozgási sebességét fázisok.
Ha a megfigyelt sebessége a folyamat függ a sebességet a mozgás fázisok, a teljes sebesség a folyamat vezérli az anyagátadási sebesség. Ez azt jelenti, hogy a folyamat játszódik le a diffúziós régióban, mint az anyagátadási sebesség nő, mint az áramlási sebesség a szilárd fázis, azáltal, hogy csökkenti a vastagsága a diffúziós határréteg összhangban egyenletek, származó 1-gozakona Fick. A korlátozó eljárási lépést a folyamat áramlását a diffúziós zóna egy diffúziós sebessége révén az álló diffúziós réteg a felületen:
Ahol - a diffúziós határréteg vastagsága, ami függ az áramlási sebesség.
Például, ábrán. A hatása a keverés sebességét a oldódási sebessége cink savas
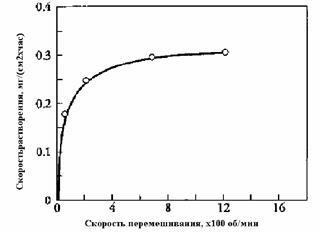
Ris.4.4.1. A függőség a cink oldódási sebesség a forgási sebességű keverővel.
Az ábra azt mutatja, hogy növeljük a keverő forgási sebességét „800 ford / perc, további növekedését a kioldódási sebesség gyakorlatilag leáll. Ez lehet az átalakulási folyamat a kinetikus régióban, ahol a sebesség a folyamat független a szállítási sebességnél a reaktáns, hogy a felület, amelyen van egy kémiai konverziós.
Egy másik módja, hogy meghatározzuk az áramlási heterogén folyamat egy általános tanulmányt a függőség mértéke a hőmérséklettől.
Ismeretes, hogy az aktiválási energia a kémiai folyamatok általában a tartomány 40¸200 kJ / mól. Miközben az aktiválási energia a diffúziós folyamatok zajlanak a folyékony vagy gáz halmazállapotú közeg a tartományban 4¸20 kJ / mol
Ris.4.4.2: A hőmérséklet hatása a reakció C + ½O2 → CO. A hőmérséklet-intervallumban 600-800 ° C, E = 174 kJ / mól (kémiai kontroll), és a tartományban 1100-1300 ° C, E = 6,3 kJ / mól (diffúzió kontroll)
On ris.4.4.2 mutatja a hőmérséklet hatását az oxidációs reakció a szén oxigénnel hiányban. Az ábra azt mutatja, hogy a hőmérséklet intervallum 600-800 ° C, a felületi oxidáció reakció lassú szakaszban bóluszt, mint a haladási sebesség az oxigén a reakcióelegyhez felületre. Amikor a hőmérséklet elérte az 1000 ° C-on a felületi reakció sebességét úgy megnő, hogy az arány a közlekedési oxigén a felszínre a reakció válik lassabb sebességgel lehetséges a fogyasztás, és a heterogén oxidációs folyamat továbblép a diffúziós szabályozás.
Effect képezzenek határfelületi felületi sebessége heterogén eljárások.
Szilárd formában is reagáltatni kell a folyékony vagy gáz halmazállapotú fázisban fontos szerepet játszik annak meghatározásában, az arány a folyamat. Ha a szilárd anyag alakú lemez vagy tárcsa, a felület területe állandó marad a reakció során, és ezért az eljárás sebessége is állandó. Azonban, ha a szilárd anyag formájában egy gömb vagy tabletta, a felület folyamatosan fog változni a reakció során, és így a sebesség is eltérőek lesznek. Ha ez a változás az, hogy figyelembe, akkor lehet megjósolni a változás a folyamat sebességét, ahogyan folyik
Tekintsük reakció „szilárd-folyadék”, így például a fém oldódását reakciót a sav.
A kioldódási sebességet a szilárd fém részecskék a sav lehet által leírt egyenlettel:
ahol W-tömeg fém egy tetszőleges időben, kg
A - felülete a fémrészecskék, M 2.
savkoncentráció a felületen
Tegyük fel, hogy a fém részecskék gömb sugara r. majd
- részecske sugara a kezdeti időben, m
- tömege részecskék a kezdeti időben, kg
- tömege egy részecske egy tetszőleges időben, kg
- részecskesűrűség, kg / m 3.
- részecskék tömegét a kezdeti időben, kg
- részecske sugara a kezdeti időben, m.
- A részecskék száma a kezdeti időben.
Feltételezve, hogy a részecskék száma a folyamat nem változik, de a változások csak a részecske tömege, állíthatjuk elő az alábbi kifejezés az aktuális tömege a részecskék:
- ahol W - tényleges tömege részecskék egy időben, kg
-részecske méretét egy tetszőleges időben, m
-a részecskék felületén egy tetszőleges időben, M 2.
-teljes felülete az összes részecske a jelenlegi a részecskék tömegének W, m 2.
Jelöljük részecskék-felszíni felület egységnyi térfogata a reaktor, megkapjuk a következő egyenletet, amely kifejezi a jelenlegi értéke függvényében fémtömegének:
- A fajlagos felület a részecskék, m 2 / m 3.
Behelyettesítve ezt az értéket a fajlagos felület az egyenletben a sebessége az egyes eljárási lépések rögzítve mind a homogén reakció, megkapjuk az egyenlet a reakció sebességét előforduló felületén a szilárd fázis tartalmaz egy egységnyi térfogatú a reakció:
Amennyiben - az arány a heterogén és homogén reakciók. volt.
Most kifejezni aktuális értékét a súlya a szilárd reagens keresztül moláris koncentrációja és térfogata a reaktor:
Ms - a molekulatömege a szilárd fázisú, kg | kmol
- moláris koncentrációja a szilárd anyagok a reaktor térfogatát, kmol / m 3.
Differenciálás egyenlet mindkét oldalát (12) idővel, figyelembe véve (11) egyenlet megkapjuk a kifejezés a változási sebességének tömege a szilárd reagens:
Ahol van dimenziója kg / m 3.
Az egyenlet (4.4.12), tudjuk írni az egyenleteket a matematikai modell, a többi komponens a következő módon:
Így kapunk egy matematikai modell egy heterogén eljárással a kvázi-homogén modell, akkor szoftvercsomag ReactOp, hozzon létre egy egyéni modellt az alábbiak szerint:
- Írja egyenleteit kémiai reakciók minden szakaszában.
- Írja egyenletet a jelenlegi tömeg értékét a szilárd fázis (ha ez megváltozott.
- Írja be a kifejezést az adott fázis érintkezési felületen.
- Szorzás rámpa komponens-koncentrációk kapott ReactOp program az érték a konkrét fázis érintkezési felületen.
Ez az eljárás némi időt vesz igénybe, és nagyon könnyen használható algoritmikus nyelvet Fortran, közel a nyelvet a normál felvételi matematikai képletek.
5. § A szintézis modell a technikai objektumok alapján hidrodinamikai modellek és egyenletek kémiai kinetika.
Oldal keletkezett: 0.009 mp.