Felnőtt típusú légzési distressz szindróma vagy felnőtt típusú légzési rendellenességek szindróma
Vészhelyzet - az angol szorongástól - komoly rossz közérzet (rendellenesség, kóros állapot).
A kifejezés a felnőttkori légzési distressz szindróma típusú (ARDS) egyesíti több heterogén etiológiájában és patogenezisében jellemzett állapotok klinikai refrakter hipoxémiához nem foglalkoztak giperoksiches Coy minta. Előnyösnek tartjuk a kifejezés szindróma a légzőszervi rendellenességek, például felnőtt (SDRvt), mint a fókuszpont a patogenezisében ez a szindróma a felületaktív anyag hiányával.
A gurulóút gyakorisága nem rögzített. Adataink szerint az SDRw körülbelül minden harmadik - negyedik gyermeket fejti ki, akik vegyes eredetű súlyos asphyxia születtek.
Etiológia. A külföldi szakirodalom van 20 ARDS szinonimák (shock tüdő-szindróma, fehér fény, fény-szindróma tömör, nem-kardiogén tüdőödéma, mikroembólia szindróma, felnőtt hialin membrán betegség, stb). Hangsúlyozzuk, hogy az etiológiai tényezők lehetnek tényezők okozzák szisztémás gyulladásos válasz (a részleteket lásd a XIV ..), és kíséri a kibocsátás túlzott gyulladásos citokinek, - szepszis, dekompenzált DIC, shock bármilyen etiológiájú, tüdőgyulladás, barotraumát és / vagy volyumotravma tüdő , hiperoxia, aspirációs gyomortartalom, belélegezve mérgező anyagok, a levegő embólia, zsírok, sugárzás pneumonitis, égés, diabetikus ketoacidózis, szisztémás vasculitis.
Patogenezisében. Az alveoláris-kapilláris membrán károsodása miatt a pulmonalis kapillárisok és tüdőödéma fokozott permeabilitása miatt nagyszámú leukociták felhalmozódtak a parenchyma során. A páciens vérplazma proteinek pro-inflammatorikus hypercytokinémiával, behatoltak az alveolákba, inaktiválják a felületaktív anyagot.
Fehérvérsejtek (neutrofilek) központi szerepet játszanak a mechanizmus fejlesztésének ARDS, de a patogén mechanizmusokkal való felhalmozódás a tüdőben, és kár, hogy a parenchyma nem teljesen világos. Azt jelzik, hogy a neutrofilek és monociták a forrása felesleges peroxidgyökök, arachidonsav metabolitok proteoliticheskihlizosomalnyh enzimek károsodás al veolyarno-kapilláris membrán, gyulladásba-tant felületaktív inaktiválódik és gátolják annak szintézisét.
Az SDRin patogenezisének különálló kapcsolata lehet:
a szervezet szisztémás gyulladásos reakciója proinflammatorikus citokinek feleslegével (citokin vihar);
hosszabb hipoxia tüdő ischaemia;
irracionális szellőztetési módok (II. típusú volumetrauma és barotrauma károsodás pneumociták és gátolják a felületaktív anyag szintézisét);
a pulmonalis microvessel endotélsejtjeinek aktivitása növeli a ragasztó képességüket és növeli a tüdők kapillárisok permeabilitását a citokin vihar hatása alatt;
mikrokeringési rendellenességek zavarai miatt a vér reológiai (iszap-szindróma) mikrotrombozov közepette túltermelés Trom boksana-Ar, vérlemezke aktiváló faktor, a leukotriének, a vérlemezke eredetű növekedési faktor és a prosztaciklin-hiány;
Tapadás az aktivált neutrofilek az aktivált pulmonális endote liotsitam-szerű idejének kezdete akut gyulladás tüdőödémás fejlődés, csökken a tüdő funkcionális reziduális kapacitás és a statikus szakító tüdőszövet;
a felületaktív anyag szintézisének és megsemmisítésének gátlása;
a lipid peroxidáció mérgező termékeinek felhalmozódása;
balról jobbra tolódás, a tartós magzati keringés szindróma a megnövekedett nyomás miatt egy kis körben;
súlyos metabolikus acidózis, amely károsítja a tüdőt;
a toxikus metabolikus termékek felhalmozódása a hipoxia során;
fényáteresztett folyadék túlterhelése (nedves tüdő);
idegen részecskék lerakódása az öntött folyadékból a tüdőbe;
intersticiális fibrózis és szklerózis;
Lehetséges időtartama az akut váladékos fázis - 1-3 napig, de abban az időben már kidolgozott tüdőkárosodás kollagén rostok a kötőszövet, microembolisms (neutrofilek, fibrin, vérlemezke). Ezután követi a proliferatív fázist, amelyet intersticiális sejtinfiltrátumok jellemeznek, a sérült és nem képes felületaktív II típusú pneumociták proliferációja; időtartama 3 - 1 0 nap. Végül pedig az intersticiális fibrózis fázisa következik be. A halál a pulmonalis szívelégtelenségből származik.
Ellentétben BGF (SDR I. típusú) tartja a másodlagos felületaktív hiánnyal elsősorban a pusztulástól, és károsodott ejekciós, bár a számát típusú pneumociták ilyen betegek javult. SDRvt lehet szakítani bármely szakaszában, de súlyosabb tüdő folyamatban jön megsértése építészeti acinus, alveoláris fibrózis, krónikus bronchopulmonáris betegségben típusú bronchopulmonáris diszplázia.
Az SDRvt gyermekek számára, akiknek nagyon alacsony a testtömegük, a VUI, valamint azok a gyermekek, akikben a szülési súlyos fulladás kifejlődött a krónikus intrauterin hypoxia hátterében.
V.A.Negovsky SDRvt tárgya kijelzők postresuscitative betegség, és így a patogenezisében sajátos szerepét és iatrogennye tényezők, beleértve hiperoxia, használja elég melegítjük, vagy a nedvesített oxigén, volumen túlterhelés során infúziós terápia, rossz infekciókontroll, poliprogmaziya, hosszú irracionális parenterális táplálkozás.
Klinikai kép. Az első klinikai jele SDRvt perzisztens hipoxémia alacsony válasz légzési oxigén-levegő keveréket, a beépítést a gyermek magas koncentrációjú belélegzett oxigént (FiO2 hosszú> 0,3-0,4) hiányában minden olyan ellenőrzött patológiák a kardiovaszkuláris rendszer . A nehézlégzés figyelhető segéd izmok légzés, nyugtalanság, szorongás, remegés, görcsök vagy rohamok készségét, tachycardia némi szívhangok tompa és elhatárolható szisztolés zörej, a tendencia, hogy az ödéma, oliguria, emelkedett vérnyomás. Eleinte, annak ellenére, hogy az expresszált tűzálló hipoxémia, hypercapnia hiányzik. Van metabolikus acidózis.
További légzési elégtelenség progresszíven növekvő (dolgozzon fakó bőrszín, márvány mintás, közös cianózis, nyögés, kryahtyaschee levegőt kifejezett kiegészítő izmok részt vevő légzés), a tüdő merevebbé válik, és amikor a ventilátor szükséges módosító üzemmódba, hogy megszüntesse hipoxémiához (növeli a belégzési nyomás , a relatív hosszát a kilégzés, légzési térfogat, stb) hallható különböző diffúz zihálás, beleértve krepitiruyuschie, nezvuchnye finoman, srednepuzyrchaty azaz a magas és az alacsony száraz és kilégzés, amely létrehoz egy képet hörgőelzáródás, ödéma és a torlódások a tüdőben. Jelei izgatottság szindróma egy gyermek kombinált időszakok levertség, veszteség izomtónus, alacsony vérnyomás. A következő termesztési feltételek letargia, amíg a fejlesztés kóma jelennek szívelégtelenség és Ishe-dasági változások szív EKG vizsgálat, állandó tüdőbeli magas vérnyomás, hypovolaemia, csökkentett artériás vérnyomás, vérzéses szindróma (dermális vérzés, gyomor-bélrendszeri és tüdővérzés), többszervi elégtelenség oliguria vagy anuria esetén.
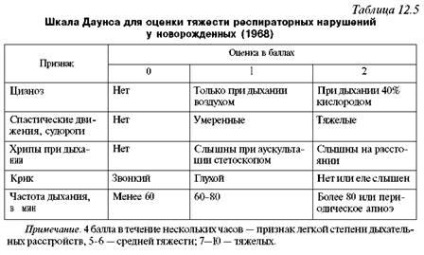
A gyermekek korai szakaszában jelentkező légzési rendellenességek súlyosságát a Downs skála segítségével határozhatjuk meg (12.5. Táblázat).
A radiográfiával detektáltuk korai jelei intersticiális és alveoláris tüdő ödéma (mellék vaszkuláris minta ödéma és interlobar mellhártya gócok árnyékok - bolyhos fény, szegmentális és részvény ödéma légzsák bronchograms). Azonban, miután néhány órán vagy napon a mellkasröntgenen megjelenő diffúz változások hasonló változásokat az SDR I. típusú (HMD). Néhány túlélő gyermekek továbbra is fejleszteni megugrott a minta a tüdő gyökér, durva egyenetlen csökkenése az átláthatóságot a tüdő mezők egyidejű jelenléte levegő broncho grammos tyazhistye árnyékok, jelezve tüdőfibrózis.
A szabály a bakteriális fertőzés rétegződése a folyamat egyik szakaszában és a tüdőgyulladás kialakulása.
A kezelés. Mivel a szerepe iatrogennyh tényező a fejlesztés SDRvt (ARDS) elengedhetetlen, hogy segítse a gyermekek születési asphyxia, gondosan megfelelnek a meghatározott VII különösen kapcsolatos hatékony folyadék menedzsment, monitoring, vérgáz, hemodinamika, szellőztető beállítások és belföldi járatokat. Nagyon fontos, hogy a VVL és az IVL oxigén-levegő elegyét ésszerűen felmelegítsük, túl korai indítani
enterális táplálkozás, fertőzés kontroll. Az SDRvt - terápia fejlesztésével a leghatékonyabb korai (!!) felhasználás az exogén felületaktív készítmények terápiás intézkedéseinek komplexumában. Bemutatja a megvalósíthatóságát korai dexametazon arányt (abban a exudatív fázisban a betegség), vagy inhalációs szteroid (flutikazon-propionát - fliksotid, budeso-nid - pulmikord) és trentala, szuperoxid dizmutáz.
Előrejelzés. Az SDRw (ARDS) és a visszanyerés fordított fejlődése minden szakaszban lehetséges. Ha azonban a IV. Stádium (súlyos élettani anomáliák - intersticiális fibrózis) kifejlődött, akkor a halálozási arány elérte az 50% -ot.