A testsejtek legfontosabb kapcsolói fehérjék
A verseny szponzora a távlátású Life Technologies.
A Wnt útvonal az egyik legfontosabb molekuláris jelátviteli útvonal, amely szabályozza a sejtek embrionális fejlődését és differenciálódását. Az egész utat az egyik ligandumból neveztük el, amely aktiválja a sejtek útját - Wnt. Ez a csökkenés a két gén nevének fúziójából adódott - W g + Int. A prototípus gént Drosophilla-ban fedezték fel, ahol a Wg génben mutatkozó mutáció (kevesebbet) elfojtotta a szárnyak fejlődését. A gerincesek homológ génje - az Int - összefügg a rákos daganatok kialakulásával.
Napjainkig ismeretes, hogy a Wnt útvonal szabályozza a szervek fejlődését az embriogenezis során, és felelős a szervezet kétoldalú szimmetriájáért. Funkciói mindegyike az embrionális sejtek által létrehozott organizmus tömegét jelenti. Felnőtteknél a Wnt útvonal betegségei a rák kockázatának növekedéséhez vezetnek. A közelmúltban végzett vizsgálatok is kimutatták a Wnt komponensek fontos szerepét az őssejtek proliferációjában és differenciálódásában.
A glikoproteinek Wnt - egy család szekretált sejt jelátviteli molekulák, amelyek részt vesznek a koordinációs viselkedésének sejtek a szervezetben. Ezek a fehérjék felfedezte a korai 1980-as években, mint a marker a sokféle rák, kiderült, hogy kulcsfontosságú szabályozói az embrionális fejlődés, a regenerációs folyamatokat a csont növekedési, őssejt differenciálódás, és sok egyéb folyamatok társított morfogenezis és a sejt sorsát meghatározása.
Wnt fehérjék szerkezete
A Wnt-család fehérjéinek szerkezete hasonlít egy kézre (1. ábra; [1]). A hüvelykujj szerepét az aminoterminális tartomány játssza, amely öt diszulfidhidak által stabilizált α-hélixekből áll. A "mutatóujj" egy olyan karboxi-terminális domén, amely két β-szálat tartalmaz, amelyeket hat diszulfid hidat tartalmaz. A "Palm" nagy rugalmassággal rendelkezik, amely biztosítja a fehérje konformációs mobilitását. Ezen túlmenően a palmitol-zsírsav, amely a transzportfehérjékkel való kölcsönhatás szempontjából szükséges, kovalensen kapcsolódik a "nagy ujjhoz". A zsírsav-maradék hozzáadását acilezésnek nevezzük. és ez a "pálma" - glikoziláció egy másik módosításától függ. Ennek hiányában a közlekedési fehérjékkel való kölcsönhatás és ennek következtében a szekréció lehetetlenné válik.
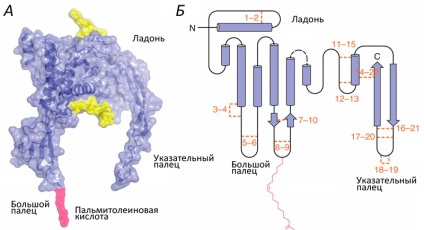
1. ábra: A Wnt.A. Volumetrikus modell Wnt8. A sárga a glikozilezett területeket jelzi. B. A Wnt. Másodlagos szerkezete Az narancssárga szín jelzi és számozott 22 cisztein-maradékot, amelyek páros diszulfid-hidakat képeznek. A rózsaszín egy kovalensen kapcsolódó acilcsoport: zsírsav. Kép: [2, 3].
A Wnt
Feltételezzük, hogy a kívül szükséges a váladék a Wnt-zsírsavmaradék hordoz atsiltranferraza endoplazmatikus retikulum Porkupin (PORCN), mivel deléciója e gén ad szekrécióját Wnt (3. ábra ;. [4]). Az acilezés befejeződése után Wnt fehérjéket felismerik a Golgi-készülék - transzmembrán receptor GPR177 (közismert nevén Wntless (Wls)), «fehérjék rakodók» p24, amelyek hordozzák Wnt az endoplazmás retikulumból a sejt felületére (3. ábra; [5].), És a transzport fehérjék Swim amely fenntartja oldhatósága és jelátviteli aktivitás komplleksa Wnt / Wls [6].
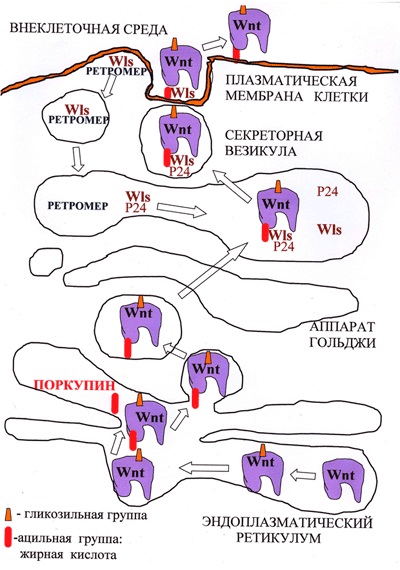
2. ábra A Wnt. Biogenezise és szekréciója A Wnt molekulák az endoplazmatikus retikulumban érlelésen mennek át, majd glikozilációnak, majd acilezésnek vetik alá. Ezután a Golgi-készülék Wntless-fehérjével együtt belépnek a szekréciós vezikulákba, amelyek belsejében a plazmamembrán kereszteződik, és ezután kiválasztódnak. A Wntless-t kivontuk az elhasznált szekréciós vezikulákból, és a Retromer-komplexbe visszük vissza a Golgi-berendezésbe.
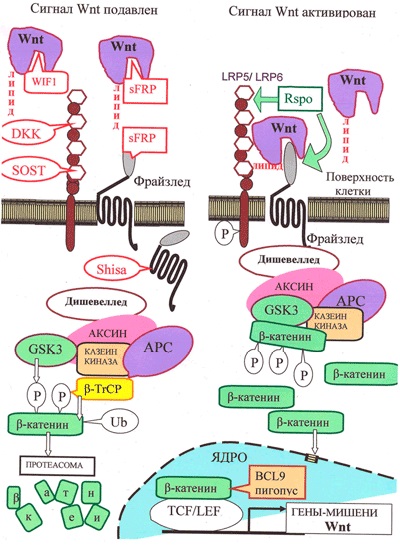
3. ábra: Wnt-jelátvitel kanonikus útja. A kanonikus út "munkaterülete" β-catenin: az inaktív állapotban kicsi, és aktív állapotban sok, aktiválja a nucleus transzkripcióját.
Inaktív állapotban: hiányában közötti kölcsönhatás és a Wnt receptor LRP5 / 6 számú citoplazmatikus β-catenin malo miatt a „komplex lebomlási”, álló APC fehérje, a kazein és a glikogén szintézis kináz GSK3, található a „platform” axin fehérje. Ezzel a komplex citoplazmatikus β-catenin foszforilálódik, majd ki vannak téve ubiquitylation fehérje β-TrCP, ami által annak lebontását a proteaszóma.
Aktivált állapot: A Wnt jel a Wnt komplex kialakulásával kezdődik az LRP5 / 6-mal és a Friedled receptorral, ami a Disheveled protein aktiválódásához vezet. Ez gátolja a β-catenin "degradációs komplexét", és kikapcsolja a "β-catenin" ubiquitilitását. Ennek eredményeképpen a citoplazmában felhalmozódó szabad p-katenin [16] behatol a sejtmagba és aktiválja a TCF / LEF transzkripciós faktorok és más mások által végzett transzkripciót.
A Wnt-útvonal szabályozása: a Wnt molekulákkal, antagonistákkal: Wnt-gátló faktor (WIF) és Freysled-felismerő protein 1 (sFRP) közvetlenül kötődnek. Ezenkívül a DKK és a szklerosztin az LRP5 / LRP6 fehérjékkel érintkeztethető a Freisled-Wnt-LRP komplex kialakulásának megakadályozása érdekében. Proteinek Shisa, miután elfogták a Frayszled receptort, megakadályozzák, hogy elérje a sejt felszínét. Ha a Wnt egy LRP5 / 6 és Freysled összetett komplexet alkot, akkor a riasztás aktiválódik. A Freysled és az LRP5 / 6 receptorok stabilizálásához szükséges R-spondin 2 (RSPO) fehérje növeli a jelátvitelt a Wnt útvonal mentén. Az endoplazmatikus retikulumban az LRP5 / 6 érettsége kísérő MESD fehérjét igényel.
A membrán receptorok Wnt
Annak érdekében, hogy a célsejten cselekedjen, a Wnt-nek kapcsolatba kell lépnie a sejt receptorokkal. Mivel ezek a receptorok a sejt felszínén transzmembrán fehérje nyúljanak Frayzled Frizzled (Fz) * és az alacsony sűrűségű lipoproteinek LRP5 / LRP6. Ha kapcsolatba lépnek velük, a Wnt molekulát aktívan befolyásolja különböző antagonisták, amelyeket az agonisták ellenzik (3. ábra). Ezen receptorokon kívül a Wnt kötődik a Ror és Ryk * receptor tirozin kinázokhoz. Ror a Wnt5a-t érintkeztetve foszforilálja a Dicheveled fehérjét, és így szabályozza a szövet morfogenezisét, míg a Ryk a Vangl2 membránfehérjék foszforilezésével szabályozza a sejt polaritását.
A Wnt mechanizmusai hatással vannak a sejtre
Hagyományosan a Wnt-nak a sejtre gyakorolt hatásának mechanizmusai a következőkre oszthatók:
- kanonikus (β-katenin-függő) útvonalat, amely végső soron szabályozza a sejtek sorsának és morfogenezisének meghatározásával kapcsolatos génexpressziós programokat [9]. és
- nem kanonikus (β-katenin független) útvonalak [10]. amelyek szabályozzák a sejt polaritását, stimulálva a citoszkeleton [11, 12] és a kalcium anyagcserét [13].
A kanonikus Wnt jelátviteli út központi eleme a citoplazmatikus β-catenin fehérje stabilizációja (3. ábra). Jel hiányában a β-katenin nem aktív és gyorsan lebomlik. Amikor a sejteket Wnt aktiválja, a p-katenin lebomlási sebessége csökken. A degradáció elkerülése érdekében a β-katenin felhalmozódik a citoplazmába, és belép a magba.
A mag β-catenin nukleáris proteinek befogására BCL9 és pigopus (Pygopus), kölcsönhatásba lép a fehérje TCF / LEF. alakítja át őket erős aktivátorok átírás. TCF / LEF fehérjék mnogofuktsionalnoy, hogy miután a képességét, hogy szelektíven kötődnek a specifikus DNS-szekvenciák és fehérjék specifikus aktivátorok „dönteni”, amely a gén aktiválódik Wnt jel [14]. Azt találtuk, hogy a kapcsolat a β-catenin és a TCF 4 szükségesek az ilyen aktiválás lehet osztani rezveratrol. Ez arra utal, hogy a rezveratrol, amely egy flavonoid nyersbőr a fekete szőlők és a bor az azokból nyert lehet használni, mint gyógyszerek ártalmatlanok, hogy gátolják Wnt jel a rák [15].
A Wnt jelátvitel hatása a sejtciklusra és a sejtproliferációra
Több bizonyíték van a kanonikus Wnt-jelátviteli útvonal és a sejtciklus összetett összekapcsolására. A Wnt jelkaszkád komponensei közvetlenül a mitotikus orsó kialakulásában járnak el. Így például, a kedvenc modell organizmusban molekuláris biológusok - féreg C. elegans - Wnt jelátvitel okoz aszimmetria a mitotikus orsó, amely így egy aszimmetrikus eloszlása β-catenin [17]. Sőt, Wnt jelátvitel erősen aktivált a mitózis során, ami arra utal, hogy a „mitotikus Wnt-jelátvitel” fontos szerepet játszik szervezésében a program a sejtosztódás, és így elősegíti a sejtek szaporodását [18].
Az őssejteket elsősorban két tulajdonság jellemzi: az önmegújítás és a különböző típusú sejtek differenciálódásának képessége *. Ezeket a folyamatokat különböző növekedési faktorok szabályozzák, beleértve a Wnt fehérjéket [19]. Az összegyűjtött adatok azt mutatják, hogy a Wnt / P-katenin jelátviteli út kulcsszerepet játszik a pluripotencia fenntartásában, valamint a szomatikus sejtek reprogramozásában. Ugyanakkor a Wnt / β-catenin jelzése fontos szerepet játszik a differenciálódás folyamatában.
Azt találtuk, hogy hozzáadásával Wnt fehérje, vagy éppen ellenkezőleg, gátolja a Wnt (IWP2 kis molekula) csökkenti sejtpopuláció heterogenitása. Ebben a formában, vagy sejtek egy stabilan magas szintű szintézisét Wnt, vagy sejtek alacsony szintű Wnt-szintézis. A differenciálódás során, embrionális sejtek magas szintű Wnt szintézis előnyösen alkotnak endodermális és kardiális sejtek, és az alacsony - elsősorban neuroektodermális sejtekben [23]. Annak ismeretében, hogy a jelzés Wnt a korai szakaszában a differenciálás növekszik, és a későbbiekben az ellentétes gátolja a fejlődését a szív, engedve a helyes stratégia az alkalmazott kis molekulák és jelátviteli Wnt elő in vitro indukált pluripotens őssejtek szívizomsejtek elérhetetlen mostanáig hatékonyság - akár 98% [24]!
kilátások
30 éve, mivel minden évben hatalmas számú cikk van, amelyek valahogy befolyásolják a Wnt jelzés témáját. Az ehhez a témához hasonló figyelem nagyon megérdemelt, mert az "mindenütt jelenlévő" Wnt molekula rendszeresen meglepetéseket jelent. Például, azt találták, hogy β-catenin, megszökött degradáció aktiválása miatt Wnt-jel aktiválja a szintézisét enzimes alegységének telomeráz (tercbutoxi) őssejtekben és a rák. Ebben volt munkáját egy transzkripciós faktor plyuripotentsii - Klf4, irányítva a terc gén promóter [25]. Ismeretes, hogy a telomeráz - egy enzim fenntartásában telomerhosszúság ellensúlyozni a rövidülés, ami öregedés a sejtek [26]. Ezért a Wnt szerepének feltárása a telomerek stabilizálásában mind a rák elleni küzdelemben, mind az öregedés elleni küzdelemben segíthet.