Propán móltömeg (c3h8), képlet és példák
A propán a szerves természet komplex anyaga. Az alkán osztály homológ tartományának (telített / telített szénhidrogének) képviselője.
A molekula szerkezetét az 1. ábrán mutatjuk be. 1. Normál körülmények között a propán olyan színtelen és szagú gáz, amely kevés vízben oldódik. Robbanásveszélyes keverékek levegővel.
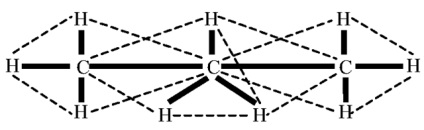
Ábra. 1. A propánmolekula szerkezete.
A bruttó propánképlet C3H8. Mint ismeretes, a molekulatömege a molekula az összege a relatív atomi tömegek a atom alkotja a molekula (relatív atomtömeg értékeket vett Mendeleev Periódusos Táblázat egész számra kerekítve).
Mr (C3H8) = 3 × 12 + 8 × 1 = 36 + 8 = 44.
A moláris tömeg (M) 1 mól tömegű anyag. Könnyen azt mutatják, hogy a számértékek a moláris tömege, és a relatív molekulatömeg úr egyenlő, de az első érték az alábbi méretekkel rendelkezik [M] = g / mol, és egy második dimenzió:
Ez azt jelenti, hogy a propán móltömeg 44 g / mol.
Példák a problémamegoldásra
Tegyük fel a kén oxigénhez való csatlakozásának képletét, ha az elemek tömegfrakciói: ω (S) = 40%, ω (O) = 60%.
Az X elem tömegtörzsét a HX kompozíció molekulájában a következő képlet segítségével számítjuk ki:
ω (X) = n × Ar (X) / M (HX) × 100%.
Jelöljük meg az összetevők móljainak számát, amelyek az "x" (kén) és az "y" (oxigén) vegyületet alkotják. Ezután a mólarány így fog kinézni (a DI Mendeleev periódusos táblázatából vett relatív atomtömegek értéke egész számra kerekítve):
x: y = ω (S) / Ar (S). ω (O) / Ar (O);
x: y = 1,25. 3,75 = 1. 3.
Ezért a kén oxigénnel való összekapcsolására szolgáló képlet SO3 formában van. Ez kén-oxid (VI).
Számoljuk ki, mennyi magnézium-oxidot termelünk magnézium égetésével 6,4 g oxigénben!
Írjuk le a magnézium oxigénnel való kölcsönhatásának reakciójára vonatkozó egyenletet:
Az oxigén mennyiségét az alábbi képlet segítségével számoljuk ki:
Ehhez meg kell jelölni az oxigén móltömegét (a DI Mendeleyev periodikus táblázatából vett relatív atomtömeg értéke a legközelebbi egész számra). Mint ismeretes, egy molekula móltömege megegyezik a molekulát alkotó atomok (M = Mr) relatív atomtömegének összegével:
M (O2) = 2 × Ar (O) = 2 × 16 = 32 g / mol.
Ezután az oxigén mennyisége:
n (O2) = 6,4 / 32 = 0,2 mol.
A reakció n (O2): n (MgO) = 1,2 egyenlet szerint:
n (MgO) = 2 × n (02) = 2 × 0,2 = 0,4 mol.
Találjuk meg a magnézium-oxid móltömegét (ebben az esetben érvényes az oxigén móltömeg kiszámításánál feltüntetett feltevés):
M (MgO) = Ar (Mg) + Ar (O) = 24 + 16 = 40 g / mol.
Határozza meg a magnézium-oxid tömegét:
m (MgO) = n (MgO) xM (MgO);
m (MgO) = 0,4x40 = 16 g.