Elektron transzfer - energia átalakítása egy cellában
Az elektronok a hidrogén atomok, kiválasztott szubsztrátok a Krebs-ciklus szállítjuk, hogy az elektron transzport lánc, más néven az elektron transzport lánc (ETC), vagy légzési vagy a légzési lánc, és a hidrogén-H + ionok átjut a vizes közegben. CET áll több molekulák különböző jellegű, hogy könnyen vissza (felvesznek elektronokat) és oxidált (elektrondonor). Ehhez áramkör az elektronok átkerülnek lépésenként, így az energia, amíg nem érkezik meg a végső akceptor egyik hordozóval, hogy egy másik, és kis részletekben - oxigén (ábra9, 11). Csatlakoztatása elektronok oxigén, hogy készítsen citokróm-oxidáz vagy citokróm komplex (a + A3), kíséri felszívódását 4 protonok H +. Ennek eredményeképpen vízmolekula képződik:
A gáz halmazállapotú hidrogén és oxigén keveréke, amelyet csörgő gáznak neveznek, könnyen felrobban, hogy vizet képezzen. Nagyon rövid idő alatt, hő, fény és hang formájában jelentős mennyiségű energiát szabadítanak fel, amely nem tárolható közvetlenül. A légző láncban ez az energia kis részeken felszabadul az elektronátvitel minden egyes szakaszában. Ez lehetővé teszi a reakciót enyhe körülmények között 37 ° C-on és 1 atm nyomáson, és a kibocsátott energia jelentős részét proton gradiens formájában tárolja a belső mitokondriális membránon. A gradiens energiájának köszönhetően az ATP-k szintetizálódnak. A Krebs-ciklus egy forradalmára 8 elektront táplál be az elektronszállító láncba, amelynek energiája miatt a 36 H + protonok átjutnak a mitokondriális membránon keresztül. A protongradiensben tárolt energiát felhasználhatjuk 9 ATP molekula szintézisére.
Elektronikus szállítási lánc
Amikor elektronátvivő végzett redox reakciók elektronemittáló transzporter molekula egymás után oxidált vagy redukált (vagy csatolt adott elektronok, sorrendben). A molekulák transzporterek lokalizált elektronok a rendszerhez p-szinteket a szerves molekulák konjugált kötések (piridin, flavinok, kinonok) vagy fém atomok egy változó vegyérték, mint például a vas (Fe 2+ # 45; Fe 3+) vagy réz (Cu + # 45; Cu 2+). A Krebs ciklus szubsztrátumaiból az oxigénbe való átvitel során (11. Ábra) az elektronok fokozatosan alacsonyabb energiaszintre váltanak. Ebben a folyamatban a tápanyagok energiájának nagy részét felszabadítják és tárolják. Az elektronok átadása a CET-ben háromféle módon történik: (a) közvetlen átvitel, mint a reakcióban: Fe 3+ + e # 45;> Fe 2 +; (b) a hidrogénatom (azaz a H + és e # 45; ) és (c) hidridion-transzfer: H # 45;. azaz proton, amelyet két elektron egyidejűleg tartalmaz. Az oxidációs redukciós folyamatok leírására a "redukciós ekvivalens" kifejezést használjuk, amely az átvitel módjától függetlenül az elektron transzfert jelenti.
A három bekezdés Krebs-ciklus enzimek malát-dehidrogenáz, izocitrát-dehidrogenáz, és egy-ketoglutarát-dehidrogenáz két atomot tartalmaz a N szubsztrátok malát, izocitrát és ketoglutarát és át az egyiket a koenzim nikotinamid-adenin-dinukleotid (NAD +) formájában egy hidrid-ion: H # 45; (12A. A H + proton formájú második hidrogénatom ebben az esetben a vízhez jut:
R-CH 2-OH + NAD +> NADH + R-C = O + H + (vízben)
Továbbá a NADH-dehidrogenáz enzim koenzim FMN (flavinadenin mononukleotid) két redukciós ekvivalensével rendelkezik hidrid-ion formájában: H # 45; NADH:
NADH + H + + FMN> NAD + + FMNH2
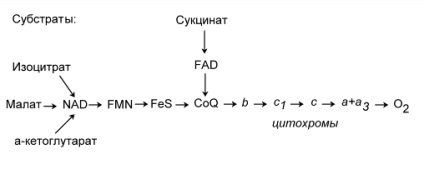
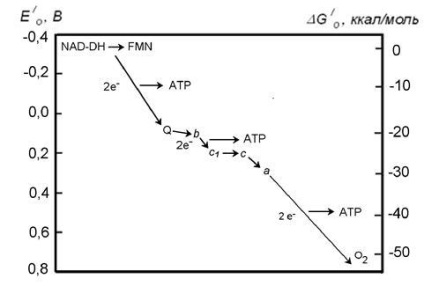
11. ábra - Az elektronikus szállítás lánca. A. Az elektron hordozók sorrendje a CET-ben. B. ábra, amely vázlatosan mutatja a CET különböző szakaszaiban kibocsátott energiát
A hidrogént ezután Q koenzimre (CoQ) viszik át:
Molecular CoQ elektronok átkerülnek egyenként egy lánc citokrómok fehérjék és továbbá az oxigén, ami ebben az esetben van kötve a H + ionokat képeznek vízmolekulák. Amikor elhaladnak a elektronpár ezen az úton a legnagyobb mennyiségű energia szabadul fel (11. ábra). Valóban, az adatokat a redoxpotenciálok különböző szakaszaiban elektron transzfer, a 3. táblázatban, akkor lehet számítani, megfelelő értékeket a standard szabad energia változás. Az energia különbség elektronok átvitelét párja között end link ETC (½ O2 + 2H + + 2e # 45;> H2 O), és az első kapcsolat (NAD + + H + + e # 45;> NADH): = -37,6 - 2 • 7,36 = - 52,3 kcal / mol.
Légzési arány: az elfogyasztott foszfát és az elfogyasztott oxigén aránya P: 0 a becslések szerint 3: 1, azaz. az oxigénatom két elektron által hordozható elektron általi redukciója lehetővé teszi, hogy 3 molekula szervetlen foszfátot 3 ADP molekulához adjunk, amely 3 ATP molekulát ad. Ehhez normál körülmények között 3 (-7,3 kcal / mol) = -21,9 kcal / mol szükséges, azaz. hatékonyság ez a folyamat körülbelül 42%.
Egy másik eleme a Krebs-ciklus, szukcinát, a szukcinát-dehidrogenáz enzim kofaktor flavin-adenin-dinukleotid (FAD) szintén kiválasztja két hidrogénatom (Ris.8,11), és tulajdonít nekik CoQ, ahol a két átadó redukáló ekvivalens. Ebben az esetben, a folyosón a rövidebb rész ETC szintetizált csak két ATP molekula. De így nem kevésbé, de energiát igényesebb, mert a szukcinát-dehidrogenáz hatékonyabb.
3. táblázat: A mitokondriumok elektronszállító láncának komponenseinek redox reakciói (félig reakció)
A mitokondriumok elektronszállító láncának komponenseinek redox reakciói (fél reakció)