Réz-szulfát és tulajdonságai


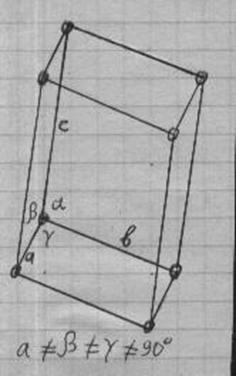
Réz-szulfát CuSO 4 kikristályosodik vizes oldatok réz-szulfát (lásd alább.), És a jelentése egy fényes kék kristályok triklin rendszer rácsparamétereket: a = 7, 15 # 506;. b = 10. 70 # 506;. s = 5,97 # 506; ; a = 97 ° 44 ' # 946; = 125 ° 20 ' # 947; = 94 ° 19 '; sűrűsége 2, 29 g / cm3.
Fölé hevítve 105 ° C-on olvad részleges elvesztése kristályvizet, és megváltoztatja CuSO 4 H 2 O 3 (kék) és CuSO 4 H 2O (fehér). Teljesen dehidratált hőmérsékleten 258 ° C-on Az intézkedés alapján száraz NH3 kialakítva CuSO 4 CuSO 4 5NH 3. cseréje a nedves levegőn NH3 H 2 O. A alkálifém-szulfátot CuSO 4 formák egy kettős só típusú Me 2SO 4. CuSO 4. 6H20 festett zöldes színű.
Az iparban, a réz-szulfátot oldásával nyert fém rézzel fűtött hígított H 2SO 4 levegővel buborékolás: Cu + H 2SO 4 + ½ O 2 = CuSO 4 + H 2 O. Ez is egy mellékterméke elektrolízises finomításhoz réz.
A rézszulfát a réz legfontosabb technikai sója. Ezt alkalmazzák előállítására ásványi festékek, a fa impregnálására, leküzdésére kártevők és növényi betegségek a mezőgazdaságban, az öntet a szemek, a barnító, a gyógyászatban, a galvánelemek; kiindulási anyagként szolgál más rézvegyületek előállításához.
Réz-szulfát (réz-szulfát) CuSO 4 - színtelen kristályok 3 sűrűségű, 64 g / cm 3. Amikor fűtött disszociál: CuSO 4 = CuO + SO 2 + ½ O 2 intermedier termék kialakítására mag-szulfát CuO. CuSO 4. 766 ° C-on a nyomás disszociációs CuSO 4 eléri a 287 mm-es. higanyoszlop és CuO. CuSO 4 - 84 mm. higanyoszlop. A CuSO 4 oldhatósága grammban 100 grammban. a víz: 14 (0 ° C); 23, 05 (25 ° C); 73, 6 (100 ° C). A szabad H2S04 jelenlétében az oldhatóság csökken. PH = 5, 4 - 6, 9 CuSO 4 hidrolizáljuk képezhetnek bázisos sókat képeznek. CuSO 4 higroszkópossága, így használják, mint egy szárítószer; rögzítené víz kék, néha használják kimutatására a víz alkohol, éter és mások.
Réz vitriol - fényes kék kristályok.
Melegítéskor a réz-szulfát elveszti a vizet, és szürke porrá válik. Ha hűtés után néhány csepp vizet csepegtet rajta, a por ismét kék színű lesz.