Delokalizációja molekulapálya fémek - az abszolút minimális
Delokalizáció molekulapálya fémekben
Hogyan elektronok mozoghat egy fémdarab? Mi a különbség egy fém és egy szigetelő? Mi egy félvezető? Miért fémek melegítünk mozgását elektronok? Mi szupravezetés?
Válaszként az első három kérdésre, meg kell kiterjeszteni a vitát a kiterjesztett molekulapályák, hogy mi található molekulák aromás vegyületek, mint például a benzol és a naftalin (lásd CHAP. 18) MO makroszkopikus darab fém és egyéb anyagok. A választ az utolsó két kérdésre kell elmozdulni vita hatására a termikus rezgések az atomok, amelyek egy fémdarab, hogy megvitassák a mozgás az elektronok a fém.
10. fejezet a hidrogén molekula a vita, kiderült, hogy két atomi hidrogén kombinálódhatnak a két molekulapályák - kötés és antibonding. Abban az esetben, benzol, azt láttuk, hogy a hat atomi pz pályák - egy-egy minden egyes szénatom - formában három kötési és három antibonding MO. Tíz naftalin pz atomi pályák együtt alkotnak tíz MO - összekötő öt és öt szétesést. Minden esetben, a Honvédelmi Minisztérium fedezi a teljes molekula. A 11. fejezetben, szentelt a periódusos, azt mondtuk, hogy a nátrium (Na) egy fém, mert van egy elektron (3S) felett neon zárt héj konfigurációban. Na ilyen könnyen ad egy elektront a sókat képeznek, mint például asztali só NaCl. NaCI-ot feloldunk vízben, és alakítjuk az ionok Na + és Cl -. Mint már említettük, a szilárd állapotban van Na fém és vezeti az áramot, és most már készen van, hogy miért.
Tekintsük kiindulási 3S orbitális két nátrium atomok, amelyek szomszédosak egymással, és kölcsönhatásba. A nátrium-3s elektronja egy vegyértéke, amely részt vesz a kialakulását a kötések. A felső részén a ábra. 19.2 ábra az energia szintjét a két 3s atomi pályák, a molekulapályák a kombinálásával. Az energia szintje egy ilyen MO alacsonyabb, mint az atomi pályák. Ez köti össze MO. Egyéb MO magasabb energia szinten - antibonding orbitális. A középső része az ábra azt mutatja, hogy a három atomi pályák alkotnak három MOS. Mutatja a helyzet hat együttműködő nátrium atomok. Hat 3s atomi pályák egyesítjük hat MI - három kötési és három antibonding.
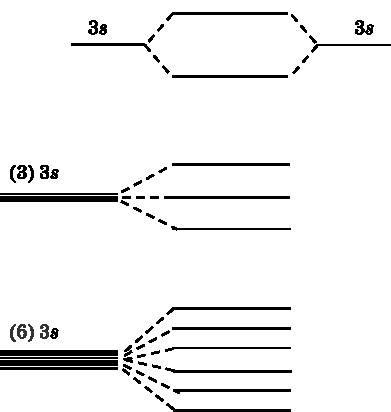
Ábra. 19.2.Vverhu: 3s-két atomi pályák nátrium kölcsönhatásba, és ezáltal két molekulapályák - az egyik egy kis energiájú (kötés) és egy magasabb (antibonding). A középső három atomi 3s-reagálnak, és ezáltal három Mos. A földszinten: hat nukleáris-3s pályák egyesítjük hat MI
Minden atom van egy Na 3s-elektron, ami megy, hogy töltse MO. Egy rendszer hat nátrium atomok töltésére MO lesz hat elektronokat. Mindegyik MO tudja fogadni két elektron ellentétes pörgetés (egy felfelé irányuló, a másik - lefelé). Ezért a három MO tele lesz elektronokból legalacsonyabb energiájú, azaz összekötő MO. Három MO magasabb energiák üres lesz.
Most meg kell vizsgálni, hogy mi történik abban az esetben, igen nagyszámú kölcsönhatásban nátrium atomok. Vegyük rúd hossza 10 cm, átmérője 1 mm. amely nátrium (lásd. ábra. 19.1). Ilyen méretek a száma, Na atomok, amelyek tartalmaznak egy rudat, legyen N = 2 • Október 21-ig (kétmilliárd billió) Na atomok. Két milliárd billió atomi pályák 3s együttes két milliárd billió molekulapályák. Mivel abban az esetben, a benzol és a naftalin MO, MO nátrium-rudat kell tekinteni kiterjesztve az egész rendszer, hogy van, az egész darab fém.