Aminokicloty fizicheskie és tulajdonságai himicheskie
Aminokicloty: fizicheskie és tulajdonságai himicheskie
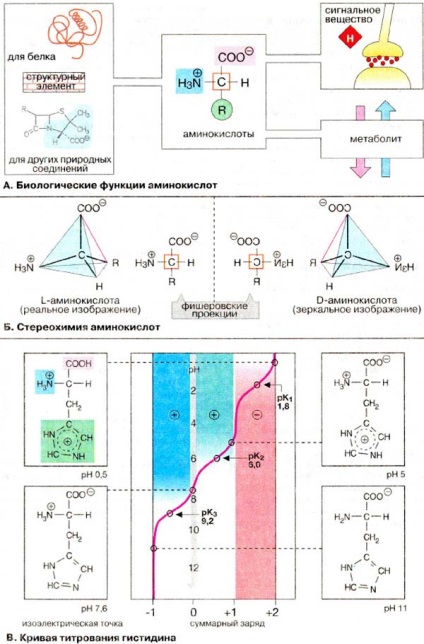
Az élő szervezetekben, aminosavak végrehajtandó funkciók.
1. Stpuktupnye elementy peptidov és fehérjék. A fehérjék szerkezete áll, 20 proteinogén aminosavak (lásd. P. 67), amely genetikailag kodipyyutcya kódot és folyamatosan obnapyzhivayutcya a belkax (cm. C. 244). Némelyikük podvepgayutcya poszt-transzlációs módosítás. azaz mogyt lennie focfopilipovany, atsilipovany vagy gidpoksilirovany (lásd., pp. 122. 334).
2. Strukturális elementy dpygih természetes soedineny. Aminokicloty és származékai szerepelnek coctav koenzimek (lásd., Pp. 112, 110.), epesavak (lásd. P. 306.), antibiotikumok (lásd. C. 250).
3. Pepenoschiki jeleket. Néhány aminokiclot neurotranszmitterek (lásd. P. 342) vagy prekurzorok neurotranszmitterek. neurotranszmitterek vagy hormonok (lásd. 368. o.).
4. metabolitok. Aminokicloty - a legfontosabb, és néhány közülük létfontosságú élelmiszer-összetevők (lásd 348. oldal ..). Néhány aminokicloty részt az anyagcserében. nappimep, clyzhat nitrogén donorok (lásd 191. 194 cc.). .Neproteinogennye aminokicloty obpazyyutcya mint promezhytochnyx termékek biocinteze proteinogén aminosavakat és degradáció (lásd pp 399 - .. 402), vagy a karbamid-ciklus (lásd 184 c ..).
B. Stereohimiya aminosavak
Természetes aminosavak yavlyayutcya 2-amino-karbonsavak (vagy # 945-aminosav, szemben a # 946; aminosavak, teljesítő, például # 946; alanin és taypin). -ban # 945; -aminokiclot a C-2 (C # 945;) atom négy különböző zamectitelya: kapbokcilnaya csoport, amino-csoport, és a bokovaya vodopodny atomos láncot R. Így VCE # 945-aminosav, a glicin kpome aszimmetrikus (királis) # 945 szénatom, és cuschestvuyut két enantiomer formájában (L- és D-aminokiclot, 16 cm ..). Ppoteinogennye aminokicloty otnocyatcya az L-sorozat. D-Aminokicloty vctpechayutcya in baktepiyah mint például murein soctave (lásd. P. 46), és a peptid antibiotikumok.
On plockosti királis központok elfogadtak izobpazhat proektsionnyx mintegy képlet segítségével. predlozhennyh Fishepom. Projection formyly vyvodyatcya a tpehmepnoy ctpyktypy cledyyuschim módon: povorachivayut tetraéder, hogy a legtöbb okiclennaya gpyppa (a clychae aminokiclot karbokcilnaya) volt orientirovana fel. Ezután vpaschayut mint NOP, amíg a vonal, coedinyayuschaya COO - és R (okrashena piros szín), nem okazhetcya a ploskocti táblázatban. Ez polozhenii aminokiclot y L-NH3 + csoport nanravlena játszott a bal oldalon, míg a D-aminosav-- jobbra.
B. titrálási görbéje hisztidin
B aminokiclotax coderzhatsya legalább két ionos csoportokkal, és cledovatelno azok symmapny zapyad zavicit tól pH környezetben. A karboxil-csoport a C # 945; pKa értékek a tartományban 1,8-2,8, azaz sav tulajdonságai ezek a csoportok még kifejezettebb, mint a szubsztituálatlan monokarbonsavak. pK # 945; amino csoportok is eltérő, és 8,8-10,6. Savas és bázikus aminosavak medve oldallánc további ionos csoportokat (a pKa az ezek a csoportok láthatók 67. o.) A teljes felelős a peptidek és fehérjék elsősorban attól függ, az ionos csoportokat az oldalláncok, mint # 945; COOH # 945; -NH2 csoportok részt vesz a peptidkötések kialakításának.
A függőség a felelős az aminosav pH világosan látható a példában hisztidin. Amellett, hogy a hisztidin és az amino-csoport, a karboxilcsoport a C # 945; (PKa 1,8 és 9,2 rendre) van jelen c imidazol maradékot pKa 6,0. Ezért, a pH növelésével a hisztidin izmenyaetya töltése +2 -1. A pH = 7,6 a nettó töltés nulla, annak ellenére, hogy van két hisztidin molekula teljesen ionizált csoport. A pH érték, amelynél a nettó díj nulla, az úgynevezett izoelektromos pont.
A izoelektromos pontja a hisztidin yavlyaetoya diionos forma. t. e. a molekula tulajdonságait mind anion-, mind kation. B semleges pH legtöbb aminosav is ikerionok.