A iniciációs a gyökös polimerizáció
képezhet szabad gyökök hatására kémiai és fizikai tényezők, így kezdeményező gyökös polimerizációs vannak osztva fizikai és kémiai (lásd reakcióvázlat)
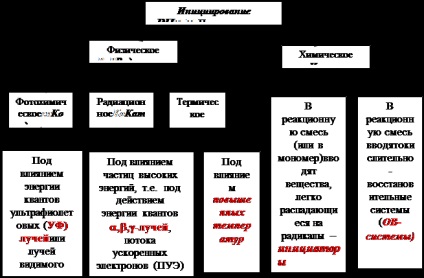
A polimer gyártási technológia előnyösen elosztott kémiai módszerek iniciációs, ha a reakcióelegyet bevezetjük iniciátorok (J) - olyan anyagok, amelyek bizonyos körülmények között könnyen gyökökké bomlanak.
A csoport a iniciátorok közé tartoznak a következő anyagok (10. táblázat)
10. táblázat-típusú gyökös polimerizációs iniciátorok
Formula (általában)
A mechanizmus a bomlás gyökökké
Specifikus képviselők a iniciátorok, a feltételeket és mechanizmusa bomlása a 11. táblázatból látható.
Egyszerű és gyors bomlása iniciátor csoportok fordulnak elő kapcsolatokról oxigén - az oxigén vagy szén - a nitrogén, mivel ezek a kötvények rendelkeznek kisebb szilárdságú (kötési energia).
A kötődési energiát, kJ / mol
A legkisebb bomlási hőmérsékletéig (50 ÷ 85 0 C-on), és rendre legkisebb aktiválási energia (Ea) y iniciátorok, mint például ammónium-perszulfát, dinitril azobisizomaslyanoy sav, benzoil-peroxid. Ezek az iniciátorok nem leggyakrabban használtak a gyökös polimerizáció.
Redox rendszerek (OS-System) - egy átfogó rendszer, amely tartalmaz egy oxidálószert és egy redukálószerrel (promoter). Szerepe oxidálószer leggyakrabban játszott fent idézett iniciátorok J (peroxidok, hidroperoxidok és mások.). Promoter egy anyag, amely felgyorsítja a bomlás szabad gyökök iniciátorok. Promóterek OB rendszerek fémsók változó vegyértékű egy alacsonyabb oxidációs állapotba. mint például a vas-klorid, vas FeCl2. vegyértékű réz-klorid CuCl, kobalt-naftenát, nikkel-naftenát (), stb Amellett, hogy ezeket promoterek, a szerepét aminok, szulfitok, stb a festékiparban promoterek - .. szikkatív úgynevezett polimerizációt gyorsító.
A hatásmechanizmus redox rendszer eltérő. A legegyszerűbb rendszerben OB Fenton-reagenssel - keveréke hidrogén-peroxid, H-O-O-H és vas-klorid FeCl2. Ebben a rendszerben, Fe 2+ kation instabil könnyen elveszti egy elektron e „és továbblép a legmagasabb oxidáció mértéke. Fe 3+. Az elkülönített elektron gyorsítja hidrogén-peroxid bomlását HO ----- O-H ion DK - és a radikális HO ·.
A szétesési iniciátorok gyökökké jelenlétében OB-rendszerek nagyon gyors, és az aktiválási energia a kezdeményezés szakaszában alkalmazásával OB rendszerek alacsonyabb használatakor csak egy kémiai iniciátorok (E a és (S) <Е а и (J) ). Обычно энергия активации окислительно-восстановительного инициирования Е а и (ОВ ) составляет 42÷84 кДж/моль, а энергия активации инициирования с применением только инициаторов Е а и (J) равна 112÷170 кДж/моль.
Kezdeményezése a Lengyel Köztársaság, azaz a szabad gyökök képződését két stádiumban megy végbe. amely sematikusan a következőképpen:
a) kialakítunk egy radikalovJ · eredményeként bomlása molekulák initsiatoraJ:
b) képződése aktív gyökök rostaJ- M · molekulák monomerovM:
A példa a vinil-klorid monomer, ez a reakció a következő:
A kezdeti szakaszban (a) mindig szükség az aktiválási energia Ea és költség áramlik a kis sebességű, és korlátozza az egész folyamatot. Nem az összes iniciátort gyökök okozhat J · második b) lépésben, és a képeznek gyököket rostaJ- M +.
Rész iniciátort gyökök eltűnnek a rekombinációs reakció előfordulását fordított J · + J · = J2.
Fotokémiai iniciációs használják ritkábban, mint a kémiai. Amikor a fotokémiai iniciációs monomer M molekulák energiát elnyelni QUANTA (hn) hullámhosszú sugárzást a 100 nm Az aktivációs energia E fotokémiai iniciációs és (y / x) lényegesen alacsonyabb, mint az aktiválási energia a tisztán kémiai iniciációs és E egy (E a és (y / x) <<Е а и (J) ) и близка к 0 (Е а и (ф/х ) » 0 кДж/моль). Вследствие этого фотохимическая радикальная полимеризация может протекать при низких и даже отрицательных температурах. Azonban, a csillapítás mértéke a monomerek gyökökké, ha UV sugarak vagy látható sugárzás (VI) alacsony. Annak érdekében, hogy felgyorsítsa a fotokémiai polimerizációs alkalmazásával 2 vétel: 1. Írja be a monomer anyagok - fotoiniciátorok 2. Írja be a monomer anyagok - fotoszenzibilizálókkal. A fotoiniciátorok - olyan anyag, amely alatt a hatás az energia az UV sugarak vagy VI - sugárzás könnyen gyökökké bomlanak, mint a monomerek maguk. Fotoiniciátorok haloalkiiok (szén-tetraklorid CCI4. 1.2 -trihloretanC2 CL6), szerves fémvegyületek. A hatásmechanizmus CCl4 következő: A fényérzékenyítő - olyan anyagok, amelyek elnyelik és felhalmozódnak energiát UV sugarak vagy VI - sugárzással szélesebb hullámhosszúságú, mint a monomer, akkor a nagyobb értéket kap a felhalmozott energia részek monomert. monomer molekulák gyorsan mozdulnak el egy gerjesztett állapot és gyökökké bomlanak. A szerepét fotoszenzibilizálókkal tartalmazó anyagok a szerkezetükben egy konjugált kettős kötés (kromofor csoportok) vagy aromás gyűrűk, például fluoreszcein vagy dibenzfenon A hatásmechanizmus fényérzékenyítő (F) a következő: + Hn F F * F * F + M + M * M * M · + M · 11. táblázat - A bázikus csoportokat a gyökös polimerizációs iniciátorok, a mechanizmus és feltételek azok bomlásKapcsolódó cikkek