Onnaya polimerizáció
Az elméleti rész. A szintetikus polimerek által termelt polimerizációval vagy polikondenzációval.
Polimerizáció - A vegyület reakciója több molekula, ahol nem kapott, és nem választja el-termékek, és az egységeket alkotó polimer és a monomer azonos elemi összetételű, vagy más szavakkal, a polimerizáció egy összekötő kisméretű monomer molekulák (miatt többszörös kötéseket, vagy gyűrű-nyílás) a kapott hosszú láncú polimer nevű molekula makromolekula. Általában a polimerizációs eljárás leírható a rendszer:
ahol M - a monomer molekulát, M „- a monomer egység a makromolekula, N - az egységek száma a polimer láncban.
A kémiai jellege a ismétlődő egységet és egy polimerizációs foka a polimer meghatározzuk tulajdonságait. A polimerizációs a telítetlen monomerek zajlik törvényei szerint a láncreakció. Az a képesség, a lánc polimerizációs egy karakterisztikus tulajdonsága a dién és vinil-vegyületek. Ez okozza a jelenléte a molekulában a vegyületek a kettős kötések. Mivel az energia a π-kapcsolat körülbelül egyenlő 218 kJ / mól, és a α-kapcsolatot - mintegy 353 kJ / mól, a π-kötés reakcióképesebb. Ezért a polimerizáció lép fel nyúlás π-kötés.
A tulajdonságait elasztomerek függ nemcsak a típusú monomer, hanem a jellegét és feltételeit polarizáció.
A polimerizációs eljárás három szakaszból áll:
Megindítása - kialakulását egy aktív centrum A → A *;
Magasság lánc A * + A → AA * → An + 1, A *, stb.;
Külön szakaszok különböznek lánc polimerizációs sebesség és a termikus hatás. A aktiválási energiája az aktív központ az oktatás magas, és a reakció viszonylag alacsony sebességgel.
Jellemzők lánc polimerizációs folyamat természete határozza meg az aktív hely (kation, anion, fókuszpont).
Kétféle polimerizációs: szabadgyök és ionos (kationos, anionos, ion-koordináló).
Ionos polimerizációs izgatott vegyületek képzésére alkalmas ionok szénhidrogén közegben, kivételes szelektivitással monomerek és számos jellemzői és előnyei:
Ez erősen függ az oldószer polaritásától;
Úgy folyik a nagy sebesség és jelentősen alacsonyabb aktiválási energia;
A polimerizációt végezhetjük hőmérsékleten elérve akár -100 ° C-on
Alacsony hőmérséklet, a magas polimerizációs sebesség, és az orientáló hatást az aktív centrum a katalizátor a monomer molekulában vezet az a tény, hogy ezek a molekulák kapcsolódnak egy bizonyos sorrendben egymással, és így képezhetnek:
Polimerek nagy molekulatömege és viszonylag szűk molekulatömeg-eloszlással.
Vázlatosan kationos (például a sztirol) lehet az alábbi képlettel ábrázolható:
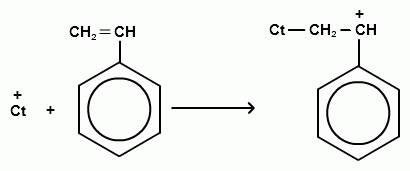
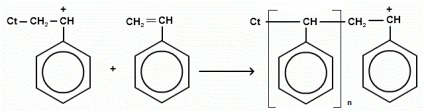
A kationos polimerizációs katalizátorok az erős elektronvonzó anyag:
Friedel-Crafts-katalizátorok - BF3, AICI3, SnCl4, TiCl4, SbCl 5, stb.;
Hidrogén sav - H2SO4, HCI, H3PO4, stb.;
Más savak - I2, ICI, IBr, stb
A legtöbb aktív katalizátort sorba vannak rendezve:
BF3 Leggyakrabban használt TiCl4, AICI3, SnCl4, BF3. A katalitikus aktivitás ezen vegyületek jelentősen javul, ha a polimerizálható rendszer, mint szennyezések tartalmaz vizet, hidrogén-halogenidek, alkil-halogenidek és más protikus anyag. Az ionos folyamatok rendkívül érzékenyek a vízre, és a különböző szennyeződések a reakciórendszerben. Így a víz és bizonyos más anyagok szolgálnak kokatalizátorok. A leghatékonyabb ko-katalizátorokat két csoportba lehet sorolni: Vegyületek könnyen leadó protonok - a víz, alkoholok, hidrogén-sav; Típusú vegyületek az alkil-halogenid, amely képes alkotnak karbónium kation. Kinetics kationos polimerizáció áll az a tény, hogy a: Az általános polimerizációs sebesség egyenesen arányos a tér a monomer koncentrációja, és a katalizátor koncentrációja az első fokú; A polimerizáció foka egyenesen arányos az első monomer koncentrációja, és független a katalizátor-koncentráció; A teljes aktiválási energia függ, beleértve a hőmérsékletet - az alsó van, annál nagyobb a polimerizáció sebessége. Hatása oldószer: sebessége és mértéke polimerizációs növekedésével növekszik oldószerrel dielektromos konstans értékek, és nem is függ az oldószer jellegétől. Célkitűzés: előállítása polisztirol sztirol- blokk az intézkedés alapján a kationos típusú katalizátort és annak elválasztása kicsapással a reakciórendszerből. Reagensek. Sztirol, nátrium-hidroxid, ón-tetraklorid, diklór-etán, izopropanolt, a keveréket lehűtjük (jég nátrium-klorid). És evőeszközök: Kúpos lombikot lezártuk 50 ml-es választótölcsérbe, üvegampullák, porcelán csésze, Dewar, üvegbot. Eljárás: Keverjük össze egy üvegampulla 4 ml sztirolt és 2 ml katalizátor (1 ml SnCl4 30 ml diklór-etánban). Azt hogy a fiolát Dewar edényben (a hűtési elegyet -20 ° C hőmérsékleten). Polimerizációt oly módon végezzük 15 percig. 15 perc elteltével a keveréket megvastagodott, és mozgatni, hogy egy porcelán csésze izopropanollal, ahol a polimer kicsapódik. Öntsük ki az első része a kicsapószer, és adjunk hozzá még egy kis mennyiségű izopropanolt amely mossa ki az anyagot. Merge teljes polimer izopropanol és nyomjon egy vékony rétegben az a csésze alján. Hagyjuk megszáradni füstszekrényben. Initiation: A katalizátor komplex formák szennyeződések dissotsiiruya vegyületet ionokra: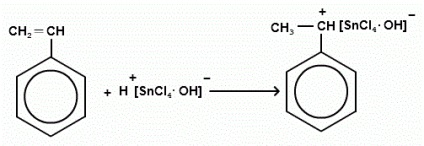
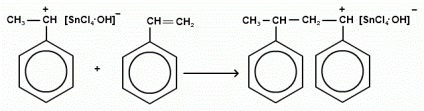
Nyílt lánc: a lánc megszűnése áll csatlakozni a negatív macroion karbóniumionnak katalizátor.
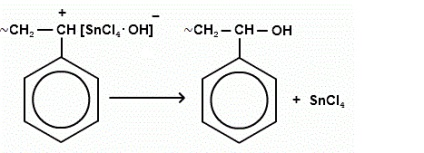
megszűnése lánc növekedés gyakran társul egy elválasztó negatív hidrogén-ion katalizátor a polimer láncban.
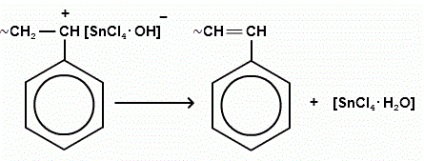
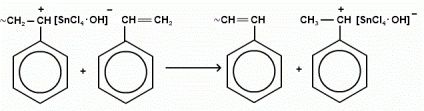
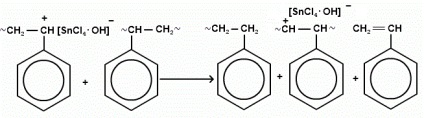
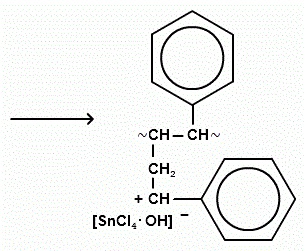
A súly a kapott polimer:
elméleti tömege a polimer:
Kiszámítása átalakítás:
A reakció hozama számítás: