Összegének kiszámításakor kicsapó
Ha porleválasztó illékony, akkor ajánlott használni a két - háromfogásos időben a felesleges; ha porleválasztó nem illékony használni 30-50% feleslegben.
Számítsuk ki a térfogatát egy 2% ezüst-nitrát oldattal sűrűsége 1 g / ml szükséges, hogy kicsapjuk a klorid anion a minta tömege CaCl2 • 6H2O 0,4382 g
Egy sor ezüst-nitrát kicsapásához szükséges a klorid anion formájában ezüst-klorid.
Mi a törvényt ekvivalens:
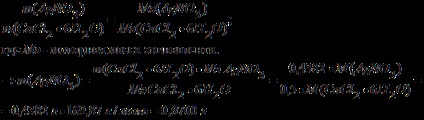
Találunk a tömeg egy 2% -os ezüst-nitrát oldat:
Az oldat térfogata megegyezik a tömege az oldat, t. K. A oldat sűrűsége 1 g / ml. Következésképpen, a térfogata az oldat 34,00 ml.
Milyen mennyiségű 5% -os ezüst-nitrát oldat sűrűsége 1 g / ml szükséges ezüst-klorid válik 200 ml 0,01 M sósav-oldatot.
Megtalálása tömeg sósav 200 ml 0,01 M oldat.
Keresse meg a tömeg az ezüst-nitrát egyenértékű a törvény:
Egy sor 5% ezüst-nitrát oldat.
Térfogatú 5% -os oldat egyenlő az oldat tömegére vonatkoztatva, t. K. A oldat sűrűsége 1 g / ml. Következésképpen, a térfogata az oldat 6,8 ml.
További teljes kiválását vesszük, hogy 30% -os feleslegben precipitáló:
Vrastvora = 6,8 ml • 1,3 = 8,84 ml.
Számítsuk ki a súlya 5% kénsav oldatot, hogy kicsapjuk ólmot 0,5865 g mintát tömegű frakció 12% ólmot tartalmaz.
Találunk sok ólom a mintában:
Azt találjuk, a masszát tiszta kénsav kicsapása vezetést. Mi a törvényt ekvivalens:
Egy sor 5% -os kénsav oldat:
Határozzuk meg a kötet egy 2% -os oldatának 8-hidroxi-kinolin sűrűsége 1 g / ml-venni a 10% feleslegben, a teljes kicsapódását 8-gidroksihinolyata magnézium 100 ml oldatban, amely 50 mg magnézium.
Az összeg a precipitáló megtalálható joga szerint ekvivalens, vagy a reakcióegyenlet:
MgCl2 + 2C9H6NOH Mg (C9H6NOH) 2 + 2 HCI
Arra számítunk, hogy térfogata kicsapó oldatot:
A tömege az oldat az oldat térfogatát, azaz. K. sűrűsége 1 g / ml. Következésképpen, az oldat térfogatával egyenlő 7,5 g 1 • g / ml = 7,5 ml. Kötet kicsapószer kivett oldat 10% -os fölöslegben van 7,5 ml • 1,1 = 8,25 ml.