Előadás a téma a leckét - salétromsav - a célból, hogy a lecke 1
Bemutatása a tárgya „Chemistry” a „téma LECKE” salétromsav „Purpose :. 1. megismertesse fizikai és kémiai tulajdonságait a salétromsav elektrolitként 2. javítani.”. Letöltés ingyen és regisztráció nélkül. - átirata:
1 Tárgy objektív „salétromsav” Cél 1. megismertesse őket a fizikai és kémiai tulajdonságai a salétromsav, mint az elektrolit. 2. A jobb gyakorlati ismeretek a diákok technikák és módszerek kémiai kísérletet. 3.Vesti felkészítse a tanulókat a vizsgára. lecke mottója „ZNAT- nem árt”

2 Bemelegítés: A1. Az oxidáció mértéke nitrogén salétromsavban A1. Az oxidáció mértéke a nitrogén salétromsav 1) +4 2) +5 3) +2 4) +3

3 előállítása E T A HU 2. A fizikai tulajdonságait az ammónia-nitrogén és az A 2. A fizikai tulajdonságai a nitrogén és az ammónia 1) Gázok 2) Folyékony 3) Szárazanyag

4. előállítás a vizsgára 3. számú a hidrogénatomok a salétromsav (HNO3) 3. Számos monobázikus 1) monobázikus 2) dibázikus 2) dibázikus 3) hidrogénatom salétromsav (HNO3) 1) 3 tribázisos) tribázikus 4) több-bázisú 4 ) több-bázisú

5 készül a vizsgára A4. A4 nitrogén protonok a sejtmagban. A protonok a sejtmagban nitrogén 1) 14 1) 14 2) 28 2) 28 3) 7 3) 7 4) 2 4) 2

6 készül a vizsgára A5. Az anyag, amely után disszociációs vizes oldatban képez hidrogén kationok és anionok A5-maradék. Az anyag a disszociációs hidrogén kationok vannak, amelyek vizes oldatok és anionok savmaradék 1) Acid 2) sol3) osnovanie4) -oxid

7. előállítás E G E B, 1. a következő állítások igaz ammónia, 1. a következő állítások igaz ammónia A. Az ammónia jól oldódnak vízben. B. A készítmény az ammónia-nitrogén oxidációs állapota +5. 1) Egy igazi csak 2) csak akkor érvényes, B 3) egyaránt igaz szűkület 4) Mindkét értékelések nem igaz

8. Fizikai tulajdonságai HNO 3 1. Színtelen folyadék, szúrós szagú. 2. koncentrált salétromsavat (98% plotnost1,51g / cm3) levegő „dohányzik”, mert a levegővel, hogy cseppek keletkezzenek a köd.

9 Osztályozási sav Salétromsav: Salétromsav: -odnoosnovnaya-oxigén-illékony -strongly elektrolit - oldódik vízben

Előállítása sav 10 1.Azotnaya savat ismert ember a 17. század óta. 1.Azotnaya savat ismert ember a 17. század óta. 2.Vpervye tudós Glauber kapott savat a nitrát, a rá ható koncentrált salétromsavval. 2.Vpervye tudós Glauber kapott savat a nitrát, a rá ható koncentrált salétromsavval. 3.Zhyul Verne könyvében: „A rejtelmes sziget” írta le ezt a módszere, salétromsav. 3.Zhyul Verne könyvében: „A rejtelmes sziget” írta le ezt a módszere, salétromsav.

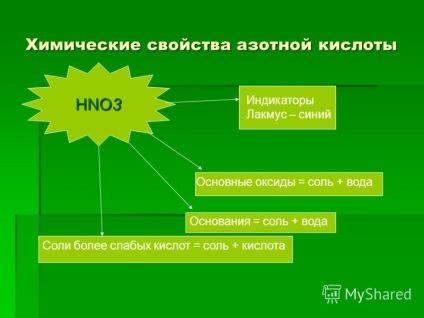
11 A kémiai tulajdonságai salétromsav HNO3 Lakmusz indikátorok - Blue = Alap-oxidok só + víz = Basis só + víz sókat gyengébb savak + sav = só
12 Lab „jellemző tulajdonságai salétromsavat egy elektrolit” Lab „jellemző tulajdonságai salétromsavat egy elektrolit” TB szabályok. TB szabályokat. A munkaterv: A munkaterv: PRACTICE1. sav kölcsönhatás a mutatók. PRACTICE1. sav kölcsönhatás a mutatók. 2. kísérlet Kölcsönhatás a bázisos oxidok. (CuO + HNO 3) savat 2. kísérlet Kölcsönhatás bázikus oxidok. (CuO + HNO 3) savat Kísérlet 3. Kölcsönhatás bázisokkal. (NaOH + HNO 3) 3. kísérlet Kölcsönhatás savval bázisok. (NaOH + HNO 3) 4. kísérlet Kölcsönhatás savas sók gyengébb savak. (Na 2CO 3 + HNO 3) 4. kísérlet Kölcsönhatás savas sók gyengébb savak. (Na 2CO 3 + HNO 3)
13 különleges tulajdonságai, salétromsav. 1. Ha fűtött és hatása alatt a fény salétromsavat elbomlik. 2. Mivel a terpentin reagál robbanásszerűen 3.Drevesnye fűrészpor, papír tömény salétromsavban lángra. 4. Amikor reagáltatunk tömény salétromsavval a fehérje anyag képződik egy világos sárga színű, jellegzetes a savval való reakciót. 5.Vstupaet reagáltatunk nemfémek. (Kén, foszfor, szén)
Gyulladás 15 terpentin tömény salétromsavban.
16 Házi feladat: Házi: 26.§ 4. célkitűzés, 44. oldal 4. lehetőség 26.§ 4. célkitűzés, 44. oldal 4. lehetőség ..
17. Következtetés A tanulság: Salétromsav - erős oxidálószer - az elektrolit kiállított valamennyi jellegzetes erős savak - különleges tulajdonságokkal rendelkezik - meg kell tudni, hogy a tulajdonságok a salétromsav, hogy ne bántsd magad, és a környezetet. - meg kell tudni, hogy a tulajdonságok a salétromsav, hogy ne bántsd magad, és a környezetet. Az anyagot vizsgálták osztályban szerepelnek a KIM CSE (a kodifikatoru (1,3; 2,5; 2,11; 2,8; 2,9,2;)