Hogyan értékeli a molekula méretétől - Bemutató 74863-7
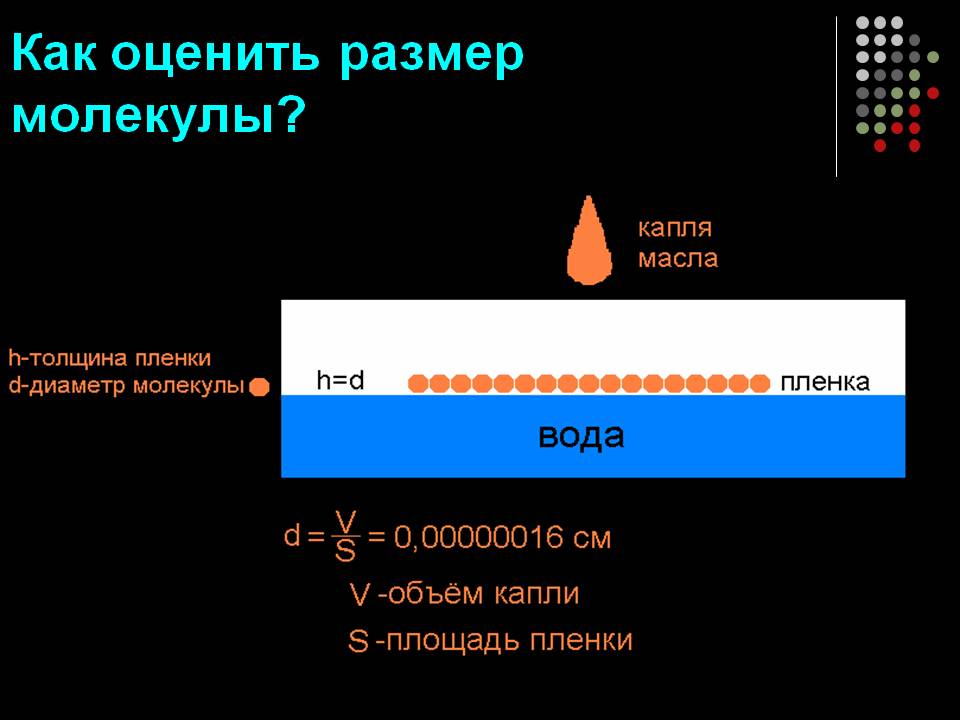
Hogyan értékeli a molekula méretétől?
7. dia bemutatásának „A belső anyag szerkezete”
Méret: 720 x 540 pixel formátumban. jpg. A dia letöltéséhez használata az osztályteremben, kattintson jobb egérgombbal, kép, és kattintson a „Kép mentése más néven. ”. Töltse le a teljes előadást tart „A belső szerkezet veschestva.ppt” lehet zip-archívum mérete 1222 KB.
Kapcsolódó bemutatása
„Location molekulák” - Mik a tulajdonságai szilárd, tudod? Wax. Crystal. Tesztelje magát! Kaotikus mozgások rendezetlen molekulák. A nagy távolságok a molekulák között. Szabályos elrendezése molekulák. Az anyag. Milyen tulajdonságai gázok? Folyadék. Kontraszt az anyag tulajdonságaival, illetve az aggregált állapotok.
„A gázmolekulák” - És akkor kifejezetten a sebesség molekulák képlete: 3. Írja alapegyenletének MKT. Alapegyenletének MKT ideális gáz. 1. Van egy ötlet az ideális gáz mint fizikai modell. Ideális gáz. 2. Értse és felsorolni azokat a mennyiségeket gáz a nyomástól függ érfal. Koncentrációk molekulatömegű molekulák mozgási sebességek molekulák.
„Ammónia-molekula” - Az iparág. Izolálása cseppfolyós levegő. A szerkezet a molekula. Kommunikáció: -kovalentnaya poláros -troynaya -Rugged. Megközelítés. Fizikai tulajdonságok. A laboratóriumban, - bomlása instabil nitrogénvegyületek. Nh4no2. n2 + 2H2O. Ammónia. Molecule: -nagyon rezisztens -Alacsony reaktivitást. Kémiai tulajdonságok.
„A szerkezet a molekulák az anyag” - a harmadik helyen. NH3. CH3Br + H2O. CH3CH2NH2 + HCI. Tulajdonságok. Sysoev ON St. Petersburg IED. 2CH3OH + 2Na. (1828 -1886). A kölcsönösen befolyásolják egymást az atomok a molekulák a példa anilin. 1. pozíció. Ammónium-klorid. 2. pozícióban. Fenilammoniya kloridot. NH3 + HCl. + 2Na. Major típusú szerves anyagok. 2CH3ONa + H2.
„Molekulatömeg” - Mendeleev felfedezett (1869) a periodikus törvény a kémiai elemek. A moláris tömeget. Dmitri Ivanovics Mengyelejev (1834-1907), orosz kémikus, sokoldalú tudós és tanár. Amedeo Avogadro - olasz tudós. Amedeo Avogadro. Mass molekulák. Kommunikációs súlya és anyagmennyiség. Molekulatömegű. A molekulák száma 1 mól anyag volt 6,022045 (31)? 1023.