Példák problémák megoldása
A probléma a tömeghatás törvénye
Hányszor kell változtatni a sebességét egy közvetlen kémiai reakció homogén rendszerben: 2 NO + Br 2 = 2NOBr2
ha: a) növeli a NO koncentráció kétszerese
b) koncentrációjának csökkentésére Br2 háromszor
Mivel a. Államokban, hogy a homogén rendszerben, hogy valamennyi anyag a gázfázisban és azok koncentrációját a képletben a tömeghatás törvénye. Írunk a kifejezés a törvény ebben a reakcióban: 1 = k [NO] 2 [Br 2]
a) koncentrációjának növelésével NO háromszor képletű tömeghatás törvénye a következő lenne: 2 = k [2NO] 2 [Br2] = 4k [NO] 2 [Br2] (2 alatt végzett koncentráció-lemez és emelt annak négyzet). Így 2 / 1 = 4k [NO] 2 [Br2] / k [NO] 2 [Br2] = 4. Következésképpen a közvetlen reakció sebességét növeli 4-szer.
b) csökkentése Br2 koncentráció megháromszorozódott képletű tömeghatás törvénye a következő lenne: 2 = k [NO] 2 [
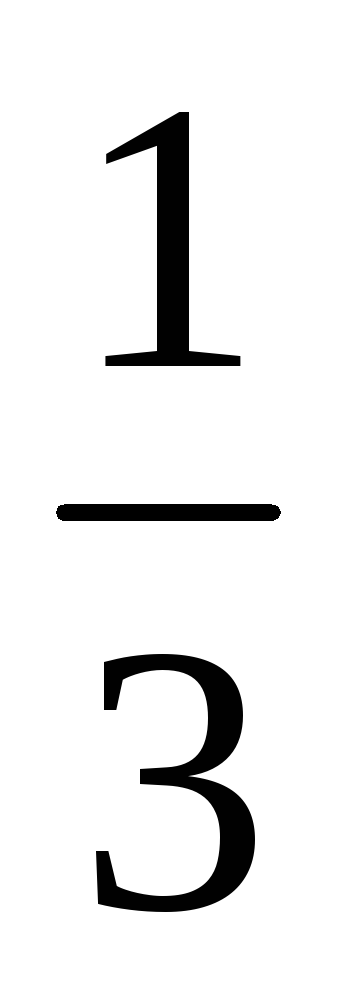
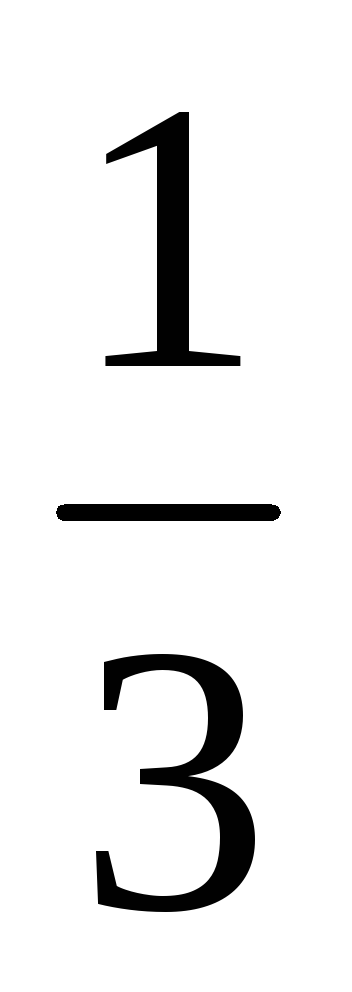
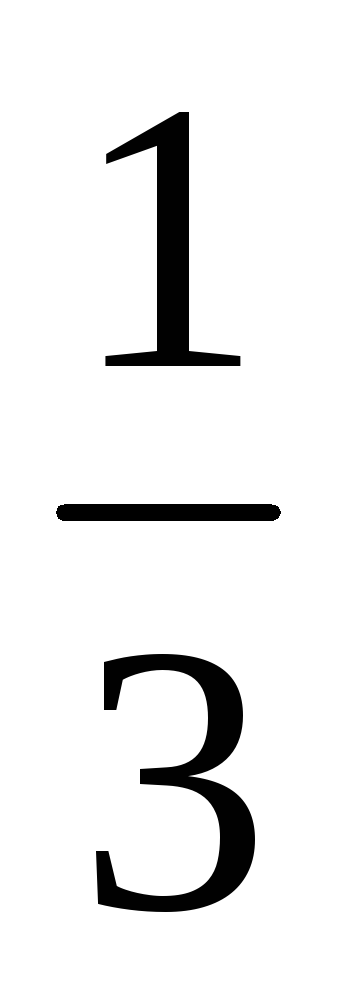
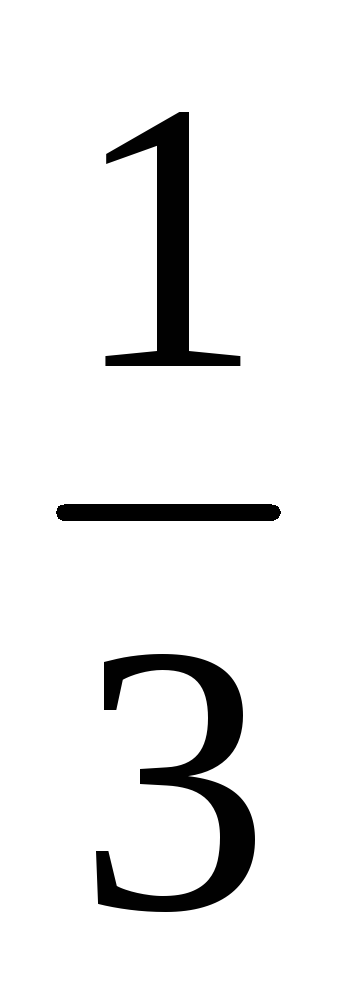
Hányszor változás sebessége közvetlen kémiai reakcióval előforduló a rendszerben: 3A (z) + V (r) = 2C (t)
ha: a) mennyiségének növekedése akár ötször
b) egyre nagyobb a nyomás a felére
T. k. Minden anyagokat a gáz halmazállapotú, ezek szerepelnek koncentrációban képletű a tömeghatás törvénye.
Mi írjuk a expresszióját a törvény ebben a reakcióban: 1 = k [A] 3 [B]
a) a mennyiségi növekedés (vagy csökkenő nyomásnál) az N-edik szám, ahányszor a koncentrációja a reagáló gáz halmazállapotú anyagok csökkentette az azonos idő alatt, t. e. a növekvő térfogat ötszörösét koncentrációja az A és B csökken öt alkalommal. Ezért 2 = k [
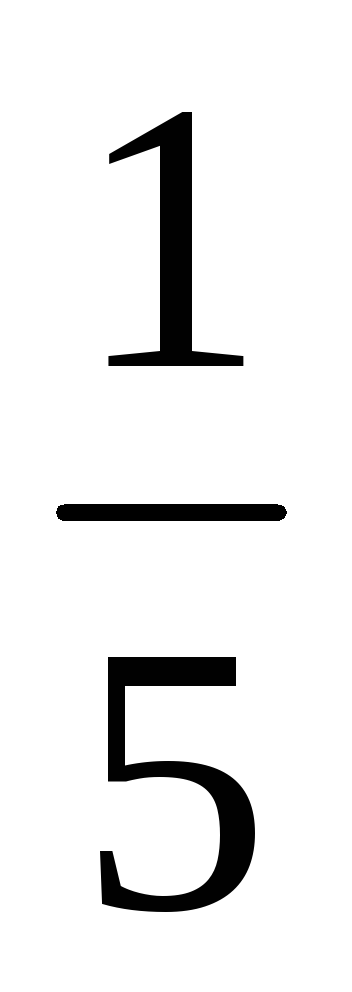
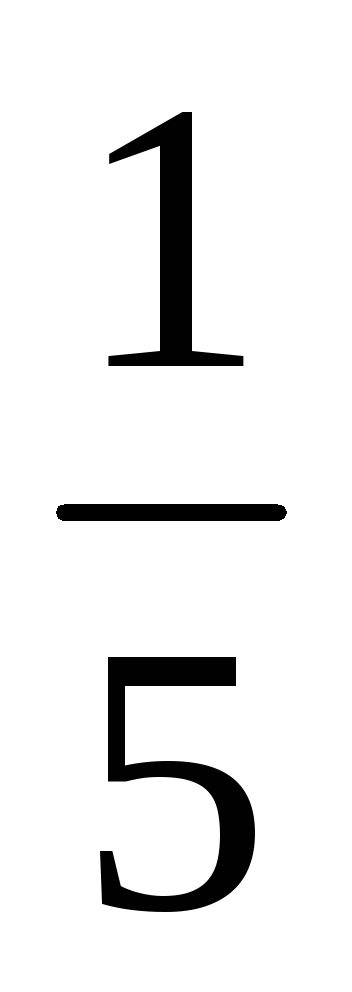
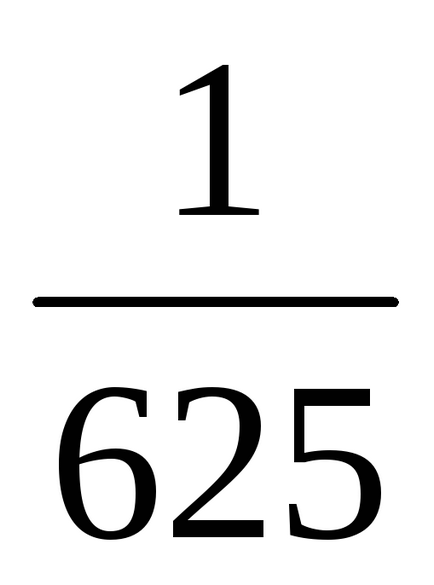
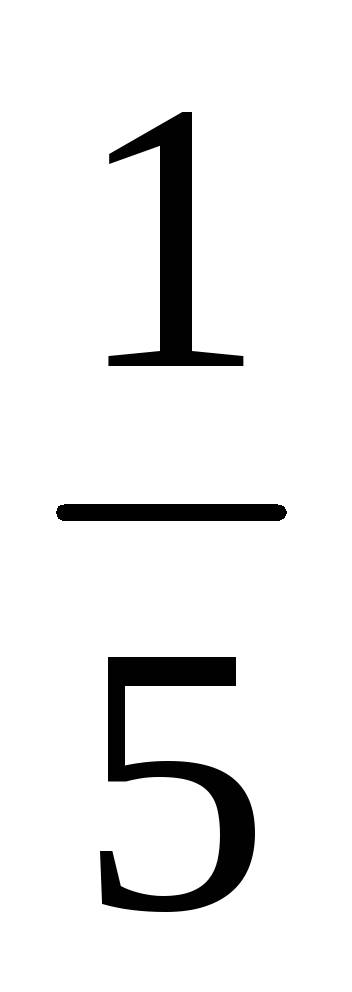
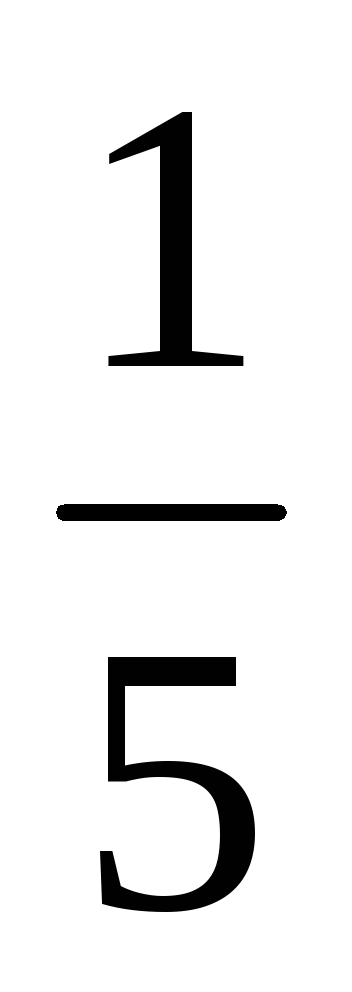
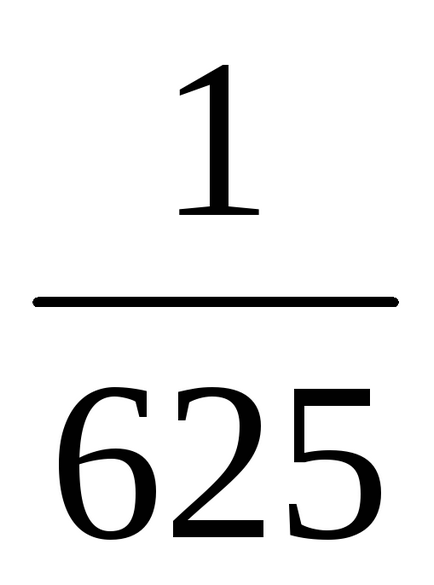
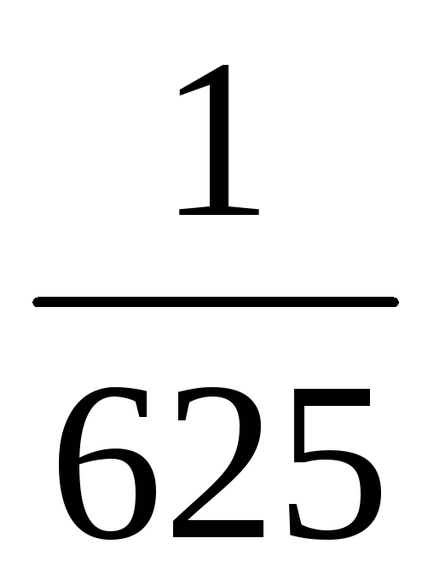
b) Amikor a nyomás növelésével (vagy csökkentésével térfogat) az N-edik számú alkalommal a koncentrációja a reagáló gáz halmazállapotú anyagok megnövekedett az azonos idő alatt, t. e., ha a nyomás növekszik kétszerese koncentrációja az A és B megduplázódott. Ezért 2 = k [2A] 3 [2B] = 16k [A] 3 [B]. Így 2 / 1 = = 16k [A] 3 [B] / K [A] 3 [B] = 16. Következésképpen a közvetlen reakció sebessége növekedni fog 16 alkalommal.
Hogyan lesz a mennyiségének csökkentéséhez négyszer a sebesség a következő reakciók:
a) Mivel ebben a rendszerben egyik anyag (C) van a kristályos állapotban, annak koncentrációja nem szerepel a képletben a tömeghatás törvénye. Következésképpen 1 = k [O 2]. Amikor térfogatának csökkentésével négyszer az O2 koncentráció négyszeresére nőtt, hogy 2 = k [4O2] = 4 K [O 2]. Ezért 2 / 1 = = 4k [O2] ./ k [O 2]. = 4, és a határidős reakció sebességét növeli 4-szer.
b) Mert között a kiindulási anyagok, csak egy anyag, és a kristályos állapotban, a hangerő változás nem érinti az arány az előre reakció és ez nem változik. __________________________________________________________________________
TIP: Vegye figyelembe, hogy az a tény, bármely halmazállapotban olyan anyag a reakcióban, és emlékezni, hogy az anyagok koncentrációjának a kristályos állapotban nem tartalmazza.