Egy ideális gáz nem erői intermolekuláris kölcsönhatás és a belső energia az összege
A törvény az egységes energia-eloszlás a szabadsági fok: az energia egy anyajegy-ku-ly egyenletesen elosztva a ste-ne-yum szabadságát, azaz a minden ste-csonkja szabadságát, függetlenül a szerkezet con-TION molekulában azonos az energia, ravnayakT / 2.
Clausius
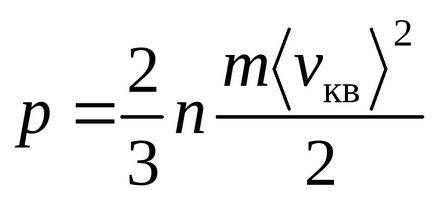
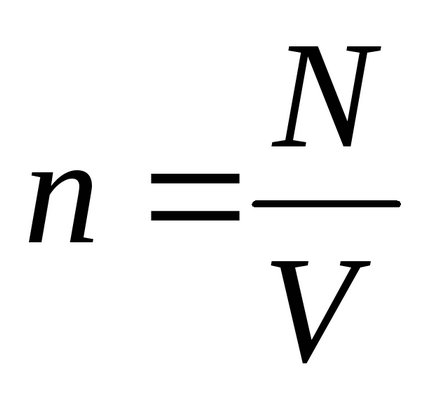

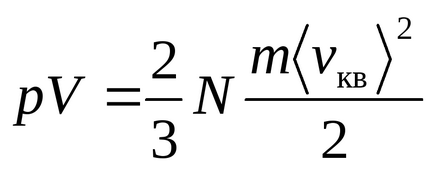
Egyenlet Mengyelejev - Clapeyron
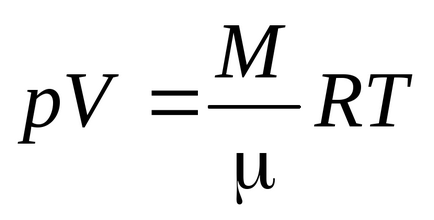

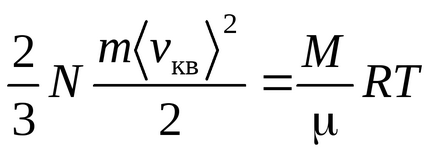

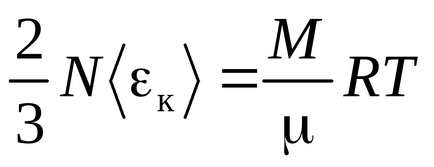

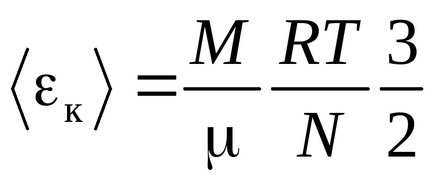
Clausius egyenletet kapjuk az a feltételezés, hogy a gázmolekulák - lényeges pontokon (egyatomos molekulák), amely három szabadsági fok a transzlációs mozgást. Mivel minden megközelítés egyformán valószínű, az összes energia a molekula egyenlően osztják el a három szabadsági fok és minden fokú szabadságot kT / 2 energia
Az energia egyetlen molekula:
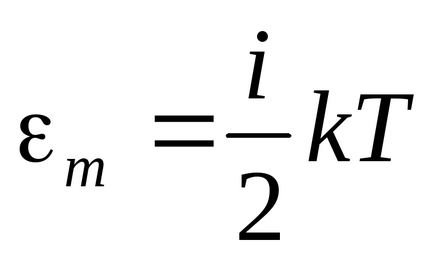
Az energia egy kilomole :.
Az energia egy tetszőleges gáztömeget
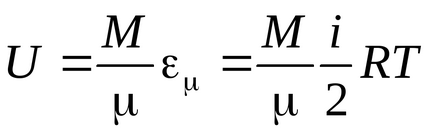
3. Munka és hő. Hő, a faj.
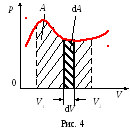
Elementary munkát. a gáz által végzett, amikor a dugattyú elmozdul, hogy a szegmens dh,
Végzett munkát a gáz végső térfogat változás V1 V2,
Ha dV> 0, dA> 0: a rendszer nem működik, a külső szervek - ad nekik az energia.
Ha dV <0, то dA <0: внешние тела совершают над системой работу – система получает энергию извне.
Grafikusan, a művelet ábrázolt p és v koordinátáit (folyamatábra) által határolt területen a görbe p = f (V) és két ordinátán megfelelő Chal-de-edik V1 és V2 végső térfogatot.
A hővezető energia (hő) kíséri változások a testhőmérséklet. Jellemzi az on-the-figura-tic szervezetek képesek felmelegíti a hőség miatt kívülről érkező kerül bevezette a fajhő.
TeploemkostS- skalár fizikai mennyiség, a Jellemzők-rizuyu-schaya közötti kapcsolat juttatott hő mennyisége a rendszer és a változás a hőmérséklet.
típusú hőkapacitás
Teljes teploemkostSpol számszerűen egyenlő a hőmennyiség amelyet át kell vinni, hogy a rendszerhez annak érdekében, hogy növelje a hőmérsékletet egy fokkal
Moláris teploemkostS számszerűen egyenlő a hőmennyiség kell jelenteni egy kmol érdemben növeli annak hőmérsékletét egy fokkal:
Fajlagos hő kapacitás (C) számszerűen egyenlő a hő mennyiségét kell jelenteni, hogy az egység tömegének anyag növeli annak hőmérsékletét egy fokkal:
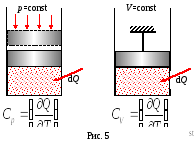
Jellegétől függően a folyamat különböztethető hő állandó térfogaton CV és állandó davleniiSr.
Fizikai munka a bővítés smyslR- 1 mol ideális gáz izobár folyamat melegítéssel 1 TO