Erők molekulák svyazyvayuschieatomy
Mi erők ténylegesen tartsa a tartalmaznak a molekulában egymás mellett, ha a molekulák bomlanak semleges atomok a gázt kell hevíteni körülbelül 4000 K? Mik a főbb problémákkal állunk szemben, amikor megpróbálja megtalálni a választ erre a kérdésre, amely gerjeszti vegyészek az egész világon a mai napig?
Vegyük ezeket a kérdéseket részletesebben. Alapján megfogalmazott kapcsolati ábrázolásai atomi szerkezetének is rendkívül egyszerű modellt javasolt hidrogén molekula - két proton (egy-egy minden mag) és két elektron (1. ábra).
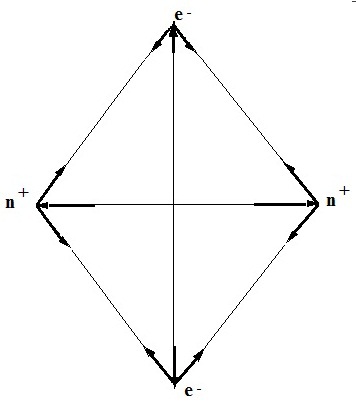
1. ábra Egy egyszerű modell a hidrogén molekula
Ennek megfelelően a modell, a pozitív töltésű atommag vonzza az elektronokat a cselekvés terén, a két mag. Egyszerre működik, és taszító erő között, mint a töltött részecskék. A kísérletekből ismert, hogy a kialakulását bármilyen kommunikációs jelentkezik az energia kiadás. Így, ha a kapcsolat van kialakítva, ebből következik, hogy az erő a vonzás a molekulában felett kell állnia az erők a taszítás.
Azonban, végzett számítások alapján kísérleti paraméterek meghatározása, mint az ionizációs potenciál, elektron-affinitása (energia szabadul fel, amikor egy elektron csatlakozott a semleges atom), a hossza (központjai közötti távolság a kölcsönható atomok), éles ellentétben ezzel az egyszerű rendszer. Mivel a affinitása az elektron a hidrogénatom (FE) egyenlő 72 kJ / mól, az energia, hogy legyőzzük az erőket a vonzás az elektronok nem haladhatja meg a 2SE atommagok, azaz 144 kJ / mól. Azonban annak érdekében, hogy elbontja a hidrogén-molekula, szükséges, hogy fordítsuk az energia egyenlő 432 kJ / mól. Ezek az eltérések között kiszámítása és a kísérlet valójában még nagyobb, ha figyelembe vesszük az erők közötti taszítás a magok.
Méréseiből az Kovalenciasugár ismert, hogy a távolság a két mag a hidrogén molekula 0,068 nm. Mivel ez a távolság sejtmagok taszító (Coulomb kölcsönhatás) összege 1877 kJ / mól. A formáció a hidrogén molekula szükséges hogy ezek az erők a taszítást. Összhangban a viriáltétel, a töréséhez szükséges energia a hidrogén molekula legyen felével egyenlő a potenciális energia, azaz a 1877: 2 ≈ 939 kJ / mól. Így, a formáció a hidrogén molekulák energia nyereség lesz 939 + 432 = 1371 kJ / mol, míg a modell (lásd. 1. ábra), ebből következik, hogy a maximális energia nyereség egyenlő 144 kJ / mól, mely csak 10,5% kísérletesen talált. Így, arra lehet következtetni, hogy ez a modell egy kémiai kötés a hidrogén molekula nem alakítható. Ismét nem kaptunk választ arra a kérdésre: Mi erők tartsa tartalmaznak a molekulában?
Súlyos ellentmondások merülnek fel, amikor megpróbálja megtalálni a választ a következő kérdésre: Milyen a megfelelő teljesítmény megzavarják a kommunikáció, át a molekula?
Mint már említettük, a kémiai kötés disszociációs energia kell jelenteni, hogy a rendszer. Feltételezve, hogy a kötési energia összemérhető az energia az elektronok, azt kell várni, változások az energia, mint amikor a molekula és a pusztulástól. Még egy ilyen egyszerű magyarázat ellentmond a kísérleti adatokkal.
Kísérletileg találtak a kötési energiája hidrogén molekula egyenlő 432 kJ / mól. Ezért, ha megszakad, azaz ha mennyiségben energiaráfordítást, az energia a elektronok az atomok kell emelkednie 432 kJ / mól. Azonban, összhangban a spektrális adatokat az atomok, elektronok képesek elnyelni csak egy részét energia 1000 kJ / mól (
166. 10 -23 kJ / elektron). Ezen kívül néhány tapasztalati tények, nem csak nem kap magyarázatot keretében az elektrosztatikus modell, hanem hogy vele éles ellentétben. Például egy kémiai kötés általában kialakítva két elektront. Ha az elektronokat igazán egyesültek, akkor miért mindig 2 (nem 1 és 3)? Továbbá, az elektrosztatikus jellemzőit összes atom (PPI, elektronegativitási, elektron-affinitása) növeli időszakban balról jobbra (azaz, az első csoport a periódusos rendszer), míg a függését az energia a M-M (ahol M - bármely tagja) az első ionizációs potenciál kíséreletek ugyanabban az irányban egy maximumon megy keresztül. A maximális érték a parabola csúcsa, jellemzően esik a középső időszakban. Ugyanakkor a kötés hossza a időt csökkentette.
A kérdés, hogy a természet a kémiai kötés továbbra is nyitott nem csak abból a szempontból a kémia, hanem a szempontból a fizika, valamint az a kérdés, hogy létezik egy harmadik erő.