Malyugina találhatóak
Malyugina OV Előadás 3. felépítése a periódusos rendszer DI Mengyelejev. Időszakokban.
Rövid-időszak periódusos rendszer kiviteli alakja áll időszakok, sorozat, csoportok, és alcsoportok.
Hosszú sorokban opció nincs megadva.
Időszak - vízszintes sorban a periódusos rendszer a kémiai elemek, helyezni a növekvő sorrendben az atommag töltés, amely kezdődik egy alkálifém (Li, Na, K. Rb, Cs, Fr) és végződik egy inert gáz (He, Ne, Ar, Kr, Xe, Rn ).
Kivételek: egy első időszak, amely kezdődik hidrogénnel (nemfémes).
A periódusos rendszer hét időszakok és 10 sor.
Időszakok vannak osztva kis és nagy.
Az első időszakban. tartalmaz 2 elem, valamint a második és a harmadik. 8 számozás elemek minden, az úgynevezett kis. Ezek közé tartozik egy vízszintes sor.
A fennmaradó időszakban, amely két vízszintes sorokban az egyes, az úgynevezett nagy.
A negyedik és ötödik időszakok 18 tartalmazzák a kémiai elemek az egyes. Az ötödik és hatodik időszakok - 32 kémiai elemek. Hetedik időszak tartalmazza az utolsó adatelem 32, amelyek közül sok a mesterségesen állítunk elő úgy nukleáris fúziós reakció.
Minden nagy időszakban, két sorozat.
A felső soraiban a hosszú ideig nevezik még. alsó sorok - páratlan. A páros sorok nagy időszakok csak a fémek.
A hatodik utáni időszakban lantán La (sorszáma Z = 57) 14 elemek (sorszáma Z = 58-71), amelyek hasonló tulajdonságokkal, hogy a lantán és a lantanidák nevezzük, ezek találhatók alján a periódusos rendszerben.
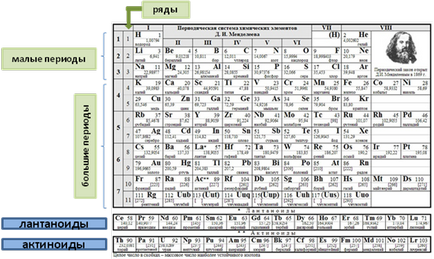
A befejezetlen hetedik időszak Ac utáni aktínium (sorszáma Z = 89) van 14 elemek (sorozatszámok Z = 90-103), amelyek hasonlóak a tulajdonságai, hogy tengeri rózsák, és az úgynevezett aktinidák. Ahogy lantanidák, ezek találhatók alján a periódusos rendszer (1. ábra)
1. ábra. Elhelyezkedés időszakok és sorozatok
a periódusos rendszer DI Mengyelejev
1. táblázat elemeinek száma az alábbi időszakokban:
Törvényszerűségek megfigyelt időszakban.
Minden periódus (kivéve az elsőt) indul egy tipikus fém (Li, Na, K, Rb, Cs, Fr) és végződik a nemesgáz (He, Ne, Ar, Kr, Xe, Rn), amely előtt egy tipikus nemfémes (F, Cl, Br, I, At).
Az egyes időszakok, balról jobbra növeli a felelős az atommag, atomrádiusz csökken, van egy gyengülése fémes és nem fémes tulajdonságai amplifikáció, csillapítás és helyreállítás elemek amplifikációs oxidáló tulajdonságai és azok képezik az egyszerű és komplex vegyületek.
Kérdések samoprooverki
Mik a szerkezeti elemek a periódusos rendszer a kémiai elemek?
Mi az az időszak?
Hány időszakok és sorozatok a periódusos?
Hány elem minden időszakban?
Ami az időt nevezzük kicsi, és miért?
Hány sorozat kis ideig?
Ami az időt nevezzük nagy? Hány sorozat nagy korszak?
Milyen tulajdonságai vannak a szerkezetben VI, VII ideig?
Mik az elemei az elején minden időszakban?
Mik az elemei az egyes időszakok végét?
Mik az elemek a korábbi nemesgáz (semleges) gázok?
Hogyan változtassuk meg a tulajdonságait az elemek időszakok balról jobbra?
Időszakok, sorok, csoportok és alcsoportok.
Időszak - vízszintes sorban a periódusos rendszer a kémiai elemek, helyezni a növekvő sorrendben az atommag töltés, amely kezdődik egy alkálifém (Li, Na, K. Rb, Cs, Fr) és végződik egy inert gáz (He, Ne, Ar, Kr, Xe, Rn ).
7 időszakok és 10 sorok.
Lásd az 1. táblázatot.
Kis úgynevezett I, II és III időszakok tartalmaznak, illetve 2, 8, 8 kémiai elemek.
Kis ideig egy sorban. Lásd. 1. ábra.
Nagy úgynevezett IV, V, VI, VII időszakokban. Minden nagy időszakában 2 sor. Lásd. 1. ábra.
VI soderdit 14 elemek - lantanidák, VII időszakban tartalmaz 14 elemeket az aktinidák. A kényelem, ezek alján található az asztalra.
Minden periódus (kivéve az elsőt) kezdődik jellemző alkálifém (Li, Na, K, Rb, Cs, Fr)
Minden periódus véget ér nemesgáz (He, Ne, Ar, Kr, Xe, Rn).
Megelőzik tipikus nemfémek - halogének (F, Cl, Br, I, At).
Az egyes időszakok, balra, van egy gyengülése fémes és nem fémes tulajdonságai amplifikáció, csillapítás és helyreállítás elemek amplifikációs oxidáló tulajdonságokkal és azok képezik az egyszerű és komplex vegyületek.
Feladatok az önálló döntési
Egy olyan időszakban, és számos, az elemek atomszáma 14, 48, 52, 56, 78? Adja jellegét, az orosz nevét, relatív atomtömeg.
Írja karakterek, nevek és relatív atomtömeg páratlan számú eleme IV időszakban.
Melyik elem kifejezettebb fémes tulajdonságai kalcium- vagy kálium-? Miért?
Melyik elem kifejezettebb fémes tulajdonságai foszfor- vagy klórt? Miért?
Melyik elem a negyedik periódus a legaktívabb nemfém? Miért?
Melyik elem ötödik időszak legaktívabb metal? Miért?
3. Kálium. Meg kell nézni a helyzetét elemek PSKHE. Kálium (K) és a kalcium (Ca) ugyanabban a (negyedik) időszakban. Abban az időszakban, balról jobbra meggyengülnek fémes tulajdonságokat.
4. A klór. Meg kell nézni a helyzetét elemek PSKHE. Foszfor (P) és a klór (Cl) ugyanabban a (harmadik) időszakban. Abban az időszakban, balról jobbra amplifikált nemfémes tulajdonságokkal.
5.Samy aktív nemfémes ebben az időszakban - bróm. Abban az időszakban, balról jobbra amplifikált nemfémes tulajdonságokkal. A közömbös elemének kripton nem mutat kémiai reaktivitást, előzi meg a leginkább aktív nem-fém.
6. A legaktívabb fém, amely időszakban - rubídium. Aktív időszakban kezdődik egy alkálifém (Li, Na, K. Rb, Cs, Fr), mozgó balról jobbra fémes tulajdonságokat gyengült a időszakban.
Malyugina OV előadás szerkezete a periódusos rendszer Mendeleev. időszakok
Előadás №1. Meghatározása az operációs rendszer, a történelem, a fejlődés és a funkciót. (2 óra).
Természetes foszforvegyületet és megszerzése
Áttekintés szintézis kémia leckét Referencia: Jelentés periodikus törvény a periódusos rendszer, és
Módszertani útmutató a laboratóriumi munka „A szerkezet és elvei a szervezet a fájlrendszer ext2» fegyelem
Slavneft Jaroszlavl finomító őket. Mengyelejev
Esszé tűnt érdekes, mert az oxigén, mint bármely más elem a periódusos rendszer, fontos a számunkra. Oxigén nélkül az élet a Földön nem lenne lehetséges. Oxigén - a leggyakoribb kémiai elem a
Hozzávetőleges szerkezet vizsgált hitel - 2. modul