Biológiai oxidáció - studopediya
Amikor a biológiai oxidáció, a szerves molekulák a megfelelő enzim által hasított két hidrogénatom. Egyes esetekben, míg között az enzim és az oxidált molekula képződik instabil, energiában gazdag (makroenergeticheskaya) kötés. Ezt alkalmazzák az ATP - a „végső cél” a legtöbb folyamat a biológiai oxidáció. A két hidrogénatom veszik el, mint egy reakció eredményeként kapcsolódó koenzim NAD (nikotinamid-adenin-dinukleotid), vagy NADPH (nikotinamid-adenin-dinukleotid-foszfát).
Az ezt követő sorsa hidrogénatom eltérő lehet. A anaerob oxidációt, akkor azt átvisszük valamilyen szerves molekulák. A aerob oxidációja hidrogén-át a oxigénből víz képződik. A fő része a hidrogén-transzfer áramkör található, a membránok a mitokondriumok. Így a ADP és szervetlen foszfát mennyiségét ATP.
Meg kell jegyezni, hogy az aerob oxidáció sokkal hatékonyabb anaerob. Az első esetben a 1 glükóz molekula előállított 2 molekula ATP és a második - 36, ahol a glükóz „égett”, hogy a CO2 és víz. Ez magyarázza a széles körben elterjedt és erőteljes fejlődése aerob szervezetek.
A fő energiaforrás a sejt - az oxidációs szubsztrátok légköri oxigénnel. Ezt a folyamatot végezzük három módon: oxigén hozzáadása a szén-lehasításával hidrogénatom vagy veszteség egy elektron. A sejteket az oxidáció végbemegy formájában egymást követő szállítási hidrogén és elektronok a szubsztrát az oxigénre. Oxigén szerepet játszik ebben az esetben egy redukáló vegyület (oxidálószer). Az oxidációs reakciókat okoznak energia felszabadulással jár. A biológiai reakciók jellemzője a viszonylag kis változás energiát. Ezt úgy érjük el, zúzás az oxidációs folyamat egy több közbenső szakaszaiban, amely lehetővé teszi harisnya kis részletekben formájában energiában gazdag vegyületek (ATP). Recovery a oxigénatom reagáltatva egy pár protonok és elektronok képződéséhez vezet egy vízmolekula.
Szöveti légzést. Ez egy olyan folyamat, oxigén fogyasztása sejtek a test szöveteiben, amely részt vesz a biológiai oxidáció. Ez a fajta oxidáció hívják aerob oxidáció. Ha nem a végleges akceptor oxigént működik, mint egy hidrogén-transzfer áramkört, és egyéb anyagok (például piroszőlősavat), egy ilyen típus az úgynevezett anaerob oxidáció.
így biológiai oxidáció - egy dehidrogénezési szubsztrát alkalmazásával köztes vektorok hidrogén és a végső akceptor.
Légzőszervi Chain (légzőszervi enzimek szövet) - a proton és elektron-hordozóként az oxidálható szubsztrát oxigént. Az oxidálószer - egy vegyület, amely képes elfogadni elektronokat. Ez a képesség, mennyiségileg az oxidációs-redukciós potenciál viszonyítva a standard hidrogén elektród, a pH egyenlő 7,0. Minél alacsonyabb a potenciálja a vegyület, annál erősebb a redukáló tulajdonságai, és fordítva.
Így. bármilyen vegyület lehet adományozni elektronok csak egy vegyület egy nagyobb redox potenciál. Minden ezt követő légzési láncszem van egy nagyobb potenciállal rendelkezik, mint az előzőt.
A légzési lánc áll:
1 NAD - függő dehidrogenáz;
2 FAD- függő dehidrogenáz;
3 ubikinon (KoQ);
4 Tsitohrmov b, c, a + a3.
NAD-függő dehidrogenáz. Mivel a koenzim például a NAD és NADP. A nikotinamid piridingyűrű kapcsolni képes a hidrogén-protonok és elektronok.
FAD és FMN-függő dehidrogenáz koenzim tartalmazzák, mint a foszfor-észter-vitamin B2 (FAD).
Ubikinon (KoQ) hidrogénatom megfosztja flavoproteinek és alakítjuk hidrokinon.
Citokróm-- chromoproteids fehérjék kapcsolni képes elektronok jelenléte miatt az összetételét, mint prosztetikus csoportok ferroprotoporphyrin. Vesznek egy elektront egy anyag, ami egy kicsit a Bole erős redukálószer, és adja át a erősebb oxidálószer. Vas atom kapcsolódik a nitrogénatomhoz az imidazolgyűrű a hisztidin aminosav-maradékot ugyanazon az oldalon a porfirin a gyűrű síkjával, és másrészt a kénatommal metionin. Ezért a potenciális képességét, a vas atom a citokrómok oxigénkötő elnyomott.
A citokróm c sík porfirin kovalensen kötött fehérje keresztül két cisztein csoport, és a citokrómok b és egy. ez nem kovalens svyazanos fehérje.
A citokróm-A3 + (citokróm-oxidáz) helyett tartalmazhatnak porfirin protoporfirin Egy eltérő számos szerkezeti jellemzők. Ötödik koordináció által elfoglalt amino vas tartozó aminocukor maradékot alkotó fehérje is.
Ellentétben gemolgobina hem vas atom a citokrómok is reverzibilisen átmenet két vegyértékű állapotba, ez biztosítja a közlekedési elektronok.
A mechanizmus a elektrontranszfer lánc. Mitokondriális külső membrán átjárható a legtöbb kis molekulákat és ionokat, a belső szinte minden ionok (kivéve a protonok H) a legtöbb töltetlen molekulák.
A folyamatok oxidáció és ATP képződése származó ADP-t és a foszforsav, azaz foszforiláció előfordulnak a mitokondriumok belső membránjában - Kristen. Ez a molekula tartalmazza a három nagy energiájú kötések. Macroergic vagy nevezzük energiában gazdag kötés, amely megjelent nyúlás nagyobb, mint 4 kcal / mol. Amikor a hidrolitikus hasítása ATP ADP-t és a felszabadított foszfát 7,3 kcal / mol. Pontosan ugyanez költenek a ATP képződése ADP és foszforsav maradék, és az egyik legfontosabb eszköze az energia tárolására a szervezetben.
A szállítás során a légzési lánc elektron energia szabadul fel, amely fordított összekötő foszforsav maradék, hogy ADP alkotnak egy molekula ATP-t és egy molekula víz. Az átvitel során a egy pár elektronok a légzési lánc felszabadul, és tárolják a formájában három molekula ATP 21,3 kcal / mol. Ez megközelítőleg 40% -át a felszabaduló energiát elektron transzport.
Ez a módszer az energiatárolás a sejtben az oxidatív foszforiláció vagy kettős foszforiláció.
Az arány az oxidatív foszforiláció elsősorban attól függ, az ATP-tartalom, annál gyorsabban fogy, annál felhalmozott ADP, annál nagyobb szükség van az energia, és ezért megy aktív folyamata oxidatív foszforiláció. Fordulatszám szabályozás oxidatív foszforiláció ADP koncentráció a sejtben az úgynevezett légzési kontroll.
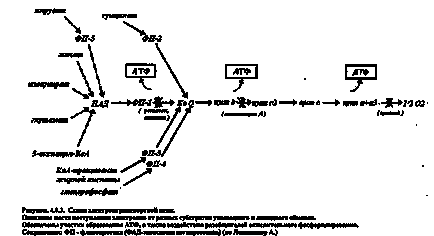
Ábra 27-légúti kontroll