A kémiai összetétele sejtek
A kémiai összetétele fehérjék.
Származó sejteket szerves anyagok az első helyen a száma és értéke fehérjék. A készítmény összes fehérje hidrogénatom, oxigén, nitrogén. Számos proteint tartalmaz, amellett, kénatomot. Vannak fehérjék, amelyek szintén tartalmaznak fématomok - vas, cink, réz.
Eltérően más szerves vegyületek, fehérjék számos funkcióval. Először az összes fehérje jellemzi egy hatalmas molekulatömegű. Összehasonlítás: molekulasúlyú alkoholban - 46 ecetsav - 60 benzol - 78, és albumin (egy fehérje a tojás) - 36 000 hemoglobin (a fehérje a vörösvértestek) - 152 000 miozin (egyik izomfehérjék) - 500 000. egyértelmű, hogy, szemben a molekula alkohol, ecetsav, benzol, valamint más fehérje molekulák óriás. Az építés során magában ezer tartalmaz. Hangsúlyozni a gigantikus méretű ezeket a molekulákat nevezik makromolekulák (a görög „makro”. - nagy, óriás).
A fehérjék szerkezete.
Közül a szerves vegyületek legösszetettebb fehérjék. Utalnak arra vegyületek úgynevezett polimerek. polimer molekula egy hosszú láncú, ami ismétlődik többször, azonos viszonylag egyszerű szerkezet az úgynevezett monomer. Jelölő az A monomer, a polimer szerkezet a következőképpen ábrázolható: A-A-A-A-A.
Emellett a fehérjék a természetben sok más polimerek, mint például cellulóz, keményítő, gumi. A vegyiparban teremtett számos mesterséges polimerek, - a polietilén, poliészter, nylon és mások.
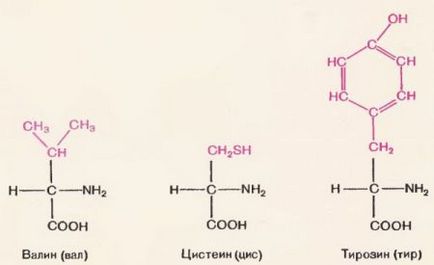
A legtöbb természetes és szintetikus polimereket készítünk azonos monomerek. Fehérjék is állhat hasonló, de nem egészen azonos monomerek. Monomerek fehérjék aminosavak. Mint látható a 70. ábrán, az aminosav-molekula, mivel két részből áll. Az egyik rész (fekete betűkkel) minden azonos aminosavakat.
Ez a csoportosítás. Ez áll egy aminocsoport (-NH2) és a közelében található a karboxilcsoport (-COOH). A másik része a molekula valamennyi aminosav különbözik (ez nyomtatott piros betűkkel). Ez a rész az úgynevezett radikális.
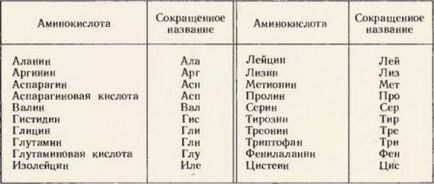
Sok különböző aminosavak. De mint monomerek bármely természetes fehérje - állati, növényi, mikrobiális, virális - csak 20 aminosavat ismert. Ezek az úgynevezett „mágikus”. A lista mutatja a táblázat.
Az a tény, hogy a fehérjék minden szervezet épülnek az azonos aminosavak - újabb bizonyíték az egység az élővilág a Földön.
Húsz aminosavak alkotják a természetes proteinek ( „mágikus” aminosav)
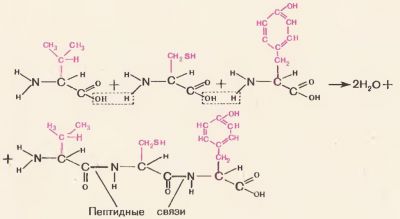
Vegyület aminosavak képződését egy fehérje molekula révén hajtják végre, a közös csoport minden aminosavat. Ahhoz, hogy megértsük ezt jobban, úgy 71. ábra: a karboxilcsoportja egy aminosav, és az aminocsoport a szomszédos aminosav osztja a vízmolekula és így felszabadult vegyértéket aminosavcsoportokat csatlakozott. van egy erős kovalens kötés az úgynevezett peptid-kötés aminosavak között. Az így kapott vegyületet az aminosavak nevezett peptidek. A peptid két aminosav az úgynevezett egy dipeptid, három aminosav - egy tripeptid, a számos aminosav - polipeptid. Minden proteinek polipeptidek t. E. A lánc sok tíz vagy akár több száz aminosav-egységet.
Minden élő szervezet nagy számban tartalmaz különböző fehérjék. Ebben az esetben, minden típusú sajátosságaival sajátos csak az ilyen típusú fehérje. Még fehérjék működnek különböző állatfajokban az azonos funkciójú, egymástól eltérő. Például, az összes gerincesek - halak, kétéltűek, madarak, emlősök - vörösvértestek hemoglobint tartalmaznak, egy fehérje, amely végrehajtja az összes állat ugyanazt a funkciót - oxigén szállítás. De hemoglobin mindegyik állatfajoknak, speciális szerkezete és tulajdonságai különböznek a többi állat hemoglobin.
Annak érdekében, hogy megmagyarázza a lehetőségét, hogy egy hatalmas különféle fehérjék, meg kell vizsgálni, hogy a fehérjék különböznek az aminosav-összetétel szerint a számú aminosav-egységek, annak érdekében, hogy kövesse a lánc. A számos strukturális változatok születik ebben a csillagászati számok. A jelentés az indiai tudós Singh biokémiai kongresszus Moszkvában a következő érdekes számítást kapott. Egy fehérje, amelynek molekulatömege körülbelül 34.000 tartalmaz 300 aminosav-egységet (a molekulatömege egy aminosav egységet átlagosan 110). Legyen egy része a fehérje nem tartalmazza az összes, a 20 aminosav, de csak a 12. Ilyen körülmények között, a számos lehetséges izomerek a fehérje egyenlő 10 300. Annak érdekében, hogy érzékelje a nagysága ez a szám, elképzelni egy pénzérmét 10.300. Egy ilyen halom érme súlya 10300 g (egy pénzérmét súlyú 1 g). A tömeg a világon október 27 g!
Tekintettel arra, hogy a méret egy aminosav egység 0,35-0,37 nm, nyilvánvaló, hogy a fehérje makromolekula áll, hogy a több száz aminosavból, volna, hogy hossza néhányszor tíz nanométer. Tény, hogy a mérete fehérjemolekulák sokkal kisebb. Néhány közülük a gyöngyök alakjában, amelynek átmérője 5-7 nm. A polipeptidláncát fehérje valahogy hullámos, egyszer lefektetett. Mindegyik fehérje természetéből adódó egy jól definiált stílus. A teljes leírása a szerkezet a fehérje molekula ismereteket igényel az elsődleges, másodlagos és harmadlagos szerkezet.
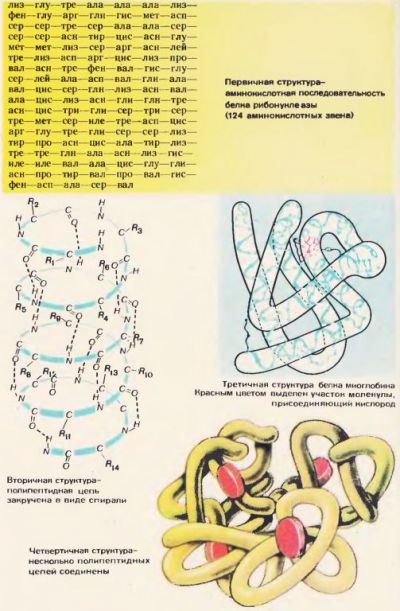
A szekvencia aminosav a fehérje molekula meghatározzák az elsődleges szerkezete. Ez olyan, mint egy fehérje formula. A 72. ábra a primer szerkezetét a fehérje ribonukleáz. A szerkezet a fehérje tartalmaz 124 aminosav szinten. A legtöbb esetben, a polipeptid-lánc teljesen vagy részben csavart egy spirál. Ez a másodlagos szerkezet a fehérje. Az aminosav gyökök tehát kívül hélix. Spirál menetek vannak elrendezve szorosan. Között az NH-csoport van az egyik tekercs, és a CO-csoportok a szomszédos tekercsek, hidrogén-kötések alakulnak ki (72. ábra). A hidrogénkötések sokkal gyengébb, mint a kovalens, de sokszor megismételt, adnak egy erős kötés. Polipeptid spirál „varrott” számos hidrogénkötések elegendően erős szerkezet.
Polipeptid spirál további felhalmozás. Letekerte furcsa, de az egyes fehérjék meglehetősen határozottan és véglegesen. Az eredmény egy konfiguráció úgynevezett harmadlagos szerkezetet. Harmadlagos szerkezetét a támogatási hidrofób kötések között előforduló hidrofób aminosav gyökök. Ezek a kapcsolatok gyengébbek, mint a hidrogén. A vizes közegben a sejtben hidrofób gyökök taszítja a vizet, és egymáshoz tapadnak. Így, a vizes közeg arra kényszeríti a fehérjemolekula, hogy fogadjon el egy adott rendezett struktúra, és ez lesz biológiailag aktív.
A harmadlagos szerkezet nem a legmagasabb formájában strukturális szerveződése a fehérje. Egy élő sejt azt találtuk sok más, bonyolultabb formák is, például kvaterner (72. ábra).