Arany vízben - Vegyi referencia 21
Szerint Svedberg, diffúziós együtthatója kolloid arany részecskék vízben 298 K 2,7 és 10 m / nap. A variancia-N0S1T, részecskék arany hydrosol. iri víz Viszkozitás 298 K RGVIA 8,94-10-3 Pa-S. [C.106]
Ábra. 3. példa függően rögzítési energia a spektrum analizátor a frekvencia evett> a kolloid részecskék (100 A átmérő) arany vízben szórási szög 6 = 40 °, 2r = 293 Hz pont - a számítás a (6) képletű.
Mindhárom fémek kémiailag inaktívak, a aktivitás csökken a réz arany. Van egy olyan tendencia, fémionok egy viszonylag könnyű visszanyerésének a fémes állapotban. Minél alacsonyabb az oxidáció mértékét a réz nem stabilak, és mutatnak erős hajlama, hogy oxidálódik, hogy nagyobb (4-1-> 2). Mindhárom fémek mutatnak diamágneses tulajdonságokat. A legtöbb vegyület festettek minden fém képződése jellemzi a komplex vegyületek a sav anionja. ammónia, aminok és m. o. réz-oxidok. Ezüst és arany nehezen oldódnak vízben és gyengén bázikus jellegű. [C.203]
A vízben való oldhatóság, az összes anyagokat három csoportra osztjuk 1) jól oldódnak. 2) mérsékelten oldódik, és 3) gyakorlatilag oldhatatlan. Az elmúlt néven oldódó anyagok. Azonban meg kell jegyezni, hogy egyáltalán nem oldódó anyagok. Elhagyva a vízüveg rúd vagy egy darab arany vagy ezüst, ezek nagyon kis mennyiségben psec azonos oldódnak vízben. Köztudott, hogy a megoldás az ezüst vagy arany vízben megöli a baktériumokat. [C.116]
Egy példa a kivételes stabilitást lehet gyakran nevezik a piros arany kolloid vízben, kicsapva több hónapig vagy akár éves tárolás normál körülmények között. Ebben az esetben a stabilitás nem következménye a helyzet. ahol a felfelé irányuló sebessége a Brown-diffúziós [c.271]
Egy példa a tipikus szol kolloid arany szolgálhat oldatok vízben, amelynek az előállítását az alábbiakban ismertetjük. Ezekben a szolok, arany töredezett le a legkisebb részecskék több ezer vagy akár több száz aranyat tartalmaznak, és amelyekben a kristályos szerkezetű. [C.12]
Ez lehetséges a kolloid oldatokat csak azokra a hatóanyagokra, amelyek nem alkotnak valódi oldatot a kiválasztott oldószerben, azaz. E. Lehet készíteni csak vizes kolloid oldatok oldhatatlan anyagok ott. Például, az arany nem oldódik vízben. de ez könnyen lehet készíteni a kolloid vizes oldat világos cseresznye, lila vagy kék. NgZYuz kovasav, hidratált vas-oxid Fe (OH) s vízben oldhatatlanok. de képezhet, jellegzetes vizes kolloid oldatokat. [C.183]
Praktikus információk a kolloidok szerepelnek az Aristoteles és alkimisták. A Proceedings M. V. Lomonosova (1751) azt mutatja, egyértelmű különbség a jelenségek a kristályosítás és a véralvadási, előállítását ismerteti arany szol vízben és az üveg (színes üveg). [C.193]
Kolloid liquophobic rendszer neve, ha a részecske nem lép közvetlenül kölcsönhatásba az azokat körülvevő oldószer, mint például a kolloid oldatokat a fémek (arany vízben és R. N.). Lio-philous kolloid oldatokat mutatnak kémiai kölcsönhatás a kolloid részecskék a környező oldószerrel. Az ilyen kolloid oldatok vizes oldatok zselatin, keményítő és így tovább. N. Ha az oldószer víz. oly módon, hogy a kolloid oldatok nevezzük hidroszolok vagy hidrogélek. [C.148]
Egyenletek (XIII.2.1) és (XIII.2.2) alapján kiszámítható a magasságban részecskekoncentráció változást egy előre meghatározott számú alkalommal. A számítások azt mutatják, hogy egy ilyen rendszer. mint a levegő, h magasság. amelyben az oxigén koncentrációját a felére csökken, 5 km. A magasság, amelynél a koncentráció csökkenés 10-szer, 100 km. Egy ilyen rendszer. például kolloid arany oldatot vízben részecskeméretű 1,86 nm, a részecskék koncentrációja a felére csökken a magassága 215 cm, és 10-szer magasságban 4300 cm. A durva arany szol szemcseméretű 186 nm (százszor nagyobb) magasságban 0 2 mikron koncentrációja a felére csökken, és csökken 10-szer magasságban 4 m. Ez azt jelenti, hogy szinte az összes arany részecskéket koncentrálni alján a hajó, és h magasságban = = 4 mikron lényegében tiszta diszperziós közegben. Egy ilyen rendszer lenne kinetikus instabil. A kolloid oldat a részecskeméret 1,86 mikron magas kinetikai stabilitása. [C.402]
Azt is megfigyelték, hogy a stabil szolok nem kapott Brediga módszerrel. figyelembe minden elővigyázatosságot, hogy biztosítsa a nagy tisztaságú fém huzal és a víz, 1 de ív kialakul, és ha a tartály készül kémiailag stabil anyagból. Például, azt figyeltük meg, hogy ha egy szol arany tisztított vízben, vezetőképesség meghatározás. ez instabil, és egy kék elszíneződése az elektrolit mellett képződéséhez vezet egy stabil arany szol piros. Nyilvánvaló, hogy stabilizálja az szolok igényel bizonyos mennyiségű elektrolit szennyeződéseket. Azok lehetnek sósav. A számát a előállításához szükséges aranyrészecskék egy adott méretű, aránya az arany koncentrációja. Ha az ív jön létre a vízben tartalmazó a szükséges mennyiségű elektrolit, a vezetőképessége a keletkező szol kisebb, mint a kiindulási oldatban. Ha arany kolloid elhelyezett erős elektromos mező. A részecskék felé a pozitív pólus. kimutatására negatív töltést. Ezek az eredmények alátámasztják az elméleti feltételezés [c.129]
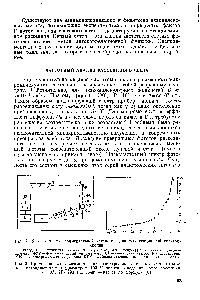
Ha a kolloid részecskék vannak kombinálva minden ütközés, a folyamat jellemzi bimolekuláris sebességi állandója a reakciót. egyenlő / d (A T / r1), amely 1,07-10 cm 1 részecske per 1-5,86 vízben vagy 10 cm-es levegő jelenlétében 20 X. táblázat. 5.1 ábra a koagulációs sebesség kolloid arany részecskék vízben találtak a Zsigmondy [53] és a Wigner és Tuorila [51]. Nyilvánvaló, az átlagos érték összhangban van az egyenlet (5.19) egészen egy tényezője nem haladja meg a 2, míg a kezdeti koncentráció a részecskék tartományban változhat a négy nagyságrenddel. Az arány a koagulációs a kolloid részecskék aeroszolok is összhangban van az egyenlet (5.19). A kísérleti értékek a tartományban 5 füstök kialakított 10 fém-oxidok, 8-10 füstök képződött gyanták és zsírsavak [50]. Ebben az esetben a Smoluchowski egyenlet végezzük. Továbbá, a hőmérséklet hatással van a véralvadási faktorok, valamint a obratnur) viszkozitása 1 / g] [6]. [C.107]
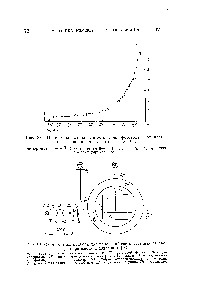
Ábra. 6.7. ellenállás közötti arány vekotorymi arany vegyületek vízben PRV 25 C-on és 1 atm davleviya. A készítményekben az oldott-klorid komponens 10 ° C, az oldott kén 10. Az árnyékolt dobozban stabilitását zolotoorganicheskih komplexek a természetes vizekben.