Alumínium korrózió - hasznos információk - Kiadó - én homlokzatok
Korróziója alumínium és ötvözetei
Alacsony sűrűségű és mechanikai szilárdsága együtt kielégítő korrózióval szembeni ellenállás nem alumínium vonzó szerkezeti anyag, amely széles körben használják az építőiparban. Mindazonáltal, a kémiai szempontból Alumínium - az egyik reakcióképes fémek, amelyek aktívan együttműködik nemcsak a savakkal és lúgokkal, hanem vízzel! A látszólagos ellentmondás magyarázata nagyon egyszerű: az oxigén (vagy más oxidálószerek) alumínium fém felület borítja szilárd, kémiailag stabil oxid film, amely megvédi a fémet a törés. Ezt a jelenséget nevezzük passziválás. Metal passzív abban az esetben, ha ez nem változhat, és akkor aktív, ha az agresszív szer elpusztítja kölcsönhatása potenciális korróziót.
Emlékezzünk, hogy a folyamat a pusztulás nevezik fémek korrózióját és fémötvözetek eredményeként a kémiai vagy elektrokémiai hatásának a környezetre.
Fém korrózióálló bizonyos körülmények között, lebontják a másik. Például az alumínium ellenáll a korróziónak a folyékony üzemanyag, és nem ellenálló a fellépés a nátrium-hidroxid (úgynevezett jelensége a passzív és aktív). Alumínium-oxid létrehoz egy kémiailag inert védőréteg, amelynek vastagsága 20-100Å. Az alumínium felületi tisztítja a védőfóliát reagálhat a vízzel, így hidrogént. Hatása alatt oxidáló az alumínium felülete van passzivált, így az oxigén lévő levegőben vagy vízben oldott, növeli a korrózióval szembeni ellenállás.
Korrózióállóságát alumínium nagymértékben függ a tartalmát szennyeződések egyéb fémek. Ismeretes, hogy érintkezés hatására a két fém merítjük egy elektrolit közegben, egy galvanikus pár képződik, ahol a több aktív fém válik az anód, és a kevésbé aktív - katód. Az anód elektrokémiai reakció megsemmisül. A szennyeződések legnagyobb része (kivéve a fémek aktívabb, mint az alumínium) szerepét a katód képest alumínium, azaz hozzájárulnak a pusztulástól. Emiatt, nagy tisztaságú alumínium van korróziós ellenállása nagyobb, mint a technikai fém, ami viszont, jobban ellenáll a korróziónak, mint az alumínium ötvözetek. Ezen túlmenően, korrózióállóság az alumínium függ környezet jellemzői és a reakciók által okozott közepes alumínium.
A mechanizmus a korrózió az alumínium
Jelenlétében oxidáló az alumínium felületét borítja védő réteg alumínium-oxid. A védőréteg viszont két rétegből áll:
Belső réteg Al2 O3. van, amelyet közvetlen reakcióját oxigén a fém. A belső oxidréteg szomszédos fém szilárdan alapozza, és annak szerkezetét és vastagsága függ az oxidációs hőmérséklet.
Kültéri reakciójával képződött a belső réteg a környezettel, elsősorban a víz. A ezen réteg vastagsága függ a bekövetkeztének időpontját korrózió és a koncentrációt a korrozív anyagok a környezetbe. Növelése a vastagsága a külső réteg az oxidáció következtében az alapfém. A külső réteg porózus, továbbítja a levegő és a nedvesség.
Ennek eredményeként a korróziós folyamatok az alumínium felületét a teljes vastagsága a védőréteg növekszik, de a vastagsága a belső réteg ily módon állandó marad.
korrózió típusai
fémek korrózióját osztható kémiai és elektrokémiai.
Elektrokémiai korrózió lép fel az intézkedés alapján a fém elektrolit oldatok (azaz, oldatok tartalmazó hordozók az elektromos áram - ionok) és kíséri a kialakuló elektromos áram. Kémiai korrózió lép fel, ha olyan fém száraz gázok, por és folyékony anyagok (nincs elektrolit), és nem kíséri a kialakuló elektromos áram. Romboló hatását a korrózió mindig indul a fém felületén. Ezután, a korrózió terjed alapos ütemben típusától függően a fém vagy ötvözet, annak összetétele, szerkezete, tulajdonságai és összetétele és jellemzői a környezetet. Ez a folyamat gyakran kíséri változások a felületi megjelenés: ez lesz unalmas, színe megváltozik, úgy tűnik pontok, foltok, hólyagok, stb Ennek eredményeként a kölcsönhatás az alumínium a környezettel kialakított anyag (korróziós termékek), amelynek tulajdonságai nagymértékben befolyásolják az áramlás .. korróziós folyamatokat. Mérlegeli a lehetséges variációk egy ilyen hatás:
A folyamat során a korrózió termelt illékony vagy oldható anyagok, amelyek könnyen és gyorsan eltávolítható a reakció tér és nem akadályozza a terjedését korrózió. Ennek eredményeként, a reakció az egész fémfelületet rendelkezésre maró és simán terjed mélységét.
Egy fém felület, amelynek vékony, átlátszó, erősen kötődik a fém rétegek, amelyek átfedik az agresszív reagens hozzáférést a fém szubsztrátum. Ezek a rétegek az oka az úgynevezett „passziválás” felületre. A formáció az ilyen korróziós réteg szinte teljesen leállt, és a maradék folyamatok zajlanak csak a külső felületén a réteg, amely részlegesen oldódik agresszív környezetben.
A heterogenitás a felszíni réteg eredményeket a megnyilvánulása egyenetlen vagy lokalizált korróziót. Egy réteg korróziós termékek egyenetlenül oszlik egész felületén a korrodálódó fém.
Tulajdonságaitól függően a korróziós termékek különbséget tud tenni a következő típusú legújabb:
A helyi korrózió formájában foltok a fém felületén.
Helyi korrózió formájában korrózió, amely akkor jelentkezik, ha a folyamat zajlik a felszínen kis területen intenzíven, és benyúlik a fém.
Szemcseközi korrózió merül fel, amikor az agresszív anyag jön a fém, és elpusztítja a külső határát kristályok (szem), hogy tartalmazzák a fúziós. A korróziós termékek maradjon a fém, és a külső felület nem teszi észrevehető változást. Ez különösen veszélyes formája a korrózió szempontjából folyamat sebességét. Ebben az esetben, az anyag generál szemcsehatár, elvégzi a szerepe az anód képest a szemek, amelyek elfoglalják egy nagy területet, és úgy járnak, mint katód.
Korrózió feszültség és egy származékával - korrózió fáradtság merül fel, ha azon kívül, hogy hatásait korrozív környezetben a fém terméket vetjük alá állandó vagy változó terhelések.
Szelektív (szelektív) korrózió, amelynek során egy vagy több összetevőt az ötvözet kitett alkatrészek korrózió, és a porózus ötvözet megtartja az eredeti alakját a termék.
elektrokémiai korrózió
A műszaki alumínium (vagy annak ötvözetéből) tartalmaz fém szennyeződések formájában az egyes zárványok (magnézium, titán, vas, mangán, stb). Mivel a jelenléte az ilyen zárványok ötvözet, elmerül a elektrolit, ez egy aggregátum nagy számú mikroszkopikus gócok galvanizáló. Ennek eredményeként az elektrokémiai reakció fordul elő, hogy ezek a gócok, fém, kiálló az anód szerepét (ebben az esetben a fő összetevői az ötvözet, alumínium), feloldjuk, miközben hidrogén szabadul fel a microcathodes. A korrózió a microsources eredendően hagyományos elektrokémiai cellák és jellemezhető:
1 mikroszkopikus mérete az anód és a katód;
2 vízszintes elrendezése az elektródák;
3, a közvetlen kapcsolat a katód és az anód.
A folyamat elektrokémiai korrózió nem mindig eredményeként az esemény a mikroszkopikus galvánelemek. Egyes esetekben a korróziós központok „látható” (makroszkopikus) méretét. elektromechanikus korróziós megsemmisítése mechanizmus különböző méretű a katód felületét (acél) és az anód (alumínium) ábrán látható. 3.
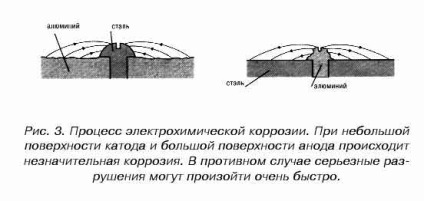
légköri korróziónak
Légköri fémek korrózióját az a folyamat, megsemmisítése a levegő eredményeként bekövetkező felszínükön kémiai és elektrokémiai reakciók. Ez a leggyakoribb példája megsemmisítése fémek.
A külső tényezők a következők:
A belső tényezők a következők:
a kémiai összetétele az ötvözet;
Nedves atmoszferikus korrózió következik be az elektrolit réteg kis vastagságú. A folyamat sebessége függ a levegő páratartalma, a légköri szennyeződések és a korróziós termékek higroszkóposság, ha ezeket az anyagokat megtartja a nedvességet a fém felületén, a korrózió sebessége növekszik.
Marine légköri korróziónak. A régiók tengeri klímájú a légkör tartalmaz nagy mennyiségű sók felületén a fém cseppek összegyűjtjük tengervíz, sókat és egyéb szennyezőket, amelyek felgyorsítják a korrózió.
A reakciót az alumínium és ötvözetei más fémek és ötvözetek
Az elektrolit közegben két különböző fém érintkezésben vannak egymással, vagy csatlakozik egy vezeték alkotnak elektrokémiai cella, azzal jellemezve, a generált elektromos áram. A mozgási iránya az elektronok a sejt által meghatározott értékek az elektród potenciál a fémek, korrózió intenzitása előforduló, amikor a két fém függ a helyét a sorozat feszültség (potenciál különbség), az arány a felszíni terület és a szint a polarizáció. Minél nagyobb a potenciális különbség a sejtben, annál nagyobb a feszültség és az intenzívebb az anód megsemmisül. potenciális feltüntetett értékeket elektrokémiai feszültség sorozat, meghatározzuk a standard körülmények között (hőmérséklet 25 ° C, és az egység aktivitása ionok az elektrolit oldat). Tartsuk szem előtt, hogy az összetételtől függően az elektrolit, ezek az adatok változhatnak. Például, lúgos oldatok korrodált alumínium sokkal erősebb, mint a sav. Cink, amely a potenciális közel van, hogy az alumínium lehet használni közvetlenül érintkező alumínium. Ha ilyen érintkezés előfordul, semleges és savas közegben, cink-funkciója van egy anódot és egy katódot, így védi az alumínium a korróziótól. Azonban, alkalikus közegben, ezzel szemben, az alumínium aktivitás növekszik, így a cink-gyorsítja a korrózió az alumínium. Az érintkező horganyzott acél alkatrészek (csavarok, stb), és alumínium-cink-alumínium réteg védelmet nyújt kezdetben, de miután törlés cink acélfelület nyitottá válik, ami oda vezethet, hogy a korrózió az alumínium. Érintkezve alumínium ajánlott használni horganyzott acél módszer, mivel ebben az esetben a bevonat vastagsága nagyobb, mint az elektrolitikus horganyzás.
Semmilyen esetben nem szabad csatlakoztatni alumínium réz és ötvözetei, mivel ez vezet a gyors korrózió alumínium (úgynevezett „katasztrofális korrózió”). Ebben a tekintetben az alumínium szerkezetek elfogadhatatlan mindenféle elemek és a rezet. Emiatt nem kell hatása az alumínium esővíz, amely lefelé folyik a tetők és réz cső közvetlenül az alumínium szerkezetek, még akkor is, ha kis mennyiségben tartalmaz a rézionok.
Azt is meg ne érintkezzen az ón és vegyületei, különösen a légkörben szennyezett ipari hulladék. ón-sók előállított savas körülmények között, jelentősen elpusztítani alumínium felületekre. Vörös ólom-oxid, a nedvesség jelenlétében, amely sav mutat erős maró. Ezért, amikor érintkezésbe kerülnek az alumínium kerülni kell acélelemek borított vörös ólom. Higany és sói már a jelenléte nyomokban nedvesség okoz súlyos korrózió az alumínium. Ebben az esetben, a korróziós folyamat tovább fokozza az amalgám képződés: amalgámozott alumínium gyorsan reagál a vízzel hiányában is a savak és lúgok! Ezért, a tárolás során az alumínium profilok is higanygőz (a törött izzó) eredményezhet pillanatnyi korrózió. A vegyület alumíniumból vagy acélból elfogadható a vidéken, de a tengerparti területeken és az ipari acél korrózióját felgyorsító alumínium. Ezért, érintkezve acél és alumínium, hogy elkerüljék a közvetlen kapcsolatot, például horganyzott acél, alumínium festés használata közben szigetelő tömítések készült szintetikus anyag. Amikor vegyületek vas, nikkel és a króm, alumínium történik jelentős potenciális különbség, így nem kell csatlakoztatni közvetlenül egymáshoz. Továbbá, ezek a fémsók (kloridok, szulfátok és hasonlók. D.), amelyek eredményeként kialakult a korrózió, szintén hozzájárul a megsemmisítése alumínium.
Kémiai korrózió.
Az eljárást kémiai korróziós hatására száraz gáz, folyékony, nem-elektrolitokat és egyéb anyagok (beleértve az építési) alumínium.
Ennek eredményeként a kémiai támadás az alumínium felülete védőréteggel álló korróziós termékek és megelőzik a kölcsönhatást az agresszív szerek a fém. A mértéke és típusa kémiai korróziós folyamat határozza meg a diffúzió agresszív anyagokat át a védőréteg. Ahogy korábban említettük, egy réteg alumínium-oxid felületén keletkezik eredményeként oxidációs a fém alapanyag a levegőből oxigént. A levegő a nedvesség kizárásával a réteg vastagsága néhány perc 10 A-ig.