A entrópia a folyékony és gőz
Mint ismeretes, az összes kerületi összefoglalva az eljárás Q1 hőt hasznos munka át csak (Q1- Q2) kcal, és kcal Q2 továbbítjuk a hűtőbordát. A hő Q2 jelentése egyenes. Bár szükséges, a veszteség, ami arra kell törekedniük, hogy csökkentsék.
Engedje meg, hogy milyen tényezők függvénye. Tegyük fel, hogy az egyensúlyi zajlik Carnot-ciklus (ábra. 5.9).
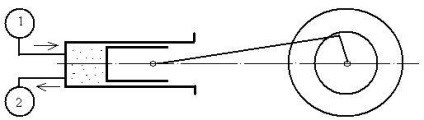
Ábra. 5.9. Rendszer részt vevő szervek a Bizottság
Ehhez ciklus, vagy a =.
Mint látható, a Q2 értéke két tényezőtől függ: a kapcsolat, és a T2 hőmérséklet. Ha a hőmérséklet tekinthető állandó érték, a hőveszteség Q majdnem kizárólag az arány. Minél magasabb az arány, annál nagyobb a veszteség a Q2.
Mivel nagy szerepet kapcsolatokat. A termodinamika bevezetett egy speciális érték, ami attól függ, hogy ez a kapcsolat, és a hívott e n t r o n e és d.
Ha egyensúlyi folyamatát ellátó vagy hő eltávolításával hajtjuk végre állandó hőmérsékleten, mint a Carnot-ciklus, a változás entrópia ilyen folyamatokban, hogy 1 kg test
q - a folyamatban részt vevő hő;
T - a hőmérséklet, amelynél a folyamat megy végbe.
A fenti képletben az S1 veszi nulla T1 = 273 ° C, a fajhője víz tekinteni, hogy az 1 kcal / kg # 8729; Grad.
Az entrópia folyadék (víz) pontja azt növekszik az entrópia 1 kg víz, amelynek hőmérséklete 0 ° C-on, melegítés közben, hogy állandó nyomáson felforraljuk.
Ha nincs víz felforraljuk, majd annak entrópia
ahol T - a végső víz hőmérséklete.
Entrópiája forrásban lévő folyadék
Entrópia száraz telített gőz egy 1 kg-os növekedése entrópiája vízben vett 0 ° C, az átalakulás során állandó nyomáson száraz telített gőzt.
A folyamat a gőz készítésére forró vízből történik állandó hőmérsékleten; ezért a változás entrópia ebben a folyamatban megtalálható az egyenletből
Ebben az esetben a (entrópia száraz gőz) (folyékony entrópia); q = r - a párolgási hőt), és a T = Ts.
Egyértelmű, hogy az entrópia nedves gőz SX. amelyre q = XR, egyenlő:
Entrópia túlhevített gőz s jelentése 1 kg növekedése entrópiája vízben vett 0 ° C, az átalakulás során, állandó nyomású túlhevített gőzt.
A folyamat során állandó nyomáson túlhevített gőz hőmérséklete megnövekszik, így a változás az entrópia során túlmelegedés kell számítani a következő egyenlettel
CPM - átlagos izobár fajhője túlhevített gőzzel
T - abszolút hőmérséklete túlhevített gőz.
Ebből az egyenletből, megkapjuk