A hemosztázis alapvető mechanizmusai
hemosztázis rendszer - ez egy biológiai rendszerben, amely vérmegőrzési folyékony állapotban, másrészt, megelőzését és ellenőrzését a vérzés - az egyéb, a strukturális integritásának fenntartása az erek, és kellően gyors trombózis legújabb amikor megsérült.
Haemostasis valósul főleg három, egymással kölcsönhatásban funkcionális szerkezeti elemek: a falak a vérerek, a vérsejtek és a plazma enzimrendszerek - véralvadási, fibrinolitikus, kalikrein-kinin és mások. A rendszer ki van téve egy komplex neurohumoralis rendelet egyértelműen működő mechanizmusok pozitív és negatív visszajelzést, hogy a celluláris vérzéscsillapítás és véralvadási kezdetben mennek önaktiválás, majd növeli a trombózis lehetséges a vér.
A magas trombór-ellenállással rendelkezõ hajók fala elsõsorban a vér folyadékállapotát tartja fenn. Az endotél tulajdonsága a következő jellemzőkkel függ össze (Barkagan ZS 1980):
- az endothelium képes hatékony thrombocytaaggregációs inhibitor - prostaciklin szintézisére és izolálására;
- a szövetaktivátor fibrinolízisének előállítása;
- antikoaguláns potenciál létrehozása a vér / szövet határán, az antitrombin III szintézise és a heparin-antitrombin III komplex rögzítése az endotheliumon;
- képtelen kapcsolatba lépni a véralvadási rendszer aktiválásával;
- az aktivált véralvadási faktorok eltávolítása a véráramból.
Másrészt az endotélium olyan anyagokat is szintetizál, amelyek hemostatikus reakciókat fejtenek ki a következő módokon:
- engedje a vérbe a szöveti tromboplasztin (Ill-as faktor), valamint a vérlemezke-stimulánsok - epinefrin, norepinefrin, ADP, stb.;
- a kollagén és a szubendothelium egyéb komponenseinek kontaktus aktiválása mint vérlemezkék (tapadás) és véralvadás (XII faktor aktiválása);
- plazma kofaktorok előállítása és a vérlemezke aggregáció - von Willebrand faktor. A kollagén a fibrinolitikus rendszert is kiváltja (ZS Barkagan, 1980, 1985).
A vérlemezkék bevonása a hemosztázisba a következő funkcióknak köszönhető:
- angiotroficheskoy - képes fenntartani a normális szerkezete, ellenállás és áthatolhatatlansága eritrociták mikroér falak. Az endothel sejtek nem képesek felvenni az általuk igényelt anyagokat, de ezek a sejtek aktív felszívják a vérlemezkéket, bármi legyen is felhalmozva. Az endothel sejtek hiányoznak vérlemezke öltözködés gyorsan distrofiruyutsya, gyorsabb törékennyé válik, és elkezd átjutni a citoplazmában vörösvértestjei;
- ragasztással-aggregációs funkció - a vérlemezkék képesek betartani a sérült érfal és egymással, így egy vérlemezke dugót, és a szállítás a hely a saját kár és az adszorbeált vérzéscsillapítás tényezők.
A vérlemezkék aggregálódását számos stimuláns valósítja meg: kollagén, ADP, arachidonsav és származékai (tromboxán), adrenalin, trombin. A kollagénhez való vérlemezke-adhézió legfontosabb plazma kofaktora a vérben keringő glikoprotein - a von Willebrand-faktor. A vérlemezkék felhalmozódnak és titkosítják a "felszabadulási reakció" alatt (3. S. Barkagan, 1985);
- a sérült hajók spasmának fenntartása a vasoaktív anyagok szekréciójával - noradrenalin, adrenalin, szerotonin stb .;
- a vérrögképződésben való részvétel - a vérlemezkék, amelyek olyan szivacsok, amelyek adszorbeálják a véralvadás sok plazma összetevőjét, aktiválják a véralvadást, amikor ezek az összetevők szabadulnak fel. Vannak vérlemezke faktorok, amelyekben vérlemezke van. Ez a harmadik thrombocyta faktor (3 pF), ami felgyorsítja a véralvadási faktorok kölcsönhatását; anti-heparin faktor (4 pF), amely magas anti-heparin aktivitással rendelkezik, amely képes a vérlemezkék és eritrociták aggregálódásának fokozására. A thrombocyták aktiváló hatása a fibrinolízisre nagyon hangsúlyos.
A hemosztázis mechanizmusa. A sérült hajó méretétől függően két hemostasismechanizmus létezik: vérlemezkeszám, primer, koaguláció vagy másodlagos. Az első esetben a vérzés leállításának vezető szerepe az érfal és a vérlemezkék közé tartozik, a második - a véralvadási rendszer. A vérzés leállításának folyamata során mindkét mechanizmus összefügg.
Érrendszeri-vérlemezke hemosztázis végezzük közvetlenül a sérülés után a kis hajók: az első görcs jelentkezik a terminális vaszkuláris sérülés helyén okozott neurovascularis reflex vazokonstrikciót továbbá feltéve, adrenalin, amely reflexszerűen a vérben szabadul fel (4. ábra).
A vérlemezke hemostazis rendszere
Ábra. 4. A thrombocyta hemostasis mintája
1-3 másodperc sérülés után kezd kiválni a hemosztatikus vérlemezke trombus: a hajó a sérülés helyén fordul elő, tapadását és aggregációját vérlemezkék, ha betartják a károsodott endoteliális sejtek, a kollagén. A vezető szerepet az elsődleges távon tartozik ADP aggregációt, a bejövő a sérült érfal és eritrociták (3.c. Barkagan, 1985). A sérült érfal aktiválja az endogén vérlemezke aggregációs faktorokra (ADP, adrenalin, szerotonin, tromboxán).
A trombin mikro-dózisai teljesítik az intragranuláris faktorok "felszabadulási reakcióját", megerősítik és megerősítik a trombust a fibrinnel. A vérzési idő növekedése (Duke tesztje) megerősíti, hogy az elsődleges hemosztázist főleg vérlemezkék, és nem véralvadás okozza.
A thrombocyta thrombus csak az alacsony artériás nyomással járó microprocesszorokban leáll. A vérerek nagyobbak, magasabb vérnyomás esetén a thrombocyta trombus már nem képes megbízható hemostasis biztosítására. Ilyen esetekben a vezető szerepe a vér koaguláló rendszere, a véralvadási hemostazis.
Véralvadási - többlépcsős kaszkád enzimes eljárás, amelyben proenzimeket egymást követően aktiválódnak, és hatnak autokatalízis erő, működik, mint egy felülről lefelé, és a visszacsatolási mechanizmus (3.c. Barkagan, 1985).
Koagulációs tényezők: I-fibrinogén; II - protrombin; III - tromboplasztin; IV - kalciumionok; V - proacceleurin; VI - egy aktinolin; VII-proconvertin; VIII - antihemofil globulin, a plazma tromboplasztin IX-komponense; X a Prouer-Stewart faktor, XI a plazma tromboplasztin prekurzora; XII - kontakt faktor (Hageman faktor); XIII - fibrin stabilizáló faktor.
A koagulációs rendszerben különbséget tesznek a hemostasis kezdetét aktiváló belső és külső mechanizmusok között. Az elsőnek (belső) a plazmafehérjéknek érintkezniük kell a kollagénnel és más szubendoteliális struktúrákkal, aktiválja az érintkezési tényezőt (XII. Faktor), majd a belső mechanizmussal a véralvadás kezdetét. A második (külső) szövettani tromboplasztin (III-as faktor) bejutása az érfalból és a szövetekből a vérbe, amely a VII-es faktorral együtt az aktivátort X alkotja. Mindkét mechanizmus szükséges a normál hemosztázishoz.
A koagulációs hemosztázis van osztva négy, egymást követő szakaszból áll: I- aktív protrombináz képződését; II-trombin; III-fibrin képződés iIV- poslefaza előírt folyamatok visszahúzás és fibrinolízis (5. ábra).
Az enzim és a nem enzim faktorok közötti kölcsönhatás komplex protein-lipid komplexekben fordul elő, amelyek a koagulációs kaszkád különböző szakaszaiban képződnek. A véralvadás kezdeti stádiumainak aktiválásában kallikrein-kinin rendszert alkalmaztak.
A IX-es faktort az "Xlla + XI + 3 pF" belső mechanizmus első összetevőjében aktiváljuk; egy összetett "factorIXa + VIIICa +++ З пф" - faktorX; Az "Xa + faktor + V + Ca ++ + 3 pF" faktor komplexében az "Y" faktor az utolsó komplex enzimatikusan hat a protrombinra, átalakítva trombinba (protrombin komplex, protrombináz).
P
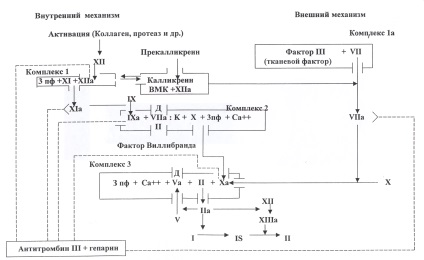
A protrombináz-aktivitás kialakulásának külső mechanizmusában a faktor "III + VII + Ca ++" komplex képződik, amelynek célja az X faktor aktiválása. Ezenkívül a koagulációs eljárás a második fázisba, a protrombin trombinná történő átalakulásának fázisába lép. A harmadik fázisban trombin hasítja le fibrinopeptid A és B a fibrinogén molekulák, ezek átalakítása fibrinmonomery amelyek polimerizálódnak spontán fibrin szálak. A trombin aktiválja a faktorXIII amely erősíti fibrin polimerek (fibrinstabiliziruyuschy faktor) igényel oldható fibrinS (szolubilis) egy oldhatatlan fibrinJ (insolubile). A vérrög fibrin késleltetett vérsejtek - a vörösvértestek, fehérvérsejtek, vérlemezkék, ami az utolsó tömítés és alvadékretrakció.
Fibrinolízis. A véralvadási rendszer funkcionális kapcsolatban áll a fibrinolitikus, kinin és komplement rendszerekkel. A fibrin lízisét biztosító fibrinolitikus rendszer a véráramban ugyanazok a tényezők, mint a véralvadás. A XIIa faktor kölcsönhatásba lép a prekallikrein és a plazma nagy molekuláris kininogénjével (IUD), és aktiválja a plazminogént. A fibrinolízis gyorsabban megy végbe, minél magasabb a lokális plazminogén koncentráció a rögökben. Szintén a fibrinolitikus enzimrendszer a szervezetben nem enzimatikus, fibrinolízis végzett heparin komplex antitrombinIII-adrenalin és működő fiziológiai körülmények között (BA Kudryashov, 1977).
A véralvadás gátlói. A hemostazis lényeges oldala a véralvadási folyamat gátlása. A gátlók megvédik a vér folyékony állapotát a vérben, megakadályozzák a helyi trombusképződés átterjedését széles körben (VA Kudryashov, 1975).
A véralvadás természetes inhibitorainak két csoportja ismeretes:
- elsődleges, megelőzve a véralvadás (antitrombin III, protein C, 2-makroglobulin);
- másodlagos, a véralvadás folyamatában képződött, a proteolízis csoportja (3. S. Barkagan, KM Bishevsky, 1978).
AntitrombinIII a leghatásosabb inhibitora a koagulációs eljárva nemcsak mint egy anti-trombin, de inaktivátorát tényezők Xa, 1HA, Xla, XIIa, VIIa, V. AntitrombinIII és kofaktora - a heparin 4/5 fiziológiás antikoaguláns aktivitást jelent.
A protein-C - által szintetizált májsejtek, K-vitaminzavisimy pro-enzim, amely a trombin aktiválja, és a Xa faktor hasítja, és inaktiválja a fő nem-enzimatikus faktorok VIIIiV.
2-makroglobulin - olyan fehérje, amely képes kötni a véralvadási rendszer aktivált komponenseit és a fibrinolízist, kikapcsolja őket más tényezőkkel való kölcsönhatásból.
A vizsgálat során megállapított vérzés típusai és súlyossága megkönnyíti a diagnosztikai keresést. A vérzés 5 fő típusa van:
I. Hematómás fájdalmas, intenzív vérzések mind a lágy szövetekben, mind az ízületekben a vázizomzat rendellenes patológiáját fejezte ki. Tipikus az A és B hemofília esetében.
2. A thrombocytopenia, thrombocytopathia jellemző petechiális foltos (szinewy), az X és P faktorokban ritkán előforduló örökletes hiányosságok, néha UE.
3. Vegyes-sinyachkovo gematomny jellemzi kombinációja kiütéses-foltos vérzés megjelenésével egyetlen nagy vérömlenyek (retroperitonealis, a bélfalban, stb) hiányában elváltozások az ízületek és csontok, akár egyetlen vérzések az ízületek: zúzódások lehet kiterjedt és fájdalmas. Ez a típusú vérzési megfigyelt súlyos hiányossága tényezők a protrombin komplex és a VIII-as faktor, a von Willebrand-betegség, disszeminált intravaszkuláris koaguláció, túladagolás antikoagulánsok és trombolitikumokkal, amikor a vér immun inhibitorok IX és VIII faktorok.
4. A vasculitikus-lilás típust bőrkiütés jellemzi kiütés vagy erythema formájában (gyulladásos alapon), jádét és bélrendszeri vérzést lehet csatolni; fertőző és immunvasculitis esetén megfigyelhető, könnyen átalakítható ICE-szindrómává.
5. angiomatous típusú megfigyelt teleangiectasia, angioma, artériás-vénás söntök, jellemző a tartós, szigorúan lokalizált és kötve a helyi érbetegség vérzést.
A vérzések felismerésekor fontos figyelembe venni, hogy egyes patológiás módszerek gyakoriak, mások ritkák, és mások rendkívül ritkák. A hemostasis örökletes rendellenességei, a thrombocytopathia (összesítve), az A hemofília és a telangiectasia vaszkuláris formái a leggyakoribbak. Ezek a betegségek a genetikailag meghatározott vérzésformák több mint 99% -át teszik ki. A petechiális pöttyös típus leggyakrabban fordul elő. A trombocitopénia, thrombocytopathia, valamint a külső koagulációs mechanizmus ritka örökletes rendellenességeivel (X, VII, II faktorok hiánya) figyelhető meg.
A vérzés típusának meghatározása laboratóriumi vizsgálatok irányába mutat.
A vaszkuláris thrombocyta hemostasis jellemzésére irányuló kísérletek:
- érfal-ellenállás;
- a vérlemezkék száma 150 000-400 000 / mkl;
- a vérzés időtartama (Duke 2-4 perc alatt, Ivy 8 perc);
Vizsgálatok a hemostasis plazma koaguláló egységeinek jellemzésére:
- a vénás vér koagulációjának ideje Lee-White 5-8 perc;
- a plazma recalcifikációs ideje 60-120 másodperc;
- protrombin idő (protrombin index) 11-15 sec;
- trombin idő 15-20 másodperc;
- a fibrinogén szintje 2-4 g / l;
- a fibrin-rögnek karbamidban (XIII faktor aktivitása) való oldhatóságának vizsgálata 45 másodperc.
Így a tanulmány haemostasisrendszerre kell állapítani az oka vérzés és differenciálódás különböző formáinak veleszületett és szerzett vérzési zavarok, thrombocytopenia és thrombocytopathy.