A gáznemű, folyékony és szilárd testek szerkezete
A molekuláris kinetikai elmélet lehetővé teszi annak megértését, hogy az anyag miért van gáznemű, folyékony és szilárd állapotban.
Gázában. A gázokban az atomok vagy molekulák közötti távolság átlagosan sokszor nagyobb, mint maguk a molekulák méretei (8.5 ábra). Például atmoszferikus nyomáson az edény térfogata több tízszer nagyobb, mint a molekulák térfogata.
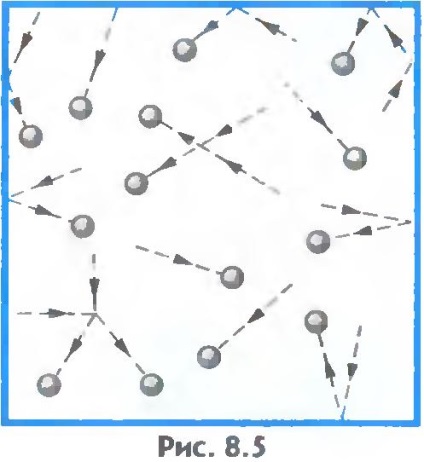
A gázok könnyen összenyomódnak, míg a molekulák közötti átlagos távolság csökken, de a molekula alakja nem változik (8.6.
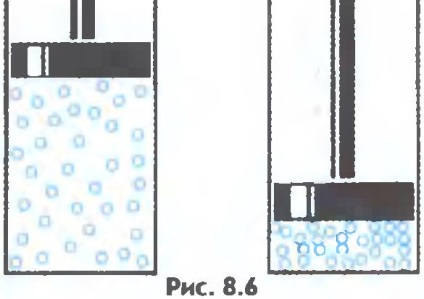
Hatalmas sebességű molekulák - másodpercenként több száz méter - mozognak az űrben. Szembesültek egymással különböző irányokban, mint a biliárdgömbök. A gázmolekulák vonzerejének gyenge erői nem tarthatják egymáshoz közel. Ezért a gázok korlátlanul bővíthetők. Nem tartanak semmilyen formát vagy kötetet.
A molekulák számos hatása az edény falára gáznyomást eredményez.
Folyadék. A folyadék molekulái szinte szinte egymáshoz közel helyezkednek el (8.7. Ábra), ezért a folyékony molekula másképp viselkedik, mint a gázmolekula. A folyadékokban van egy úgynevezett rövid hatótávolságú rend, vagyis a molekulák rendezett elrendezése több molekuláris átmérővel megegyező távolságra van. A molekula az egyensúlyi pozíciója közelében oszcillál. a szomszédos molekulákkal ütközik. Csak időről időre újabb "ugrást" végez, új egyensúlyi helyzetbe esik. Ebben az egyensúlyi helyzetben a visszataszító erő egyenlő a vonzó erővel, vagyis a molekula teljes kölcsönhatási ereje nulla. Ülő élettartama vízmolekulák, t. E. során oszcillációs egy bizonyos egyensúlyi helyzetben szobahőmérsékleten, egyenlő átlagosan 10 -11 s. Az egyik vibráció ideje sokkal kisebb (10 -12 -10 -13 s). Ahogy a hőmérséklet emelkedik, a molekulák rendezett élete csökken.

A folyadékok molekuláris mozgásának természete, amelyet először a Ya.I.Frenkel szovjet fizikus hoz létre, lehetővé teszi a folyadékok alapvető tulajdonságainak megértését.
A folyadék molekulái közvetlenül egymás mellett helyezkednek el. Amint a térfogat csökken, a visszataszító erők nagyon nagyok lesznek. Ez magyarázza a folyadékok alacsony összenyomhatóságát.
Mint ismeretes, folyadékok áramlanak, azaz nem tartják meg a formájukat. Ezt így magyarázhatja meg. A külső erő nem észleli észrevehetően a molekuláris ugrások számát másodpercenként. De a molekulák ugrásai egy elhelyezett helyzetből a másikba elsősorban a külső erő hatásának irányába fordulnak (8.8. Ábra). Ezért folyik a folyadék és egy hajó formája.
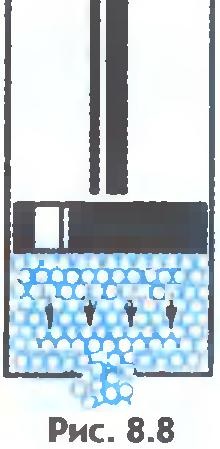
Szilárd testek. A szilárd anyagok atomjai vagy molekulái, ellentétben az atomokkal és a folyadék molekuláival, bizonyos egyensúlyi helyzetek közelében ingadoznak. Emiatt a szilárd anyagok nem csak a térfogatot, hanem az alakot is megőrzik. A szilárd molekulák kölcsönhatásának potenciális energiája sokkal nagyobb, mint kinetikus energiája.
Van egy másik fontos különbség a folyadékok és a szilárd anyagok között. A folyadék lehet hasonlítani a tömegben az emberek, ahol egyesek lökdös nyugtalanul a helyén, és szilárd, mint egy vékony kohorsz az ugyanazon személyektől, akik ugyan nem állt a figyelmet, de között tartjuk egy bizonyos távolságot, átlagosan. Ha egy szilárd atom atomjai vagy ionjai egyensúlyi helyzetét összekötjük, akkor kapjuk meg a helyes térbeli rácsot, amelyet kristályos rácsnak nevezünk.
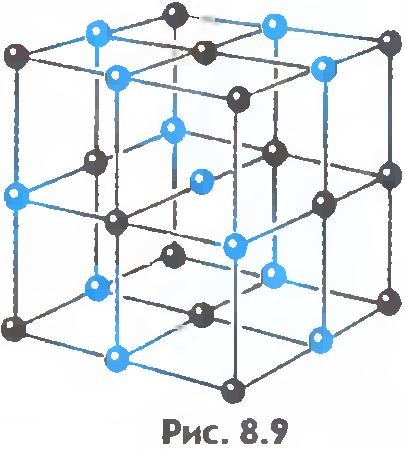
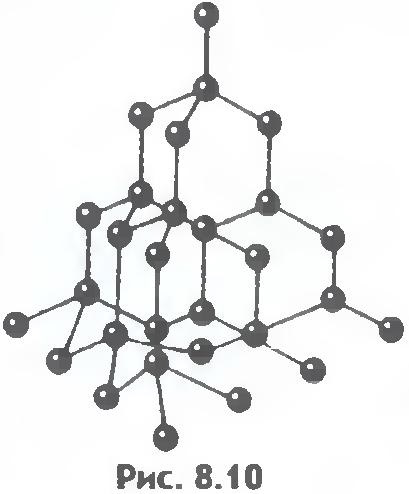
A 8.9 és 8.10 ábrák az asztali só és a gyémánt kristályrácsát mutatják. A kristályos atomok elrendezésének belső rendje megfelelő külső geometriai alakzatokhoz vezet.
A 8.11. Ábra mutatja a Yakut gyémántokat.
Egy gáz esetében a molekulák közötti távolság l sokkal nagyobb, mint a molekulaméretek: r0> l> r0.
Folyadékok és szilárd anyagok esetében r0. A folyadék molekulái dezorientáltak, és időről időre ugrálnak az egyik telepített pozícióból a másikba.
A kristályos szilárd anyagokban a molekulákat (vagy atomokat) szigorúan elrendeljük.
.
1. A gáz képes korlátlan terjeszkedésre. Miért létezik a légkör a Földön?
2. Mi a különbség a gáz, folyadék és szilárd molekulák mozgáspálya között? Rajzolja meg az anyagok molekuláinak közelítő pályáját.
G.Ya.Myakishev, B.Buhovtsev, N. N.Sotsky, a 10. fokozat fizikája
Gyűjtemény a leckék minden osztályra, házi feladat, esszék a fizikáról. könyvek és tankönyvek a fizika ütemezése szerint a 10. fokozatba
Ha bármilyen korrekció vagy javaslata van ehhez a leckéhez, írjon nekünk.
Ha látni szeretné a leckék más módosításait és kívánságait, nézze meg itt - Oktatási Fórum.