A ritkaföldfém-elemek szétválasztásának módszerei
A lantanidok tulajdonságainak közelsége miatt ezek szétválasztása összetett probléma. A korábban alkalmazott elválasztási módszerek elsősorban a lantanidvegyületek oldékonysági különbségén alapultak. Számos frakcionált kristályosodásnak vagy frakcionált lerakódásnak (néha több ezernek) köszönhetően nagyobb vagy kisebb tisztaságú különálló elemeket kaptak. Néhány elem elkülönítéséhez négy vagy több (Sm, Eu, Yb) valenciájához használták vagy helyreállították a négyértékű állapotba (Ce, Pr, Tb) való oxidálásra való képességet. Ebben az esetben a szétválasztást megkönnyítik a + 4 és + 2 oxidációs állapotú lantanid vegyületek és a +3 oxidációs állapotú lantanid vegyületek tulajdonságainak jelentős különbségei.
A lantanidok szétválasztására szolgáló modern rendszerek hatékonyabb módszerek alkalmazásán alapulnak: folyékony extrakció és ioncsere. A régi "klasszikus" módszereket a frakcionális kicsapás és a kristályosítás gyakorlatilag nem használják jelenleg.
Egyes szétválasztási sémákban a szelektív oxidáció és redukció módszereit alkalmazzuk.
A tetravalens állapotú cérium oxidációját használjuk fel a többi lantanidtól való elválasztására. Cérium Könnyen oxidálódik oxigén a folyamat a szárítás a keverék lantanida hidroxidok levegőn 120-130 ° C-on, vagy amikor az áthalad egy kosár-felmelegített iszapot szellemét hidroxidok. Más oxidálószereket is használnak: klór, hidrogén-peroxid. Miután Oki-lized Ce3 + a Ce4 + hidroxidjai háromértékű lantanidák feloldunk híg (5 - 10%) vagy a salétromsav CO-lyanoy, míg a tetravalens cérium-hidroxidot (Ge02 • yaN20) marad a csapadékot. Az utóbbi 94-96% Ge02-et tartalmaz.
Egy tiszta termék előállításához Ce (N03) 4 6 és 8 N közötti szelektív extrakcióját használtuk fel. salétromsav oldat tributil-foszfáttal vagy más extrahálószerrel.
Az oxidációs állapot +2-re való visszanyerés a szamárium, az europium és az itterbium elkülönítésére szolgál a dúsított frakcióktól. Az Sm2 +, Eu2 +, Yb2 + ionok hasonlóak a stroncium és a bárium ionokhoz. Így a szulfátok kicsit oldódnak, szemben a lantanid-szulfátokkal (+3). Mivel a restaurátorok cinket, cink-amalgámot, nátrium-amalgámot használnak.
Az oxidációs redukciós potenciálokat Sm, Eu és Yb (a hidrogénelektróddal szemben) az alábbiakban adjuk meg, B:
Sm37Sm2 + -1,72; Yb3 + / Yb2 + -1,15; Eu3 + / Eu2 + -0,43;
Zn2 + / Zn-0,76; Na + / Na (Hg) -1,86.
Ezekből a potenciálokból következik, hogy az Eu3 + ionokat szelektíven csökkenteni lehet az Eu2 + -ra cinkporral, ami nem helyezi vissza a Sm3 + vagy Yb3 + ionokat. A visszanyerést sósavoldatban végezzük. Amikor az oldathoz kénsavat adunk, enyhén oldódó EuS04 csapódik le.
Az tripile töltésű europium és a szamárium ionok együttes csökkentése nátrium-amalgámmal lehetséges, amellyel ecetsavoldatot, amely lantanidok szétválasztható keverékét tartalmazza:
L '(CH3COO) 3 + 3Na (Hg) = Zn (Hg) + 3CH3COONa. (11.4)
A visszanyert elemeket sósavval kezeljük az amalgámból. Az europium és a szamárium elkülönítését ezután az európai cinkpor helyreállításával lehet elvégezni.
Hatékony változata elválasztása európium a másik REE szelektív kivonása háromszoros töltésű ionok ritkaföldfém kationcserélő extrahálószert - di-2-etilgeksilfosfornoj sav (D2EHPA), gyakorlatilag kitermelése ionok EU2 +
A REE elválasztása extrakcióval
Jelenleg az extrakciós módszerek váltak a legfontosabbak a REE szétválasztására szolgáló rendszerekben. Az ipari gyakorlatban a szerves foszfor extraktorokat - TBP, D2EHPK és karbonsavak - használják szétválasztásra. A részleg a lantanid-sorozat eloszlási együtthatóinak rendszeres változásán alapul.
Az alábbiakban a REE extrahálás szétválasztását a leggyakoribb extrahálószer, a TBP alapján kell figyelembe venni. A TBP mint extrahálószer jellemzése a Ch. 2. Az ipari gyakorlatban a REE elválasztása a TBP extrakciójával elsősorban salétromsavoldatokból történik,
amely a REE nitrátjait tartalmazza. Az extrahálás a triszolvát képződésével kezdődik:
^ l (aq) + 3N03 (BoaH) + ZTBF (0RG) <—-
L / i (N03) 3 • ZTBF (0RG); (Ts.5)
D = ^ C [N03] ^ H) • [TBF] (ORG),
Ahol Kc az extrakciós reakció egyensúlyi állandója.
A TBF-HN03 rendszerben a nagy koncentrációjú HN03 (11-15 m / l) eloszlási együttható értéke folyamatosan nő a lantanid atomszámának növekedésével. Azonban az 5 m / l alatti koncentrációjú HN03 koncentrációjú oldatokban az europium-lutétium eloszlási együtthatók változásának szabályossága inverz (fordított). Ennek oka az alacsony kis-jj
A lateralitások növelik a hidratálási energiát egy sor nehéz nehéz REE-ben, ami megnehezíti a vízmolekulák eloszlását az ion hidrátjától a TBP molekulákkal. Ft0
82. ábra. A REE elosztási együtthatója - jq-3 hasadás (D) függvénye a t rendelési számon
> 7 59 61 63 65 67 69 71
A TBP kivonásakor
A magas pH (több, mint 12 m / L) Közepes-nagyság az elválasztási együttható a szomszédos elemek által lan-Tang terbium 0 = Dz + 1 / Dz = 1,9; a terbiumtól a lutéziumig terjedő elemek esetében ez az érték alacsonyabb. Ezért az egész REE csoport esetében 0 = 1,5. A könnyű ritkaföldfém (La, Ce (IIl), Pr, Nd, Pm) keffitsienty elosztó változás kicsit a növekedés azok koncentrációja az oldatban a 5-10, hogy 70-100 g / l: közepes P33 (Sm, Eu, Gd), és nehéz elemek
(ittrium-csoport), az eloszlási együtthatók nagymértékben függnek a vizes fázis REE koncentrációjától.
A REE-t a TBF-ből szintén gyengén savas nitrát-oldatokból extraháljuk só-kioldó szerek - alumínium, nátrium, kalcium, lítium-nitrátok jelenlétében.
A TBP kivonásakor a REE alcsoportokba történő elválasztására az eljárást 7-10 m / l koncentrációjú HN03-koncentrációjú nitrát-oldatokból hajtják végre. Ebben az esetben az ittrium belép a nehéz REE (Dy-Lu) alcsoportba.
A ritkaföldfém-elemek TBP extrahálásával történő elválasztására szolgáló nitrátoldatokon kívül rodanid-klorid oldatokat is alkalmaznak. Ezek REE vannak jelen a komplexek Ln (SCN) 3, és az Ln (SCN) 2CI, ellenállása ami növeli a lantán a lutécium. Az extrahálható komplexnek az Ln (SCN) 3 összetétele van # 9632; • "TBF, n = 3-I.
A REE kivonatok elválasztásának gyakorlatában az eljárást többnyire extrahálók, például keverő-ülepítő kaszkádban hajtják végre. Teljes ellenáramú rendszert használnak, amely extrakciós és mosási szakaszokból és egy újrahasznosítási szakaszból áll (lásd: 83. ábra). A kaszkád teljes fázisszáma 50 - 90.
Az elválasztott keveréket tartalmazó kezdeti oldat a kaszkád középső részébe kerül. Nyilvánvaló, hogy a keverék n elemeinek elválasztásához n-1 szekvenciális műveleteket vagy n-1 extrakciós kaszkádokat kell végrehajtani.
Kezdetben, teljes ellenáramú üzemmódban,
A REM (A * B)
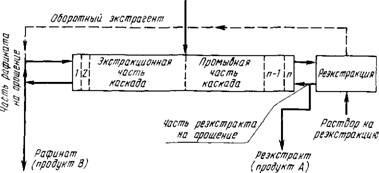
O. A REE elkülönítésének módja extrakcióval egy teljes ellenáramú rendszerben
A REE elválasztása alcsoportokba: könnyű REE (La, Ce, Pr, Nd), közepes (Sin, Eu, Gd, Tb) és nehéz (Dy-Lu + Y). Ezután minden alcsoportban további osztályozást hajtunk végre.
Ennek megfelelően, a számítás az első szakaszban hajtjuk végre, amelynek középpontjában a szétválasztása a neodímium és a szamárium (számítás alkalmazásával érték Psm / Nd)> kiszámításakor a második szakaszban vannak vezetve a határvonal terbium - diszprózium (értékét használja RDD / mh) -
Csoportmentesítés esetén a salétromsav többnyire mosóoldatként szolgál.
Más kiviteli alakokban, szétválasztása ritkaföldfém elemek, különösen a Sec-lenii kétkomponensű (A + B), például neodímium-dence önmagában is alkalmazhatunk cseréjére mosási szakaszban. Ebben a SLU-tea mosási lépésnek újrahasznosítják része a kivonat tartalmaz zhaschego jobb-extrahálható komponens például B. A mosási szakaszban miatt kapcsolatba fázisú komponens B kiszorítja a szerves fázisú komponensének a keverék-ta A. Ez hozzájárul, hogy megszerezze a több tiszta a B komponens esetében csökken a mosóoldat és az extrahálószer relatív költsége.
REE elválasztása ioncserélő kromatográfiával
Amint azt fentebb már jeleztük, jelenleg a folyadék-folyadék extrakció a legfontosabb módja az REE elválasztására. Az ioncserélő kromatográfia egy további módszer, amelyet egyénileg nagy tisztaságú REM-ek előállítására alkalmaznak, elsősorban nehéz.
A lantanidok ioncserés kromatográfiás módszerrel való elválasztására különféle típusú kationcserélő gyantákat használnak (a Szovjetunióban a KU-2 kationcserélő fokozat). Erősen savas kationcserélők, amelyeket sztirol és divinil-benzol kopolimerizálásával állítanak elő, és aktív csoportokat tartalmaznak - S03H. Az elválasztást elsősorban eluáló kromatográfiával végezzük.
A gyantához lantanidionok affinitása a La3 + -ról a Lu3 + -ra csökken, vagyis a hidratált ionok méretének csökkenésével. Azonban a ritkaföldfém-gyantákhoz való affinitás nagyon közel van, ami nem biztosítja a kellően hatékony elválasztást. A jobb elválasztást olyan eluáló oldatok alkalmazásával érik el, amelyek szerves vegyületeket tartalmaznak, amelyek különböző stabilitást biztosító komplexeket képeznek REE ionokkal.
A kiszivárgás a lantanidok anionos komplexek erejének megfelelő szekvenciában következik be. Mivel a sztrippelő oldatot elmozdulása az oszlop (vagy sor következésképpen csatlakoztatott oszlopok) keveréke kationok Sec-szorpciós kíván létrehozni az egyes zónák (csíkok), mozgassa-schiesya egy bizonyos sebesség, a kijárat felé az oszlop. Mert-myvaniya használt különböző szerves vegyületek, ob-komplexek képzésére lantanidák: citromsav, nitro- rilotriuksusnuyu triecetsav (NTA) és etilén-diamin-tetraecetsav (EDTA). Ez utóbbit a legszélesebb körben alkalmazzák az REE kromatográfiás elválasztására. Az EDTA az a-aminosavak osztályába tartozik. Két nitrogénatomot tartalmazó, tetrabáziás sav:
NOOC - CHA / CHj - szójabab
N - CHj - CH 2 - N HOOC - сН / ЧСНг - СООН.
A rövidített EDTA-formula H4V. A sav dinátrium-sójának neve "Trilon-B".
Háromszorosan töltött lantanidionokkal az EDTA intrakomplex vegyületeket (kelátokat) képez, amelyekben a nitrogénatomok kötődnek a lantánsavhoz koordinációs kötésekkel
CH2COOH N-CH 2COO-
N - -CH2COO- - SN2SOO-
Ezen összetett vegyületek stabilitási állandóját az alábbi egyenlettel határozzuk meg:
Ln3 + + HV3-z ± H (Lnv); (11,9)
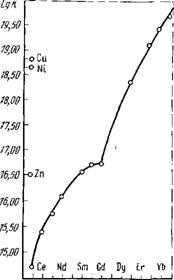
[Ln 3 +] • [HV3-] Amint az az 1. ábrából látható. A lantanidok EDTA komplex komplexeivel szembeni stabilitási állandók a lantánról a lyuténre növekednek, vagyis az elem rendszámának növekedésével. A két szomszédos REE komplex stabilitási állandói átlagosan 2,4-szer különböznek egymástól. Ez az etilén-diamin-tetraecetsav hatásának nagyobb szelektivitását eredményezi a gyantából származó REE-kationok elúciójában.
A REE-t elválasztják egymástól a gyantával töltött oszlopok sorából álló rendszerben. Az első egy vagy két oszlop a gyantát REE kationokkal telíti, a következő oszlopok elválnak. Az elúciós folyamat során szorpciós sávok képződnek bennük.
La Pr Pm Eu Th elemek
Ris.84. A REE komplexek K stabilitási állandói EDTA-val függenek az elem megrendelési számán
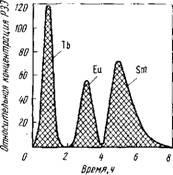
Pmc.8S. A terbium, az europium és a szamárium eluálódásának görbéi, a reszelővel szemben 0,26 M EDTA; pH = 3,62
A telített oszlopokban a gyantát először NH + ionokkal töltjük (azaz a gyantát NHJ formában használjuk). Az elválasztó oszlopokban a gyantát Cu2 + formában használjuk. Ebben az esetben a Cu2 + ionok játszanak a moderátor ion szerepét, ami elősegíti a jobb szétválasztást. A rézionok erősebb komplexeket képeznek az EDTA-val, mint a legtöbb lantán-ion (lásd a 84. ábrát). Ezért, úgy, hogy a sztrippelő oldat zhaschego-lantanida komplex ionok EDTA-val, az elválasztó oszlopon rézionok oldatba megy, kiszorítja a megoldás a ritkaföldfém ionok a gyanta és ezáltal lassítják a haladást. Ez biztosítja a ritkaföldfémek nagy koncentrációját a gyantában.
Általában dolgozik egy cserje ki az oldatot (az eluátum), tudván-chenie táptalaj kémhatását pH = 3,5 - 8,5 (alacsony pH a szétválasztása fény ritka földfémek, a magasabb - a HRE) semlegesítés ammónium-hidroxid. Következésképpen az eluálószer az EDTA ammóniumsóját tartalmazza. Mivel a lantanid komplex savak ammóniumsói EDTA-val és rézkomplexekkel szemben viszonylag oldhatatlanok, alacsony koncentrációjú (5-10 g / l) EDTA-oldatokat használnak eluálásra. Magas koncentrációban a sók szabadulnak fel, eltömve a pórusokat a gyanta szemcséi között, ami a normál működés megzavarásához vezet. Az EDTA alacsony koncentrációja az eluálóban korlátozza az elválasztási folyamat termelékenységét, mivel az oszlopon megjelenő szűrletben lévő REE alacsony koncentrációja korlátozott.
Az oszloprendszerből való kilépésnél a szűrletet külön frakciókkal összegyűjtjük. Az 1. ábrán. A 85. ábra az EDTA oldatból származó mosási görbéket mutatja három elem elválasztása esetén. Az első hullám megfelel a terbium hozamának, a második az europiumnak és a harmadik a szamáriumnak, ami megegyezik a komplex vegyületek Tb-Eu-Sm sorozatának csökkenésével.
Az EDTA regenerálódásához az oldatokat pH = 0,5 * 1-re savanyítjuk. A lantanidok összetett vegyületeit elpusztítjuk és kevéssé oldódó EDTA csapódik ki.
Ha a kezdeti specifikus terhelése (tömegarány alom-szorbeált a gyantakeveréket szétválasztott ionok a teljes súlya a gyanta) kicsi (kevesebb, mint 5 tömeg% gyanta), és a teljes hossza oszlopainak a szétválasztás elég nagy ahhoz, a szűrletet feltörekvő az oszlopról frakciók csak az egyik elválasztási trolled lantanidák.
A teljes elválasztás általános tervei
A ritkaföldfémek teljes elválasztására különböző rendszereket alkalmaznak, amelyekben a leírt módszerek kombinálva vannak. Példaként, A 86. ábra a szárítócsoport elemeinek elválasztási sémáját szemlélteti. A szétválasztás általában hidroxidok keveréke, amelyet más elemek szennyeződéséből tisztítanak. Kezdetben a cériumot az oxidációs módszerrel elkülöníthetjük a keveréktől. Ezután gyártsuk elválasztási ellenáramú extrakció három frakcióra: egy könnyű ritkaföldfém (La, Ce, Pr, Nd), átlagos REE (Pr, Nd, Sm, Eu), és a dúsított frakciót gadolínium és az elem-Menten ittrium-csoport (Nd, Sm, Eu , Gd + Yb). A második és a harmadik frakció lehet izolálni a szamárium és európium RESET-MENT nátrium-amalgámot és elválasztja őket, a fent leírtak szerint. Az egyes elkülönített frakciók egyes elemeinek elválasztását extrakciós és ioncserélő kromatográfiás módszerekkel végezzük.
Különválasztjuk az ittrium alcsoport ittrium extrakcióval izoláljuk (például felhasználva extraktorok-tését-klorid-tiocianát rendszer), és két frakcióra: Gd, Tb, Dy, és Ho, Er, Tu, Tb, Lu. További szétválasztást végzünk
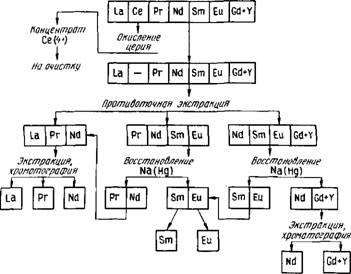
Rks.86. A ritkaföldfémek cériumcsoportból való elválasztásának vázlatos diagramja
Extrakció (teljes ellenáramú vagy félig ellenáramú módszerek) és ioncserélő kromatográfia. Az ytterbiumot amalgám-nátrium-nitrát-oldatokkal történő redukcióval izolálják.