8 A csontszövet biokémiája
A csontszövet különleges típusú kötőszövet, beleértve a szerves és szervetlen természetű komponenseket, amely a Ca depot funkcióját (99%) végzi. A csontszövetnek olyan szerkezeti jellemzői vannak, amelyek nem találhatók más típusú kötőszövetekben. A csont főbb jellemzői a keménység, rugalmasság, mechanikai szilárdság.
Cellákból és csontmátrixból áll (intercelluláris anyag). A csont mátrix 50% száraz tömeg, szervetlen (50%) és szerves (25%) és H2O (25%).
A szervetlen rész Ca (25%) és P (50%) mennyiségben tartalmaz hidroxiapatit kristályokat, valamint egyéb összetevőket: bikarbonátok, citrátok, Mg 2+ sók. K +. Na +, stb.
A szerves részt kollagén, nem kollagén fehérjék, glikozaminoglikánok (kondroitin-szulfát, keratán-szulfát) alkotják.
Maguk a csontos nem kollagén fehérjéket szialoproteinek, proteoglikánok, foszfoproteinek és egy komplex fehérje képviseli, amely szénhidrátkomponenst és ortofoszfátot tartalmaz. A hidroxi-apatit letétbe helyezése a mátrixfehérjék, a szerkezeti jellemzők és a specifikus aminosav-összetétel helyes halmazától függ, ami a szükséges Ca-koncentrációt hozza létre a mineralizációs folyamathoz.
A szialoproteinek molekulatömege 70 000, 50% szénhidrát, 12% sziálsav. A legtöbb szénhidrát oligoszacharid (fruktóz, galaktóz, glükóz, mannóz, pentóz, galaktózamin). Legfeljebb 30% szerin és más aminosavak: aszparagin és glutamin, kovalensen kötődve a foszfáthoz. A fehérje jelenléte:
A nem kollagén fehérjék a csontszövetben körülbelül 200, ezek tömege 3-5%, vagy demineralizált és szárított extracelluláris szerves mátrixának tömege 15-17% -a. Mindegyik részt vesz a hisztogenezis, önfenntartás, immunológiai tulajdonságok biztosításában az élet és a csontszövet javításának folyamataiban.
A csontszövet kalciumkötő fehérjei.
Osteonectin - molekulatömege 32 kDa. Kalciumkötő helyeket tartalmaz szialinsavak és ortofoszfát formájában, amelyek lehetővé teszik a kollagénnel való kölcsönhatást és szelektíven a hidroxi-apatitot. Támogatja a Ca és a PO4 3 kollagén jelenlétében történő kicsapódását.
Az oszteopontin - moláris tömege 41,5 kDa, gazdag aminosavakban és dikarbonsav foszfoszerin, 30 monoszacharidok maradékok, 10 sziálsavmaradékot. Meg tudja erősíteni az osteoblastokat a fiziológiai és a reparatív csontképződés területén. A szintézis drámaian megnő a vírusok átalakulása során.
Az osteokalcin glicidint tartalmazó fehérje.
Az a tény, hogy a csont, mint a más szövetekben, tartalmaz proteineket, amelyek mennek keresztül poszt-transzlációs módosítást a K-vitamin-függő enzimek, így a maradékok képződése y karboksilglutaminovoy sav (GLA). Az így módosított aminosavval a fehérjék képesek Ca 2+ -ot kötni a szomszédos karboxilcsoportokon keresztül. A molekula a fehérje a következőkből áll 49 aminosavból (a 17., 21., 24. pozíciók - maradékok karboksilglutaminovoy y-sav). Ezek szerepe a hidroxiapatit kristályainak kötődése, és ezáltal hozzájárulnak a szövetben való felhalmozódáshoz.
Az osteocalcin szintézise nemcsak a K-vitaminra, hanem a D-re is jellemző, amely hangsúlyozza annak kapcsolatát a mineralizációs folyamattal.
gla-fehérje mátrix (molekulatömege 15 000). A csontmátrixban demineralizáció után tárolják, ellentétben az osteocalcinnal, amely könnyen kivonható ebben az időszakban. Az y-karboxil-glutámsav-maradék legfeljebb hat. Ez kötődik ásványi kristályokhoz és könnyen oldhatóvá a vízben lévő csont morfogenetikus fehérjébe, és átadja a célsejteknek.
A protein-S- szintetizálódik a májban, a csontszövet metabolizmusában való részvételt igazolja a csontvázcsillapítás ténye a betegeknél, akiknél a fehérje hiányzik. De még mindig nem világos, hogy milyen típusú csontszöveteket szintetizálnak.
A proteoglikánokat - osztálya komplex vegyületek, amely különféle fehérjék kapcsolódó oligoszacharidok a glikózamino-glikánok (kondroitin-szulfát, dermatán-szulfát, keratán-szulfát, heparin). Közülük:
Nagy kondroitin-szulfát tartalmú proteoglikán. Feltételezzük, hogy ez a proteoglikán "megragadja a helyet", amely csontvá válhat, mivel a szulfát magas mennyisége miatt jelentős mennyiségű helyet foglalhat el a hidratált állapotban.
A dekorin és a bigalkan szerkezetükben nagyon hasonlóak, egy vagy két glikozaminoglikánja van, a fehérje 24 leucinban gazdag aminosavat tartalmaz. A biokémiai hasonlóság ellenére ezek a fehérjék a lokalizációban különböznek egymástól. A legelterjedtebb decorinus lokalizálása egybeesik a kollagén helyével, amely megfelel a kollagén molekulák "lebontásának" és a fibrillák átmérőjének szabályozására. A Biglikan a mátrixban van tárolva.
Napjainkig számos más típusú proteoglikán izolálódott, de ezek többnyire sejtfelszíni fehérjék, amelyek szerepe kevéssé tanulmányozható.
Az albumin a nem kollagénfehérjék többségéért felelős. Az immunológiai tulajdonságok megegyeznek a szérummal.
A szénhidrátok hatalmas szerepet játszanak a csontszövet létfontosságú aktivitásában, kialakulásának folyamata során. A glikogén részaránya 50-80 mkg 1 g nedves szövetre vonatkoztatva. A glikogén jelenléte szükséges feltétele a mineralizációs folyamatnak, elsősorban a jövőbeli mineralizációs központ helyére koncentrál. A glikolízis és a pentóz-foszfát útvonal nagy intenzitással jár a csontszövetben.
A lipidek fontos szerepet játszanak az ásványosodás és az ionok membránon történő szállításában. Poláris lipidek dominálnak: foszfatidil-kolin,
foszfatidil-szerin, foszfatidil-etanol-amin. Száraz szövetenként csak 0,61% lipid.
1. oldható - részt vesz a trikarbonsavak ciklusában;
2. Oldhatatlan - inaktív, a csontszövet ásványi komponensének egy része.
A csontszövetekben az anyagcsere folyamatok aktívan uralkodnak. Jellemző jellemzője az aerob glikolízis. A glükóz fogyasztása mind az aerob és anaerob körülmények között az oszteogén sejtekkel sokkal nagyobb, mint a májban, az izmokban és más szervekben.
A csontszövet szerkezetét és funkcióit olyan specifikus enzimek tartják fenn, amelyek szintetizálják és lebontják a csont szerves mátrixának makromolekuláris összetevőit és a csontsejteket energiával ellátó közös metabolikus útvonalak enzimjeit. Az enzimek fontos szerepet játszanak a mineralizáció és a csontreszorpció folyamatában.
Meg kell jegyezni az enzimek specifikus lokalizációját. Az osteoclastokban a dehidrogenázok, a savas foszfatáz, a aminopeptidáz nagyobb aktivitása van a többi sejthez képest. Ugyanakkor az osteoclastok nem tartalmaznak alkalikus foszfatázt. Az adenilát-cikláz, a piruvát-kináz, a foszfotranszferázok nagy aktivitása növekedési zónákban, ahol a meszesedési folyamatok folynak.
A savas foszfatáz osteoklasztokban koncentrálódik. Közvetlenül részt vesz a csont reszorpciójában, végrehajtva a foszforsav szerves észtereinek frakcionálását. Így a savas foszfatáz egy lizoszóm enzim, amelynek fő funkciója a katabolizmus, míg az alkalikus foszfatáz részt vesz az ásványosodás folyamatában.
A csontszövet fő fehérje a kollagén, amely 15% -os mennyiségben van jelen kompakt anyagban, 24% -ban szivacsos anyagban.
A csont kollagén - I. típusú kollagén - ez több, mint a más típusú kollagén, hidroxi-prolin, a lizin és a hidroxilizin, a negatív töltésű aminosavak a szerin maradékok magában foglalja a sok-foszfát, ezért, a csont kollagén - egy foszfoprotein. A csont kollagén sajátosságai miatt aktív szerepet játszik a csontszövet ásványosodásában.
A csontszövet létfontosságú aktivitásának folyamata a komponensek és a vérplazma szervetlen ionjai között állandóan kicserélődik.
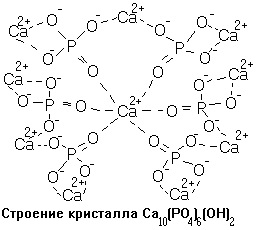
A szervetlen csontkristályok rácsának szerkezete megfelel a Ca10 (PO4) 6 (OH) 2 hidroxi-apatit kristályainak szerkezetéhez - ez a csont ásványi fázisának része, a másik pedig amorf kalcium-foszfát. Ez egy sűrű, nem kristályos anyagot ábrázol amorf granulátumok formájában, ovális vagy kör alakú, 5,0-20,0 nm átmérőjű. Fontos összetevője a csontszövetnek, és jelenléte nem függ a csont anatómiai szerkezetétől, de az életkorától függően jelentős ingadozásoknak van kitéve. Ez a fázis korai életkorban uralkodik, míg érett mátrixokban a kristályos hidroxiapatit túlsúlyban van. A csontsűrűség kialakulását az általános egyenlet tükrözi:
A csontszövet feloldódását elősegíti a tápközeg savasodásának helyi növekedése. A hidrogén-protonok mennyiségének enyhe emelkedésével a csont elkezd feloldódni, és elhagyja az első kalciumkationokat:
A közeg nagyobb savasságával a teljes bomlás következik be:
Az amorf kalcium-foszfát hidrolízise konstans kalciumkoncentrációt biztosít a csontszövet intersticiális folyadékában.
Jelenleg több mint 30 nyomelem ismeretes: Cu, Sr, Zn, Ba, Al, Be, Si, F és mások. Ezek szükségesek az oocyogén sejtek létfontosságú aktivitásához a csontosodás és decalcifikáció folyamatában.
A csontszövet meszesedése és dekalcifikációja szorosan összefügg a nyomelemek tartalmával. Tehát Sr és V hozzájárulnak a meszesedéshez, és a Zn és Ba részt vesznek a dekalcifikációs folyamat szabályozásában. Az Mg számos enzimet aktivál, különösen az alkalikus foszfatáz enzimet, amely részt vesz a mineralizációs folyamatban.
Különös megjegyzés van Sr. Kémiai tulajdonságai közel vannak Ca. Sr verseng a Ca-val a kristályrács helyén, azonban Sr kisebb mértékben megmarad, mint a Ca, ha a Ca uralkodik az étrendben. Ha az Sr étrendjében a Ca hiányossága sokkal nagyobb mennyiségben szívódik fel a szervezetben, mint a normában. Hosszú távú szállítása túlzott mennyiségű Sr szubsztitúciós okoz nekik Ca ionok kristályrácsba a hidroxiapatit, kapott demineralizált csont és deformált.
Egy érett szervezetben a mineralizáció és a csontreszorpció folyamata dinamikus egyensúlyi állapotban van. Az ásványosítás a csontszövet ásványi sóinak kristályos szerkezete. Az ásványiodás aktív részvételét az osteoblastok veszik. Az ásványi anyagok sok energiát igényelnek (ATP formában), amelyet számos tényező szabályoz, beleértve az enzimeket, hormonokat és vitaminokat.
A mineralizációs kutatás döntő fordulata 1923-ban kezdődött. röviddel az alkalikus foszfatáz enzim csontszövetében való felfedezés után. Az angol biokémikus, R. Robinson azt javasolta, hogy a kalcium-foszfát lerakódjon, ahol az enzim működik. Azonban az alkalikus foszfatáz számos olyan szövetben megtalálható, amelyek nem bányásztak, és egyéb tényezők szükségesek a meszesedéshez.
Később számos tényezőt megerősítettek: glikogén, hyholizis enzimek, ATP, CTC, glikozaminoglikánok.
Minden elméletre és néhány kísérleti adatra vonatkozóan az általános elgondolás az enzimek vezető szerepe, amely a szerves foszfátot a szerves szubsztráttól elvágja. A foszfát koncentrációja ezen enzimek működésének területén növekszik, elérve a spontán csapadék kezdetét, ami kristályosodáshoz vezet. •
További vizsgálatok arra utaltak, hogy a folyamat fokális elmeszesedése nukleációs hidroxiapatit oldataiból Ca és P az intézkedés alapján a kollagén rostok, amelyek előírják, egyedi közbeiktatásával reaktív csoportok aminosav-oldalláncok, amely alapul szolgálhat a kristályosodás központok.
Fontos szerepet mineralizáció működnek glükózaminoglikán, különösen a kondroitin-szulfát, amelyek nagy affinitást mutatnak a Ca ionok és R. visszaigazolást a kísérleti adatok azt mutatják, hogy a glikózaminoglikán intenzíven kiválasztódik oszteoblasztok területén mineralizáció, majd alávetjük lizoszomális enzimek, alkotó erősen ionok.
Az elsődleges embrionális kristályok nukleációjának biokémiai alapja a kollagén, az ATP, a Ca és a kondroitin-szulfát közötti komplex kialakulása. A kristályképződést szabályozó tényezők a kollagénrostokon is pirofoszfát, amely gátolja a mineralizációt. A foszfolipidek szerepe ebben a folyamatban is bizonyított, amely nélkül a csontszövet szerves mátrixa elveszti kalcifikálási képességét.
A csontszövetek korral összefüggő változásai és az alapbetegség.
Az ontogenetikai fejlődés folyamatában a csontszövet kimutatható szerkezeti és morfológiai és biokémiai változásokon esik át. Ebben történik a szerves komponensek tartalma és az ásványi összetevők növekedésének rendszeres csökkenése. Ezek a változások szorosan kapcsolódnak a mikrotápanyagok cseréjéhez. Sr, Pb, Si, A1 felhalmozódik, és a Cu koncentrációja csökken, a foszfor és a kalcium anyagcseréjének intenzitása tízszeresére csökken.
Az egyik vezető korral járó változásokat a csont - csontritkulás - progresszív szisztémás vázbetegség jellemző az alacsony csonttömeg, a csont szerkezete a jogsértés, növekedéséhez vezet a csont törékenysége és a törési kockázat.
-a menstruációs állapot megsértése (hosszan tartó másodlagos amenorrhoea, korai menopauza - akár 45 év, később a menstruáció);
-endokrin betegségek (primer hyperparathyreosis, tiretoxicosis, cukorbetegség, Cushing-szindróma);
-a vér betegségei (myeloma multiplex, szisztémás masto-
citozis, limfóma, leukémia);
-gyulladásos reumás betegségek (rheumatoid arthritis, dermatomyositis, szisztémás lupus erythematosus);
-az emésztőrendszer betegségei (malabszorpció, Crohn-betegség, krónikus májbetegség);
-krónikus veseelégtelenség;
-idegrendszeri betegségek.
I. Postmenopausalis osteoporosis (megfigyelést igényel 15 évig az elejétől
menopauza). A csontos gerendák elvékonyodnak, a frekvencia nő
a csigolyák és egyéb csonttörések.
P. Senile osteoporosis a 70 év feletti férfiak esetében jellemző.
III. Másodlagos osteoporosis - a szindróma glükokortikoid terápiájának hátterében
Cushing-szindróma, malazorpciós szindróma, étkezési rendellenességek, megnyúlt
Az osteoporosis megelőzése könnyebb, mint a gyógyulás. A gyógyszerek (kalcitonin, ösztrogének, kalcium, D-vitamin) csak a csontvesztés sebességét lassítják, de általában elvesztik csonttömegük helyreállítását.
Estrogének - a menopauza kialakulásának fontos eszköze a nők körében
Az osteoporosisban szenvedő betegek napi 1000-1500 mg-ot mutatnak (500 mg kalciummal együtt).