A víz-alkohol tisztítására használt aktivált aktív szén minőségének meghatározása
Péter I Aleksejevics (1672-1725) rendelete a vendég méltóságáról, a gyülekezeteken. Az edényeket mérsékelten fogyasztjuk, úgyhogy a has nem vesz nehéz táncot. Bájital, hogy bőven inni, a lábadat tartod: nem fognak inni. A hazugság nem hozza, hogy ne fojtson, még akkor sem, ha megkérdezte. Ugyanolyan dicsőséggel fojtogatva, mert az ősidők óta Oroszországban ez a halál becsületes.
A vodka és az alkoholtartalmú italok technológiája
Az aktív szén minősége meghatározása
Korábban [1] azt mutatja, a vizsgálatok eredményeit voltak tisztítás adszorpció aktív szén és etanollal szennyeződéseket úgy találta, hogy a meghatározása adszorpciós acetaldehid és izoamil-alkohol nem lehet a meghatározására szolgáló eljárás a minőségi szenet.
Feltételezve, hogy az alapján a hatásmechanizmusa aktív szén, amely javítja a vizes-alkoholos oldatokat nem onnye-adszorpciós, ioncserés és kemiszorpciós folyamatok, már átkerült a EK-tapadását szorpciós a savak és bázisok.
A szorpciós módszert a közelmúltban széles körben alkalmazták az ionok elektrolit oldatokból történő elnyelésére, valamint összetett elegyek szétválasztására.
Az ioncserélő szorpció kémiai reakció (ioncsere) alapul egy szorbens és egy oldat elektrolit között. A szorbensnek olyan ionogén csoportokkal kell rendelkeznie, amelyek képesek az átváltási reakcióra.
Az E.V. Trostyanskoy, I.P. Losev, A.S. A Tevlin [2] áttekintést nyújt a különböző iparágak különböző tanulmányaiban alkalmazott kationcserélő és elektro-cserélő gyantákról.
A kationcserélő szorpcióhoz a szorbensnek olyan savas csoportokkal kell rendelkeznie, amelyek hidrogénje könnyen cserélhető az oldatban lévő elektrolitkationra.
A szerves anyagok szuporpciója elsősorban a molekuláris szorpció típusától függ, kivéve, ha a szerves vegyület ionokat képezhet.
Savak és bázisok szuszpendálása aktív szénnel
Az erős elektrolitok adszorpciója a mechanizmusban élesen eltér a kissé disszociált anyagok és a nemelektrolitok adszorpciójától. Ebben az esetben helyesebb a kemiszorpciós folyamatról beszélni.
Az aktív szén, mint szorbens, visszafordíthatatlanul oxigénbe szorítja, amit az oxigén kémiai kölcsönhatása a szén felszínével magyaráz.
Shilov és munkatársai úgy vélik, hogy az oxigén és az aktív szén felületén való kölcsönhatásakor háromféle aktív szén keletkezik különböző körülmények között. Így egy szokásos hőmérsékleten és alacsony nyomásoknál egy olyan oxid képződik, amelynek bázikus jellege van, és vízzel való kölcsönhatás után ez az oxid egy bázist képez.
A hidroxilionokat, amelyek az aktív szén felületéről az oldatba kerülnek, a felület ellentétes töltései tartják, kettős elektromos réteget képeznek.
Frumkin úgy gondolja, hogy a szokásos hőmérsékleteken az oxigén kémiai kölcsönhatása a szén felületével nem következik be, és az oxigénnel egyensúlyban lévő szén oxigénelektródot képez.
Az adszorbeált oxigén "O-ionokat" küld, amelyek kölcsönhatásban vannak a vízmolekulákkal. Az OH-ionok kettős elektromos réteget alkotnak.
Úgy döntöttünk, hogy összehasonlítjuk a friss és használt szén kemiszorpciós képességét a savak és bázisok felszívódásának tanulmányozásával.
Lúgok és savak aktívszén-adszorpciója
A savak és bázisok adszorpcióját vizsgáló tanulmányok kimutatták, hogy az aktívszén alapú BAU kis adszorpciós kapacitással rendelkezik a bázisok tekintetében, és szignifikánsan magasabb a savakhoz viszonyítva.
Az aktív szén mintájának nátrium-hidroxid-oldat tíz perces érintkeztetése után ugyanaz a lúgadagolás mind friss, mind feldolgozott szénnel együtt jelentkezik. Például egy 100 mmol / l koncentrációjú alkáli koncentrációban a friss és aktivált szén adszorpciója után az egyensúlyi koncentráció 81 mmol / l volt. A hosszú távú adszorpció (24 óra) szintén nem mutatott különbséget az alkálifém felszívódásával friss és elhasznált aktív szénnel.
Az aktivált faanyag alkáli (BAU) kis adszorpciója a szénfelület alap jellegének következménye.
Shilov és Lepin [3] azt mutatta, hogy a szervetlen savak szorpciós képessége a következő sorrendben rendezhető:
Ismételten emelik a kutatás kimutatta, hogy SVE-faggyú-aktív szén adszorbeálja szignifikánsan jobb sav (ecetsav, kénsav és sósav), összehasonlítva a kipufogógáz és, hogy a sav adszorpciós aktivitása lehet elhelyezni a következő sorrendben:
A vizsgálatok eredményeit a 2. ábrán mutatjuk be. 1.
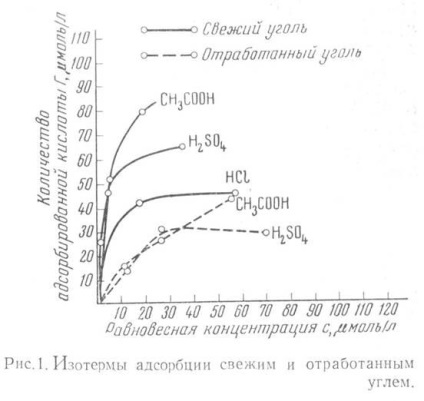
Ábra. 1. Adszorpciós izotermák friss és elhasznált aktív szén alkalmazásával.
Ugyanezek a vizsgálatok igazolják, hogy az aktív szén és a víz kétnapos kölcsönhatása gyakorlatilag nem csökkenti a savak adszorpciós képességét.
A nátrium-klorid adszorpciója gyakorlatilag ugyanolyan adszorpciót mutatott, mint a friss és elhasznált szén.
A víz elektromos vezetőképességének a szénnel való keveredés után bekövetkező változásának meghatározására vonatkozó tanulmányok jelentős különbséget mutattak a vizes oldatok elektromos vezetőképességében az all-yim és az elhasznált szén kezelésével.
Tehát 10 g friss szén és 100 ml víz 60 perces rázkódása után az oldat fajlagos elektromos vezetőképessége 1,4 * 10 -3 ohm-1 cm. és ugyanolyan mennyiségű szénhidrogént rázogatva # 955; 0 = 6,6 • 10 -5. azaz a víz elektromos vezetőképessége az aktivált szénnel való rázás után körülbelül 400-szor kevesebb, mint a víz elektromos vezetőképessége a friss szénnel való rázás után.
A friss szén szén-dioxiddal való keverése utáni vizes oldatok elektromos vezetőképessége nő a szén tömegének növekedésével, és az oldatok pH-ja 8-8,15 tartományba esik. A megmunkált aktív szén vízkivételeinek elektromos vezetőképessége csaknem változatlan marad a szénminta változásánál, és a megoldások pH-ja az 5,9-6,4 tartományban van. A mérések azt mutatták, hogy az ecetsav aldehid mennyisége 0,0025-0,01% tartományban nem befolyásolja az oldatok elektromos vezetőképességét.
Az elektromos vezetőképesség változásai nem mindig a táptalaj lúgosságának a következményei, ami minden valószínűség szerint a szén más elektrolitjainak átjutásával magyarázható.
Ily módon, amikor a lúgosság 4,8 és 6,0 (összege árok-millilit 0,01 N szükséges sav titráljuk 100 ml oldatban bromtimol kék indikátor), a fajlagos vezetőképesség-Elektroprom # 955; a = 2,4 • 10 -4.
Semleges és gyengén lúgos reakcióban (pH 7 - 7,2) a fajlagos elektromos vezetőképesség 1,0-1,3-10-4 tartományba esik. Így, az OP-elektromos vezetőképesség meghatározása A vizes oldatok (vízben keverés után a szén) lehet jellemezni a minőségi szenet, hanem azért, mert a szén-bejut megoldás nem csak az alap „, hanem a különböző elektro-Lites, amelynek összetétele nem állandó; Az oldat titrálásának módszere megbízhatóbb a vizsgált szén jellemzésére.
A fenti meghatározásokhoz a legjobb mutatót fel kell ismerni bromotimoliniumnak, amelynek színátmenete 6-7, G,
Amint azt Bauman [4] bizonyítja, a ioncserélő gyantának egy sóoldatba való átvitel során a pH-változás az ioncserélési folyamat bizonyítékaként szolgál. A jó minőségű aktív szén szintén növeli az oldatok pH-értékét, ami az ioncserélési reakciófolyamatnak köszönhető.
Végzett definíciónk pH sorba rendezi és vodkas azt mutatta, hogy szenek, így keverés közben vízzel lúgos reakciót vyzy-vayut is növeli a pH-ja vizes-alkoholos oldatok után kihagyás betétek őket a szén oszlopon m. E. PH vodka nagyobbnak kell lennie, mint az adott faj pH-ja; pH Capital és 40% rosszul sikerült vodkák magasabb a pH-féle és hogy a növekvő lúgos víz rázás után aktívszénnel pH növeli a különbséget a válogatás és a vodka (pH Moszkva különleges vodka alig különbözik a pH a válogatás, hiszen készítmény hozzá szódabikarbóna és ecetsav, hogy indokolja pufferelés hidroalkoholos RA-illesztéseket).
Így a meghatározás A pH, azaz a válogatás pH-ja és a vodka (a moszkvai speciális vodka kivételével) különbség lehet egy további kritérium a szén minőségének értékeléséhez.
Ahogy az "aktív szén" működik, a válogatási pH közelíti meg a víz pH-értékét, és a regenerálandó szén nem okoz változást a vodka pH-jában.
Feltételezhető, hogy a javulás a érzékszervi tulajdonságokat, de a víz-alkohol oldatok szűrés után aktív szénen, mint az azonos kapcsolódik a kemiszorpciós folyamat eltávolítása vagy megsemmisítése nem protein anyagok, amelyek vagy azok hidrolízis termékek, amelyek lehetnek az alkoholban nagyon kicsi koncentrációban.
Az ioncserélő reakció minden valószínűség szerint a szénfelszín oxidjai és a fehérjék aktív poláris csoportjai vagy ezek hidrolízistermékei között zajlik.
Az R. Block [5] részletesen megvizsgálja az aminosavak elválasztását az ioncserélő kromatográfia módszerével. Ugyanez a cikk azt jelzi, hogy Tzemus, Klasson és mások az aromás aminosavak szétválasztását aktivált szén alkalmazásával végezték.
A proteinek jelenlétét vagy hidrolízis termékek, például prolaminokat (gliadin, hordein) alkoholban lehet, amint azt a BM Chaguin [6], az eredmény a hiba tekercs fűtő cefre vagy hatása az elválasztó részecskék a cefre oszlop brazhnoy Epuration és elválasztó az alkohol a desztillációs oszlopok lemezei. BM Chagin [6] egy pozitív reakciót a fehérje (egy alkoholban) a feldolgozás a búza.
Az elvégzett kísérletek azt mutatták, hogy a szénen való szűrés előtt néhány víz-alkoholos oldat pozitív reakciót eredményezett ammóniával (Nessler-reagenssel).
Miután a víz-alkohol oldathoz hozzáadtuk a kálium-permanganát szénhidrogén oldatát a lúgos közegben, ez a reakció nem jelent meg.
Így a fő hatásmechanizmusa aktív szén-láb szén fokozó ízletesség hidroalkoholos oldatok, valószínűleg azzal magyarázható, ioncserélő folyamat újra-fellépés közötti oxid bevonattal, majd a felszínen a szén szennyeződések to-séta a hidroalkoholos oldatok.
Az aktivált szénfelszínen előforduló ioncserélési folyamatot a következő egyenlet ábrázolja:
-C-OH + MA = -C-A + MOH (1)
Ha a fehérje-anyagok hidrolíziséből származó termékek szennyeződésekként vannak jelen a víz-alkohol oldatban, akkor a csökkentett egyenletnek van forma
-C-OH + R-COOH = -C-COOH (2)
Hiányában az aktivált szén az oxid típusú bevonatok felületén:
a szén nem képes ioncserélő reakcióra, ezért a vízkivonatnak nincs lúgos reakciója.
A reakció alkálikus vizes kivonat lehet azzal a ténnyel magyarázható, hogy együtt a ioncserélő reakció között fellépő felületi az aktív szén és a szennyeződések vannak regia (például nitrogén vegyületeket fehérje eredetű) fordul elő ionoob-menny folyamat közötti szén-oxid bevonatok és oldott sók KORMÁNYZATI vizes-alkoholos oldatban (előállítására válogatás), ami szintén képződéséhez vezet a bázis.
Tehát a szén aktivitásának meghatározására javasolt módszert az aktivált szén oxidmentes bevonatának meghatározására redukálják
Ezen vizsgálatok alapján egy eljárást szolgáltatunk értékelésére minő-CIÓ az alkalmazott aktív szén tisztítására a víz-alkohol oldatok, meghatározzuk a lúgos a víz extrakció után a vizsgálati szén.
Azt tapasztaltuk, hogy amikor az aktív szenet vízzel keverjük, a közeg reakciója semleges vagy enyhén savas lesz. A vízben rázott, jó minőségű aktív aktív szén lúgos reakciót eredményez. Így a szén lerakódása után a víz alkalinitásának mértéke szolgálhat a tisztításhoz használt szén minõségének mérésére.
A szénminőség értékelése a következő.
Egy átlagos minta aktív szén került kiválasztásra a szén- oszlopban, a kissé-kezelés nyomja meg közötti szűrőpapírt, alaposan összekevertük, és vayut-műszaki léptékű bemérünk 30 g szén.
A szén mintáját rázógépen vagy kézzel 10 percig 150 ml vízzel rázatjuk. A rázás végén a faszenet egy szokásos papírszűrőn szűrjük. A kapott szűrlet 100 ml-éhez indikátorként 5 csepp bróm-timolint (0,1 g / 100 ml 20% -os alkohol) adunk hozzá.
Ha a szűrletnek savas reakciója van, akkor az oldat sárga színűvé válik. Lúgos reakcióban az oldat kékre válik. A szűrlet 100 ml-ét titráljuk 0,01 N kénsav vagy sósav oldattal (indikátor - 5 csepp bróm-timol-zin).
A széntartalmat regenerálni kell, ha kevesebb mint 0,2 ml 0,01 N sav oldatot használunk 100 ml szűrlet titrálásához, vagyis a közeg szinte semleges reakcióját.
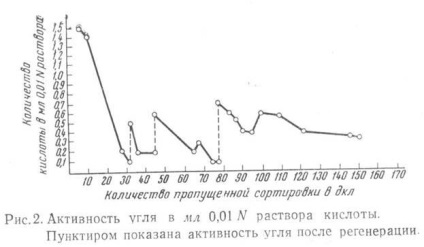
Ábra. 2. A szén aktivitása ml-ben 0,01 N savas oldat. A szaggatott vonal a regeneráció után a szén aktivitását mutatja.
A titrálás végét az oldat kék színének zöld színű, gyenge sárga árnyalattal történő átmenetével határozzák meg (a színátmenet pillanatát meg kell jegyezni).
A regenerálásnak alávetett szén minőségét a szenet válogatással, az úgynevezett "gazdasággal" történő mosás után határozták meg.
Amint a vizsgálat, a minőség a friss szén-fúj alábbiak meghatározása a következő: 200 g friss szén 1 liter desztillált vízben, majd 2 Chasa üríteni és újra öntjük szenet 1 liter vizet. Két órás infúzió után a vizet leeresztettük, és a szénmintát a fent leírt módon préseltük. Technikai méretekben 30 g vizsgálati szenet mérünk és rázzuk 150 ml desztillált vízzel. A szűrlet 100 ml-ét 0,01 N savas oldattal titráljuk indikátor jelenlétében (5 csepp bróm-timol-zin); a titráláshoz legalább 2 ml 0,01 N savas oldatot kell elfogyasztani.
Az aktívszén minőségét, mind friss, mind pedig az oszlopokban talált értékeket két párhuzamos meghatározás alapján végezzük.
A táblázatban és a 3. ábrán. A 2. ábra a moszkvai szeszesital egyik szénoszlopában lévő szén minőségi vizsgálatának eredményeit mutatja.
A kihagyott válogatás száma dl
A kidolgozott módszer már tesztelték, és végre a Moszkva, In-ronezhskom és más lepárló, és benne van a kézi vezérlés tehnohimncheskomu lepárló [7].
1. M.S. Shulman, A.N. Babkov, Az etil-alkohol aktivált szénnel aktivált szennyeződéseinek adszorpciója, Trudy TsNIISP, Vol. IX, 1960.
2. E.V. Trostyanskaya, I.P. Losev, A.S. Tevlin, "A kémia sikere", XXIV. 1, 1955, 69.
3. Shilov és Lepin, elektrolitok és molekuláris erők adszorpciója.
4. V. Bauman, kationcserélő gyanták, sz. "Ion Exchange", IL, 1951.
5. R. blokk, aminosavak elválasztása ioncserés kromatográfiás eljárással, sz. "Ion Exchange", IL, 1951.
6. B.M. Chagin, "Spirits Industry", 1954, No. 2.
7. Az alkoholtartalmú italok gyártásának technokémiai ellenőrzéséről szóló utasítás, 1960.
8. Ma beszélünk Ruslan Braginnal, a "Rodionov with Sons" társaság marketingigazgatójával az orosz alkohol történelméről, pontosabban az orosz vodka történelméről.