A termék kimenete az egyensúly - a vegyész útmutatója 21
Általában, amikor szükség van, hogy értékelje a reakció termodinamikai és kinetikai kapcsolat, helyes, hogy először a pozíció az egyensúly és a függés a külső körülmények (hőmérséklet, nyomás), és csak figyelembe véve ezeket az adatokat, hogy vizsgálja meg a kinetikai paraméterek a folyamat. Előzmények Az előző évek art több példát, hogyan lehet eldönteni, hogy szükség van előzetes elhanyagolása egyensúlyi arányokat eredményez szükségtelen költségeket a munkaerő és anyagok, valamint időveszteséget, mint például a hosszú keresés aktívabb katalizátorok körülmények között, ahol az alacsony hozam a termék B-nak okoz kedvezőtlen egyensúlyi helyzet. [C.13]
A reakciótermékek egyensúlyi kitermelését 2,0 10 Pa nyomáson számoljuk. [C.327]
Számítsuk ki a 2-metil-bután dehidrogénezési reakciójából származó termékek egyensúlyi kitermelését izoprénben 7 = 300-900 K tartományban. A reakció egy szekvenciális séma szerint [c. 279]
Határozzuk meg a reakcióban résztvevő valamennyi anyag aktivitási együtthatóit, 2,0-10 Pa nyomáson és a reakciótermékek maximális hozamának hőmérsékletén. ha az egyensúlyi nyomás 1,0133-10 Pa. [C.346]
Az ipari folyamatok fontos technológiai indikátorai a termék egyensúlyi hozamai, az egyensúlyi viszonyok az adott körülmények között és a termék tényleges hozama (hatékonyság), mind az egyensúly, mind a folyamat sebessége alapján. [C.153]
A fő technológiai paraméter - a tényleges hozam, illetve a hatékonyság a gép -... definiáljuk tényleges tömege újrahasznosított otnoschenie az alkatrész az egyensúlyi Cp, azaz, azt mutatja, milyen mértékben megközelítés egyensúlyi [c.156] ..
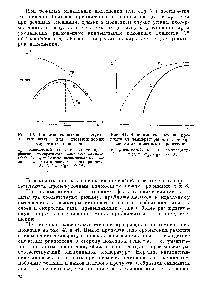
Chatelea, ha a rendszer kémiai egyensúlyi állapotban van. van egy külső hatás. Az egyensúlyi helyzetet olyan módon tolják át, hogy ellensúlyozzák e hatás hatását. Ha az egyensúlyi kémiai rendszer közvetlen reakciója exoterm, akkor a növekvő hőmérséklet csökken, ha a közvetlen reakció endoterm, majd növekvő hőmérséklet mellett a Kravn növekszik. A termékek egyensúlyi hozamát növelni lehet úgy, hogy a hőmérsékletet csak a reakció hővel történő felszívódása esetén emeljük. Annak érdekében, hogy ne tévedjünk, mindig feltétlenül meg kell jegyeznünk az egyenletet teljes egészében, figyelembe véve a termikus hatást, mintha a reakció egyik terméke lenne [c.191]
Apropó optimális arányát a reagensek, akkor kell figyelni, hogy a következő, ha az áramlási sebesség egyikük az egyik vagy másik ok miatt korlátozott, a koncentráció növekedése a ko-reagensek növeli használatának mértékére ez lesz a nagyobb, annál fel a többi reagens. Meg kell jegyezni, nem csak a kapcsolódó nehézségek eltávolítása az egyensúlyi elegyben neiroreagirovavshego fölös reagens, hanem az a tény, hogy a sztöchiometrikus keveréke szükséges, hogy megkapjuk a maximális hozam a reakció termékek. [C.82]
A hidrokrakkoló termékek hozamainak arányát az 1B karbóniumion izomerizációjának arányával, azok bomlásával és stabilizálásával határozzuk meg. Mivel a karbóniumionok bomlik a fragmensek hasadásával. kevesebb, mint 3 szénatomot tartalmaz, nagyon endoterm, és a hidrokrakkolási folyamatok alacsonyak, a metán és az etán szinte nem alakul ki. A nagy savakkal és mérsékelt hidrogénezési aktivitással rendelkező katalizátorra a karbóniumionok telítettségére vonatkoznak. amely sok szénatomot tartalmaz és gyorsan romlik, kis mértékben fordul elő, ezért az izobután hozama magas, és az eredeti n-1 paraffin izomerjeinek hozama elhanyagolható. A karbóniumionok egyenlő dimenziós izomerizációjának mértéke növekszik a bomlás és a későbbi stabilizálás során keletkező szénatomok számának növekedésével, ezért a paraffinok a termodinamikai egyensúlyi foknál nagyobb mértékben izomerizálódnak. Magas hidrogénezéssel és mérsékelt savas aktivitással rendelkező katalizátoroknál karbóniumionok intenzív telítődése következik be. Ennek eredményeként a molekulában nagyszámú szénatomot tartalmazó paraffinok képződnek, és az izoparaffinok n-paraffinok aránya a krakkolási termékekben kicsi. [C.275]