A lítiumvegyületek érccentrátumokból történő előállításának technológiája
A lítium-koncentrátumok feldolgozási termékei lítiumsók (karbonát, szulfát, klorid) és hidroxid. A leggyakoribb végtermék lítium-karbonát, amely kiindulási anyagként szolgál más vegyületek, különösen lítium-klorid előállítására, amelyből lítium-fém keletkezik.
Az ipari gyakorlatban elsősorban a lítiumkoncentrátumok bomlási módszereit alkalmazzák: kénsav, szulfát (K2S04-vel történő szinterelés) és meszes. Ezenkívül a mészkloridos módszert néha használják.
A kénsavval történő bomlást mindenféle lítiumkoncentrátumra alkalmazzák: spodumén, lepidolit és amblygonit. A koncentrátum tömény kénsavval 200-250 ° C-on történő bomlása és a termék vízzel való utána történő kioldódása következtében lítium-szulfátot tartalmazó oldatok keletkeznek, amelyekből lítium-karbonát kicsapódik.
Spodumena feldolgozása. A hatékony lebontás Spodumene kénsav szükséges kezdeti ter-dasági feldolgozási ez körülbelül 1100 ° C-on való átalakítására-TION - egy / 3-Spodumene (a - Spodumene alig lebontó etsya kénsavat.). A tüzelést egy dobkemencében végezzük. Feature kölcsönhatás kénsav / 3- Spodumene áll a csere a lítium-kationok által protonok savas megtartva a szerkezet / 3-Spodumene:
Li20 • A1203 • 4Si02 + H2S04 Li2S04 + N20 *
* A1203 • 4Si02. (10.1)
Mivel a szilícium és alumínium ugyanaz a rács alumínium-szilikát marad, a lítiumot szelektíven kivonjuk egy vizes oldatba, ami ezért viszonylag kevés szennyeződést tartalmaz.
A koncentrátumot és a kénsavat összekeverjük egy csavarban, amely az elegyet egy dobkemencébe (acél nem tartalmazó dob) adagolja, ahol 250 ° C-on a szulfatizálás gyorsan (10-15 perc) következik be.
A szulfatált anyagot vízzel leöblítjük, a krétát a reaktorba tápláljuk, hogy a felesleges kénsavat semlegesítsük (legfeljebb 6 + 6,5). A szűrt oldatot magnéziummal tisztítjuk meszes (pH = 12 + 14) semlegesítéssel, majd kalciummal CaCO3 szódával történő kicsapással.
A vas- és alumínium-oxidok hidroxidok pH-ja 7-ben képződő szennyeződései, miközben az oldatot egyidejűleg 200 g / l Li2S04 koncentrációra párologtatják.
A csapadékot szűréssel elkülönítjük, lítium-karbonátot kicsapunk az oldatból telített nátrium-hidroxid-oldattal. A mosott üledékek 96-97% Li2C03-ot tartalmaznak. A spodumén koncentrátumból származó karbonátba történő visszanyerés 85-90%.
A lepidolit feldolgozása. A lepidolit közvetlenül kénsavval szulfatálható 320-330 ° C-on. A folyamat felgyorsítása érdekében a lepidolite előzetes leolvasztását néha 1090 ° C-on alkalmazzuk, üvegszerű anyagként, amelyet köszörülés után szulfatálnak.
A lepidolit feldolgozása során kapott kénsavas oldatok Li2S04, K2S04, Na2S04, Al2 (S04) 3-at tartalmaznak.
Az alumínium legtöbb részét általában kálium-alumínium K [A1 (S04) 2] 12H20 formájában izoláljuk, az oldatokat -5 ° C-ra hűtjük
0 ° C-on (kálium-szulfátot adunk az oldathoz). Ezenkívül alumíniumot nyerünk a semlegesített oldatból az A1 (OH) 3 kompozícióban. Az oldat következő bepárlása során K2S04 és Na2S04 részei kristályosodnak. A lítium-karbonát kicsapódik a szűrt oldatból.
Az eljárás a lítium-koncentrátumok kálium-szulfáttal történő szinterezésén alapul, majd a szinterelő vízzel való leöblítésével.
A spoduménnek a szinterelési folyamatban 920-11150 ° C-on végzett feldolgozásakor az a-spodumént β-spoduménré alakítják át, amely kálium-szulfáttal való reakciót vált ki:
2 (Li, Na) [Al (Si03) 2] + K2S04 2 (K, Na) [Al (Si03) 2] + U2S04. (U-2)
Hűtés közben az a-leucit átjut a β-leucitbe. Az átmenet a * # 9632; / 3-spodumén elősegíti a szilárd adalékolású fázisreakció gyors fejlődését, mivel a rácsatomok átrendeződése megnövelt mobilitást eredményez.
Mivel a reakció (10.2) reverzibilis, nagy mennyiségű K2S04
Az 1. ábrán. A 80. ábrán a spodumén szulfátos eljárással történő feldolgozására jellemző séma látható.
A töltés zsugorítják rotációs kemencékben 1100 - 1150 ° C, 1 - 2 óra. A kimosódás végezzük a hideg dobos malmok (Li2S04 oldhatósága csökken, rózsa-sheniem hőmérséklet).
A szulfátos folyadékok 110-150 g / l Li2S04, 150 -
200 g / l K2S04, jelentős mennyiségű Na2S04 szennyeződés
Keverés és csiszolás Cnenatfue
(Átalakítás K2SO4 és pi a dump)
(Na2C03j oldat készítéséhez
80. ábra. A spodumén kálium-szulfáttal való szintereléssel történő feldolgozásának technológiai terve
Szulfátok Mg, Al, Fe. Ezeket a szennyeződéseket hidroxidok formájában kicsapjuk nátrium-hidroxiddal vagy kálium-karbonáttal. A lítium-karbonáttal felszabaduló oldatok későbbi feldolgozását számos lehetőség felhasználásával végezzük. Ezek közül az egyik az 1. ábrán látható. 80. Ebben a kiviteli alakban, egy nagy mennyiségű kálium-sul fátyol kristályosítással izoláljuk 3K2S04 kettős só - Na2S04 (glaserite) előállítására alkalmazott szakaszos Spodumene a K2S04.
A szulfatált módszert is használják, feldolgozására les pidolita tsinnvaldita és a különbség csak egy adag sul fátylat a kálium a töltés és alacsonyabb, mint a szinterezési hőmérséklet (850 - - 950 ° C).
A lítium nyersanyagok feldolgozásának szulfátos eljárásának előnyei közé tartozik a sokoldalúság és a koncentrátum nagyfokú disszekciója. A hátrány a kálium-szulfát magas fogyasztása. Mindazonáltal a K2S04 nagyfokú regenerálódását biztosító megoldások feldolgozásának racionálisabb rendszereinek létrehozása jelentősen javítja a folyamat gazdaságosságát.
A lime-eljárás lítium-koncentrátumok (spodumén vagy lepidolite) szinterelését jelenti lime vagy krétával. A torta vizes vízzel történő lemosásával lítium-hidroxidot tartalmazó oldatot kapunk, amely kristályosodik az oldat LiOH-H20-monohidrát bepárlásából.
Tekintsük a folyamat alapjait a spodumén példáján. A spodumén mész (vagy kréta) 1150-1200 ° C hőmérsékletű kemencében történő lerakódása esetén lítium-aluminát és kalcium-szilikát képződik:
Li20 • A1203 • 4Si02 + 8CaO =
= Li20 • A1203 + 4 (2CaO • Si02). (10.3)
Ha a tortát vízzel mossuk fel, a lítium-aluminát reagál Ca (OH) 2-gyel lítium-hidroxid előállítására:
Li20 • АІ2Оетв) + Са (ОН) 2 (radioaktivitás) = 2БІОН (раств) + СаО • А12Оэтв). (Yu.4)
A szinterben lévő kálium- és nátriumtartalmú aluminátok Ca (OH) 2-gyel reagálnak, KOH és NaOH keletkeznek. Lítium-hidroxid LiOH • HjO-ot az oldatokból vákuumban bepárlással kristályosítjuk. A párologtatást több lépésben végezzük. A LiOH koncentrációjú oldatokból
160 g / l hűtés után LiOH-H20-kristályokat különítünk el, amelyeket centrifugálással elválasztunk az anyalúgtól. Az anyalúgot visszavezetjük a párolgásig. A szennyeződések felhalmozódásakor az anyalúgokat rendszeresen eltávolítják a ciklusból, és regenerálódnak.
Ha szükséges, az LiOH-H20-kristályokat átkristályosítással tisztítjuk, feloldódással tisztított vízzel. A vízmentes lítium-hidroxid előállításához a monohidrátot 600- 650 ° C-on dehidratáljuk.
A lime-eljárást a lepidolitikus koncentrátumok feldolgozásánál is alkalmazzák. A spoduménnel ellentétben a lepidolit mész (vagy kréta) szintetizálása alacsonyabb hőmérsékleten (900-950 ° C) történik.
Az előnyök a módszer tartalmazza mész annak alkalmazhatóságát, hogy bármilyen típusú lítium koncentrátumok közvetlen előállítására lítium-hidroxid, olcsóság rea Gent, a hulladék termékek (salakok tartalmaznak - tartalmazó szilikátok és kalcium-aluminát) előállítására Kötött-cementkötésű építőanyagok, valamint a az alkoholtartalmú káliumsók lehetőségét.
Azonban a módszer súlyos hátrányokkal jár. Ez előnyösen alkalmazható lítium gazdag koncentrátumok, azonban ebben az esetben, extrakcióval a kész termék nem haladja meg a 70%, mivel a korlátozott rastvorimos Tew lítium-hidroxid, és a képességét, iszapok után vyschela Chivanov-beállítható. Egy másik hátránya - a szükségességét elpárolgása nagy mennyiségű folyadékot.
Tiszta lítium-klorid előkészítése
0,1; Si02 0,05; 0,005. 336
E tisztaságú lítium-klorid előállításához rendszerint szükséges tisztítani a lítium-karbonátot szennyeződésektől. A tisztítást jól oldódó lítium-hidrogén-karbonáton (Trist módszer) átkristályosítjuk. E célból a C02 vizes Li2C03-szuszpenzióján keresztül vezet, amely lítiumot LiHC03-bikarbonát-oldatba való átmenetéhez vezet.
Amikor az oldatot forraljuk, a bikarbonátot elpusztítjuk a folyóból. Az Asc-ot kicsapjuk tisztított Li2C03-tal.
A lítium-klorid-nedves-karbonát-oldattal oldjuk, 30% -os sósavat. Az oldatot tisztítjuk ion szennyező SOJ „VaS12 mellett. Ezután eltávolítására egyéb szennyezések, az oldatot hozzáadásával semlegesítjük LiOH előtt az alkáli-Ness 0,01n. Forráspont kiosztott hidroxidok, karbo-Nata vagy bázisos kalcium-só szennyeződései, bárium, magnézium és vas.
A tisztított oldatot 350-360 g / l koncentrációjú LiCl koncentrációval bepároljuk. A párolgás és a klorid dehidratálásának nehézségei a LiCl és az oldat magas korróziós kapacitásának tulajdoníthatók. A párolgás érdekében kerámiából vagy speciális ötvözetből készült készülékeket használnak, és a klorid dehidratálásához kerámia készüléket használnak. A párolgás eredményeképpen a klorid LiClH20 kristályosodik. A kloridot ezután 120-150 ° C-on dehidratáljuk.
3. A LITIUM TERMELÉS TECHNOLÓGIÁJA
Lítium termelés elektrolízissel
Az oxigénhez és a halogénhez nagy affinitás miatt a lítium előállítható olvasztott közeg elektrolízisével vagy lítium-desztillációval fém-termikus redukcióval.
Elektrolízis hajtjuk végre egy elektrolit aránnyal LiCl: KC1 = 1: 1 (tömeg), amely közel áll a készítmény ev tektiki a LiCl Rendszer - KC1, amelynek olvadáspontja 361 ° C-on Ez lehetővé teszi az elektrolízist 400-460 ° C-on.
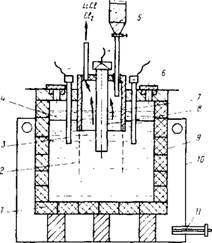
Az 1. ábrán. A 81. ábra egy olyan elektrolizátor vázlatos rajza, amelyben két katódos tér van elrendezve diafragmákkal az anódterülettől. A kádak acél burkolatát grafittal bélelik, a legstabilabb anyagot a lítium-klorid tekintetében. Azonban a grafit
Rіs.81. Az elektrolitikus cella fém lítium előállítására: 1 - grafit bélés; 2 - membrán a vasrácsból; 3 - acél katódok; 4 - folyékony levél; 5 - sótöltő só; 6 - lyuk a folyékony lítium leválasztására; 7 - membrán; 8 - grafit anód; 9 - acél fürdőkabát; 10 - kamra a kád felmelegítésére; 11 - gázégő
Tvuet Li2C2 lítium-karbid képződésével, az elektrolitban széndioxid felbomlásával. A grafit bélés és az anódok az ipari fürdőkben körülbelül három hónapig dolgoznak. A magasabb tisztaság fém lítium zlektolizery használt vízhűtéses falakkal, amely képződik a megszilárdult garnissazh sók Védő-forgó-elektrolit reakciót egy fém fal.
Az elektrolit megolvasztásához külső fűtést lehet használni, akkor a hőszabályozást a felszabaduló hő tartja fenn, amikor az áram folyik az elektroliton.
A lemezek kis széntartalmú acélból készülnek, az anódok grafit rudak. A LiCl és KC1 bomlási potenciáljai az eutektikus összetétel elektrolitjában 400 ° C-on 3,78 és 3,89 V, ami kálium részleges felszabadulását eredményezi a katódon.
Az elektrolízist 400-430 ° C-on végezzük, a katódon áramlási sűrűséggel és 2,0-5,0 és 0,8-1,5 A / cm2 anóddal. Az aktuális kimenet 90-93% -ot ér el. A katódon felbukkanó folyékony lítium lebeg az elektrolit felületére, és felhalmozódik egy vas-hálós kanállal. A fém oxidálódik egy vékony film sóktól, amely hidratálja a folyékony lítiumot.
Az anód térből származó klórt az abszorberbe töltjük, mésztejzel öntözve.
A lítium mellett elektrolízissel lítiumötvözeteket más fémekkel (kalcium, magnézium, nehézfémek) is lehet előállítani. Ehhez be kell vezetni a megfelelő fém kloridot az elektrolitba, vagy elektrolízist kell végrehajtani egy oldható anóddal a fémből, az ötvözött komponens lítiummal.
Lítium termelés vákuum-kémiai módszerekkel
A lítium megszerzéséhez szükséges elektrolitikus módszer bizonyos hátrányokkal jár: a kezdeti lítium-klorid viszonylag drága. A lítium, a kálium és a nátrium lítiációs potenciál közelsége miatt az elektrolitikus lítium észrevehető mennyiségű kálium- és nátrium-szennyeződést tartalmaz, ami további tisztítást igényel. Az anódon felszabaduló klórt fel kell használni vagy fel kell használni. Ebben a vonatkozásban a lítium-oxid, a monoaluminát (Li20A1203), valamint a spoduménből közvetlenül leválasztott vákuum-termikus módszerek víztisztító módszerek kifejlesztésére került sor.
Lítium-oxid visszanyerése. A lítium-oxidot lítium-karbonát termikus bomlásával nyerik. 810, 890 és 1270 ° C hőmérsékleten a lítium-karbonát feletti CO2-nyomás 2; 4,3 és 101 kPa (15, 32 és 760 Hgmm). Ez bomlása során lítium-karbonát nem fordult elő az olvadási (olvadáspont Li2C03 735 ° C-on), ami nehezen eltávolítása C02, lítium-oxid kapott proc-vaniem Li2C03 brikettezzük keverék és CaO (ha a kapcsolat-SRI 1: 1,5 tömeg) a 850 ° C-on vákuumban (a reakció eljuttatása a C02 felszabadulás oldalához). Ennek eredményeként Li20 és CaO elegyét kapjuk. Az utóbbi, az alábbiak szerint, a töltés hasznos összetevője.
Lítium-oxid hozzáférhető redukálószerént porított szilíciumot adunk hozzá:
2Li20 + Si = Si02 + 4Li (10,5)
Standard körülmények között a (10.5) reakciót a Gibbs-energia pozitív változása jellemzi, és dermetikus:
DS »8K = 298 kJ, ДЯ ° 298К = 320 kJ.
Következésképpen a reakció (10,5) magas hőmérsékleten folytatható vákuumban, a reakciógömbön lévõ gázlítium desztillációjával. Mindazonáltal ilyen körülmények között a lítium-oktid egy része ortosilikátra van kötve:
4Li20 + Si = 4Li (ra3) + Li4SiQ4. (10.6)
A kiindulási töltetben jelen lévő kalcium-oxid megakadályozza ezt a reakciót úgy, hogy a Si02-t a kalcium-ortoszilikáthoz köti:
Li4Si04 + Si + 4CaO = 4Li (ra3) + 2Ca2Si04; (YU.7)
Д ^ іооок = -351 КДж.
Kalcinált keveréket lítium és kalcium-zúzott, oldjuk, keverés szilícium por (10% felesleg számítva elleni CO-lichestva) és pellet az így kapott reakcióelegyet vákuumban kemencében 1000-1300 ° C, a nyomás pedig 0,113 Pa a kemencében. A lítiumot kondenzátorban gyűjtjük össze. A lítium hozama 1000 ° C-on 75%, 1300 ° C-on - 93% -ig. A fő szennyeződések: 0,04% Ca és 0,01% Si.
Lítium-aluminát visszanyerése. A nagy tisztaságú lítium 95-98% -os kitermeléssel előállítható lítium-mono-lítium-alumínium redukálásával vákuumban, 1150-1200 ° C-on. A lítium-aluminátot Li2C03 és A1203 keverékének kalcinálása útján állítjuk elő.
A helyreállítás a reakció szerint folytatódik:
3 (Li20-A1203) + 2A1 = 6Li (ra3) + 4Al203. (Yu.8)
Az egyensúlyi lítium nyomása 1100 ° C-os hőmérsékleten 33,3 Pa. Következésképpen a redukciót 1200 ° C-on és körülbelül 13,3 Pa nyomáson végezzük. A magas lítiumvisszanyerés érdekében felesleges alumíniumot használnak. A lítium-aluminát csökkentése nem igényel kalcium-oxidot a töltetbe, ami biztosítja a nagyobb tisztaságú fém előállítását.
A kapott alumínium-oxidot lítium-aluminát előállítására használják.
Tisztítás céljából a mechanikai szennyeződésektől lítiumot alkalmaztunk, és megolvasztjuk ülepítéssel réteg vazelint vagy para finnek olajat, és szűrjük a folyékony lítium szitán szűrők vagy huzal, vas, titán vagy molibdén. A porított vagy szivacsos titán és a cirkónium, az urán szolgálhat mosogatók az oxigén és nitrogén a megolvadt lítium. Ezek a fémek gyakorlatilag nem oldódnak lítiumban.
A más alkálifémektől való tisztítást a hidridek hőstabilitásának különbsége alapján végezzük. A LiH, KH és NaH hidridek disszociációs nyomása eléri a 0,1 MPa-t (1 érték) 850, 427 és 420 ° C-on. A lítium-hidrid olvadáspontja 688 ° C. Ha a lítiumot 700-800 ° C-on hidrogéngázzal melegítjük, a kálium és nátrium elpárolog, és LiH marad, amelyet vákuumban végzett melegítéssel elbontunk. A magasan szennyezett lítium például a spodumén kinyerésével nyerhető elektrolitikus finomítással tisztítható.
A lítium finomításának vákuumban való lepárlási módszere hatékony. Először 450 ° C-on az alkálifém (kálium, nátrium) szennyeződésének fő mennyiségét ledesztilláljuk. A lítiumot ezután 600-800 ° C-on bepároljuk 1,3 x 10 -3 Pa nyomáson
Biztonsági intézkedések, lítium csomagolás és tárolás
A lítium megolvasztása és öntése a levegőben meggyulladhat. A megvilágított fém ajánlott töltse sous-kémiai nátrium-klorid, lítium-klorid, szóda (nem Bikar-Bonate) vagy egy keverék, amely egy semleges por (Gras-fit, nátrium-klorid), 10-20% viszkózus szerves anyagok (gyantával kevert polietilén) és a sztearátok és a talkum adalékanyagai. A lítiumot gömböcskék, granulák, rudak, huzalok formájában állítják elő. Lítium tárolni egy zárt tartályban réteg alatt vas pépes masszát a viasz és a bánya-ásványolajban vagy benzin vagy petróleum-éter, amely a tartály töltési tetején. A lítium ásványi olajat kőolaj-éterrel vagy benzollal mossuk, majd vákuumban bepároljuk. Kényelmesen tárolja a lítium, zapressovyvaya azt zárt vékonyfalú cső alakú réz vagy alumínium héj, amelyből azután a kívánt darabokat lehet vágni lítium.