Alkoholok szerkezet, izoméria, tulajdonságokra és példákra
Alkoholok - vegyület, amely egy vagy több hidroxilcsoporttal -OH, társított szénhidrogéncsoport.
Attól függően, hogy a hidroxilcsoportok száma az alkoholok vannak osztva mono- (CH3 OH - metanol, 2 H5 OH - etanol), di- (CH 2 (OH) -CH 2-OH - etilén-glikol) és háromértékű (CH 2 (OH) -CH (OH) -CH2-OH - glicerin). Attól függően, hogy, ahol a szénatom jelentése hidroxilcsoport, különbséget tenni az elsődleges (R-CH2-OH), szekunder (R2 CH-OH) és tercier alkoholokat (R3 C-OH). A cím alkohol van jelen utótag - ol.
monoalkoholok
Az általános képlet a homológ sorozat telített egyértékű alkoholok CnH2n + 1 OH.
Ha korlátozni monoalkoholok jellemezve izoméria szénváz (kezdve butanol), és a pozicionális izomerek a hidroxil-csoport (mivel propanol) és Interclass izoméria éterekkel.
fizikai tulajdonságok
Alsó alkoholok (akár C15) - folyékony, magasabb - szilárd anyagok. A metanolt és etanolt elkeverünk vízzel bármilyen arányban. A növekvő molekulatömegű alkoholokat ODE oldhatósága csökken. Alkoholok van egy magas forráspontú hőmérséklet és olvadási képződése miatt a hidrogén kötések.
A kapott alkoholt
Alkoholok előállítását esetleg biotechnológiai úton (fermentációs) eljárással, fa vagy cukor.
A laboratóriumi módszerek előállítására alkoholok közé tartoznak:
- alkéneket hidratációs (reakciót melegítés közben, és jelenlétében tömény kénsav)
- hidrolízise alkil-halogenidek által a kereset vizes oldatainak lúgok
CH3 Br + NaOH → CH3 OH + NaBr
- karbonil-vegyületek redukálása
kémiai tulajdonságok
1. A reakciót előforduló a törés a O-H:
- savas tulajdonságai alkoholok nagyon gyenge. Alkoholok reagálnak az alkálifémek
de nem reagál lúgok. Jelenlétében teljesen hidrolizáit alkoxidok víz:
Ez azt jelenti, hogy a alkoholokat - gyengébb savak, mint a víz
- észterek képzése által elő ásványi vagy szerves savakkal:
- Alkoholok oxidálására hatására kálium-permanganát vagy dikromát a karbonilvegyületek. Primer alkoholokat oxidáljuk, hogy aldehidek, amely viszont lehet oxidálva karbonsavak.
R-CH2-OH + [O] → R-CH = O + [O] → R-COOH
Szekunder alkoholok oxidált ketonok:
R-CH (OH) -R '+ [O] → R-C (R') = O
A tercier alkoholok, jobban ellenáll az oxidációval.
2. A válasz a törés a C-O.
- intramolekuláris kiszáradás alkotnak alkének (erős melegítés történik alkoholok dehidratáló anyag (koncentrált kénsav)):
- intermolekuláris dehidratálásával alkoholok alkotnak éterek (előforduló alacsony hő dehidratáló anyagok alkoholok (koncentrált kénsav)):
- gyengén bázikus tulajdonságait alkoholok látható reverzibilis reakciók hidrogén-halogenidekkel:
Példák problémák megoldása
Határozza meg a moláris tömege és szerkezete az alkohol, ha ismeretes, hogy a 1,12 l felszabadított gáz a reakció során 7,4 g fenti alkohol fém-nátrium (STP), és az oxidációs réz-oxid (II) vegyület keletkezik, amely reakció " ezüst tükör. "
Alkotunk az egyenlet ROH alkohollal reakciókat: a) nátrium; b) egy oxidálószerrel CuO:
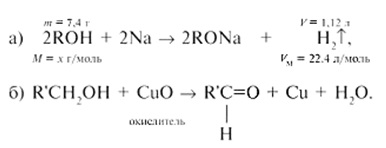
Egyenlet (a) meghatározza a kapcsolat által moltömegére ismeretlen szellem:
Az ilyen alkoholok móltömege C4 H10 O. szerint továbbá a feltétele a probléma [egyenletet (b)], ez lehet primer alkoholok - 1-butanol CH3 CH2 CH2 CH2 OH vagy 2-metil-propanol-1 (CH 3) 2 OH SNSN2.
M (C4 H10 O) = 74 g / mol, 1-butanol vagy 2-metil-propanol-1