Molekuláris felszíni víz tulajdonságai studopediya
„- porózus közeg folyadék” rendszer
Ahhoz, hogy megértsük részletesen folyamatokban fizikai és kémiai kölcsönhatás diszperziók és diszperziós közeg még részletesen a víz szerkezetét.
A vízmolekula ismert, hogy képviseli két egyértékű ionok és hidrogén-ion, egy kétértékű oxigén. A víz molekula nem energetikailag semleges. Ez azért van, mert a hidrogénatomok az oxigénatommal szomszédos egy és ugyanazon az oldalon, ami az esemény a villamos pillanatban. Más források szerint az oxigén és a hidrogén ionokat a vízmolekulák csúcsainál helyezkednek el egy egyenlő szárú háromszög, és az a szög, a háromszög csúcsa, elfoglalt oxigén ion 105 °.
A dipólus jellege vízmolekulák okozza, hogy képesek csatlakozni egymással összeköttetésben, egyre inkább vonzódik pólusok ellentétes előjelű. Ez vezet az a tény, hogy a víz szerkezete, mint egy laza szerkezetű. A valós térfogata meghaladja a számított értékeket.
Megmagyarázni hiánya elektroneutralitás a vízmolekulák és a következők lehetnek. Hidrogénatom, amelynek stabil pályára, kialakítására képes csak egyetlen kovalens kötés. Azonban, bár úgy tűnik, hogy néhány esetben a hidrogénatom, úgy, hogy magukat, és ezáltal összetartására két atom. Ebben az esetben már van egy ionos kötés, azaz kommunikáció, amelynek alapja a Coulomb vonzás között ellentétes töltésű testek. Ez a hidrogén kötés nagyobb valószínűséggel, mint a több elektronegatív atomot csatlakozott hidrogénatom. oxigén-ion van egy nagy negatív töltésű és ezért könnyen képez hidrogénkötést hidrogén-ionok. Következésképpen, a vízmolekulák könnyen jár össze komplexek. Ebben a szerkezetben a víz megváltozott. A változás lehetséges, és a felületén a szilárd fázis.
A jelenléte az elektromos mező hatására a vízmolekulák és a rendkívüli oldhatósága, mert interakció erők közötti töltött részecskék a vízben csökken 81 alkalommal. Ennek eredményeként, az erő belül a molekuláris kötés nem lesz megfelelő, és a részecskék hatása alatt Brown-mozgás oldatba.
A dipólusok lehet vonzott ionok miatt a kölcsönös vonzás elektromos töltések rejlő egyik oldalán iont, és a másik - politika vízmolekulák. Ezt a jelenséget nevezzük hidratációs ionok és ad okot, hogy a hidratációs héj körül az ionok, amely ionok vonzzák vízmolekulák. Mivel a különböző méretű ionok, akkor lehet előre látni, hogy a nagyságát a hidratáció kagyló lesz különböző ionok.
Jelenleg a szerkezete szilárd általában elég részletesen tanulmányozták. Ez alapján a modell típusától kemény labda, labdákat a vonzás és rugalmas golyót. Ennek következtében, vannak kvantitatív elmélete ideális gázok folyadékok ilyen részlegesen folyékony fémek és néhány molekuláris folyadékok. A folyadékok társított hidrogénkötések kielégítő elmélet nem.
A szakirodalomban, az elektron felhő szerkezete elsősorban tetraéderes leírt modell, egy oxigénatom a központban, és két hidrogénatom, a tetejét, és a két negatív töltéseket szimbolizáló félreeső elektronpár a másik két csúcsa a tetraéder.
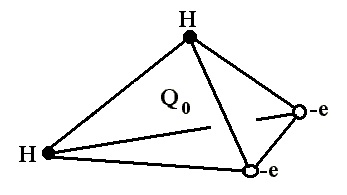
Ezért, egy vízmolekula is részt vehetnek hidrogénkötések négy: két miatt proton és két miatt a magányos pár az oxigénatom. Elsősorban azért, mert a viselkedését a vízben és a tájékozódás a magspinek a két proton. A következő strukturális modell a víz a leggyakoribb: klaszter, klatrát és a folyamatos (folyamatos).
A klaszter modell (J. Nemeth, N. Sheregi) vízzel bemutatott modell formájában klaszterek, azaz, egy adott zónában a molekulák kapcsolódnak más összefüggésben nem. Azzal a lehetőséggel, összeomlott a klaszterek, az újak kialakulását.
Klatrát modell (Samojlov SY) képezünk hidrogénkötések hálózatát a vízmolekulák közötti, amelynek belsejében üregek töltött monomer molekulák (nem-hidrogénkötés).
Continuum modell (I. Pople) biztosítja hiányában vízmolekulák által hidrogénkötések törött képező gyűrű alakú társult.
A bonyolult szerkezet okoz a víz és annak egyedi tulajdonságai és azok hőmérsékletfüggését.
Íme néhány közülük:
A fajlagos felülete olaj- és gáztartályok gyakran eléri a több ezer m 2. Ezért, a szűrő és a gyűjtőfolyadékot létezik a felület kölcsönhatás részben határokat. Ez a reakció jelentős hatással van a szűrés.
A legfontosabb jellemzője az a határfelületi felületi feszültség. Ismeretes, hogy a felületi feszültség a folyadék-gáz számos tényezőtől függ - a kémiai összetétele a folyadék és a gáz, hőmérséklet, nyomás és egyéb tényezők .. A növekedést a felületi feszültség a hőmérséklet és a nyomás csökken. A komplex jellege a felületi feszültség megváltozik a határ-olaj folyékony. Ha az olaj gázmentesített, és tartalmaz szinte semmilyen poláros komponenseket, a határfelületi feszültség vízzel gyakorlatilag független a hőmérséklet és a nyomás. Ha az olaj tartalmaz poláros komponenseket, oldható vízben, majd növekvő nyomás és hőmérséklet, a felületi feszültséget a határfelületen a vízzel növelheti. Jelenlétében oldódó gáz függőség bonyolult.
Közvetlenül mérik a felületi feszültség a szilárd felület nehéz. Ebben az esetben, a felületi feszültség értékeljük közvetve - változtatásával az érintkezési szög, amely arra is szolgál, mint egy intézkedés a nedvesítő folyadék és a szilárd felületre. egy szilárd felületre által nedvesített jobb, minél kisebb a különbség polaritása közötti a test és a folyadék. Erősen poláris folyadék, azaz amelynek nagy felületi feszültség, nedvesíti a szilárd felület rosszabb, mint a kevéssé poláros. Például a higany nedvesíti csak néhány fémek, míg a kevésbé poláris folyadék - víz nedvesíti nemcsak fémeket, hanem sok ásványi anyag, de kevesen vannak poláris olaj - összes szilárd anyagot.
Nagysága az érintkezési szög sok tényezőtől függ. Különösen nagy hatással nyújt adszorpciós folyamatok. Például, a felületaktív kezelés jelentősen növeli a nedvesíthetőség és fordítva csökken.
A nyitott időtartamát a kitermelt alakulatot, és a fejlesztés során fázishatár nem stabil marad: a nyitó - az olaj van tolva a kútból, a fejlesztés során a másik irányba. Ezzel irányváltás megváltozott, és a szög nedvesedés.