Kémia a kíváncsi
Grosse E. Vaysmantel X.
Kémia a kíváncsi. Alapjai Kémia és szórakoztató élmény.
Nézz be az elmúlt
És most, a mocsarak rothadó növények. Rothadó il megtalálható állóvíz tó vagy a part közelében, lassan folyó patak. Során bekövetkező kémiai átalakításokat hasonlóak a folyamatok, amelyek kezdődött a kialakulását a szén és az olaj. Ellenőrizze, hogy ki a segítségével a tapasztalat.
Kapjuk mocsárgáz
Ez hoz egy kis tó iszap. Akkor veszi át a helyét, és a földet az alján a mocsárból. Együtt iszapot vagy földet ott talál vizet. Ezt az iszapot töltjük egyharmadát a nagy üvegedénybe konzervet. Ezután öntsük a jar fel a tetejére mocsári víz. Meg kell erősíteni az üveg tölcsér tetején, és az ő darab gumicsövet csatolja rövid üvegcső kivont véget. Hozam zárja be a csészét egy bilincs egy gumitömlő.
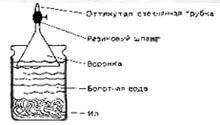
Fokozatosan a gázbuborékok képződnek, hogy a kitöltési tölcsért. Ezt követően a lehető óvatosan emelje fel a bilincset és azonnal meggyullad fejlődő gáz. Égetést főként annak a ténynek köszönhető, hogy az összetétele mocsárgáz tartalmaz metánt.
A metán - az első sorban a szén-dioxid-vegyület. Ez tartalmazza csak szén- és hidrogénatomot. Formula Metán CH4. A molekulában a négy hidrogénatomot vannak ragasztva egy szénatomot tartalmaz. Azonban, a képlet nem ad teljes képet a térszerkezet a metán molekula itt látható. Tanulmányok kimutatták, hogy mind a négy hidrogénatom található a csúcsai egy szabályos tetraéder, hogy van elhelyezve ugyanúgy képest a szénatom, amely a központban.
Metán kapunk nemcsak a pusztulás. Sok metán lévő gázkeverék képződött száraz lepárlással, szén. Továbbá ez az egyik fő összetevője a sok természetes gázok, valamint a mellékterméke a kőolaj-finomítás. Jelenleg, a metán a legfontosabb nyersanyaga a hidrogén, szén-monoxid és a más anyagok. A tökéletlen égés metán kapunk korom (carbon a finoman eloszlatott állapotban), amely a használt különösen, mint töltőanyag a gumiiparban.
Carbon természetesen nem lehet besorolni az egyik leggyakoribb kémiai elemek. A földkéreg ez csak 0,12%. De az összes többi elem, akkor egy rendkívüli sokféle kémiai vegyületek. A száma jelenleg ismert szénvegyületek több mint kétszerese a kapcsolatok számát az összes többi elem együtt.
Az ilyen szén-eredetiség magyarázható különleges képességeit annak atomokkal kémiai kötéseket.
Általában, a szén négy vegyértékű. Atomot is összekapcsolódhat egy többé-kevésbé hosszú láncok és gyűrűk. Amelyekben a fennmaradó szabad vegyértékek egység könnyen hidrogéngázzal telítjük. Ez azt eredményezi, szénhidrogének.
A legegyszerűbb közülük - metán - már találkoztak. Ezután, egy összetettebb szénhidrogén nevezett etánt. A molekula két szénatomot és hat hidrogénatomok.
Csatlakozási harmadik szén telítettség és a szabad vegyértékek hidrogénatomok képződéséhez vezet a propán képletű C3 H8.
Következő szénhidrogén, amelynek négy szénatomot tartalmazó nevezik bután és az összetétele C4 H10.
Ön is létrehozhat több hosszú szénláncú.
Most számos ismert a több mint 100 szénatomot tartalmaz.
Szénhidrogének a metántól a bután gáz halmazállapotú normál körülmények között. Kezdve pentánnal, amelynek öt szénatomot, ezek folyadékok. Vegyületek, amelyek 17 vagy több szénatomot tartalmazó, szobahőmérsékleten szilárd halmazállapotú.
Szénhidrogének metán, etán, propán, bután, és így tovább. G. Ahhoz, hogy egy sor olyan vegyületet, amelyek nagyon közel egymáshoz szerkezetét és kémiai tulajdonságait. A táblázatban „Néhány alkánok” mutatja a név és képlet legfontosabb tagja ennek a sorozatnak. Nyilvánvaló, hogy az egymást követő anyag összetételében eltérő az előzőtől a jelenléte további CH 2-csoport.
Új összes szénhidrogén képletű n szénatom CnH2n + 2. Így a hidrogénatomok számának a molekulában 2 több, mint kétszerese a szénatomok számát. Ezek két további hidrogénatom van végein a szénlánc. Az ilyen vegyületek egy sorozatát nevezett homológ sor.
A nevét az egyes tagok a fenti sorozat szénhidrogének vége a toldalék „egy”, és együtt nevezzük alkánok.
Számos alkánok
Folyékony és szilárd alkánok tartalmazott elsősorban az olaj, valamint a gyanta nyert barnaszén. Alkánok előnyösen 6-10 szénatomot tartalmaz, így oktán, tartalmazza az üzemanyag-készítmény. Követte őket egy sor folyékony alkánok - a fő összetevője a dízel üzemanyag és kenőolajok. A szilárd szénhidrogének elegye, ez a sorozat nevezik paraffin.
Ismert alkánok nem csak egyenes, hanem egy elágazó szénlánc.
Például, a szénhidrogén-C4 H10, két változatban létezik a szerkezet.
A következő lehetséges C5 H12 három szerkezetek:
A alkánok összes szabad vegyértékek a szénatom telített hidrogénatomokkal. Ezért, ők is nevezik telített szénhidrogének ezzel szemben, telítetlen szénhidrogéneket tartalmazhat kevesebb hidrogénatom. Szabad vegyértékei a szomszédos szénatomokon kölcsönhatásba lépnek egymással és képez kettős vagy hármas kötéseket.
A szerkezeti képletek ilyen kötések jelentése két vagy három vonal közötti a mindenkori szénatomok. Nyilvánvaló, telítetlen szénhidrogének, ha rendezni őket, hogy a növekvő számú szénatomot is képeznek homológ sor.
A legegyszerűbb és ugyanakkor a legfontosabb a szakterületen telítetlen szénhidrogének a molekulában egy kettős vagy hármas kötés. Az első esetben nevezik őket alkének. és a második - alkinek.
Az első tagjai a sorozat - etén (etilén) (H2 C = CH 2), és a etin (acetilén) (NS≡SN). Etén és etin fontos intermedierek a szerves szintézisekben technológia. Mindkét gáz jelenleg gyártott világszerte nagy mennyiségben katalitikus kezelése ásványolaj szénhidrogének. Továbbá, nagy jelentőséget egy eljárás etinil a kalcium-karbid és a víz.
Tanulmány tulajdonságainak a telítetlen szénhidrogének etén kezdődik, amelyek könnyen előállíthatók egy alkohol és kénsav.
Gyűjtsük össze egy egyszerű eszköz. Ez szükségessé teszi a két kémcsőbe. Egyikük vegye fel a dugó két lyukat, és helyezzen be egy hajlított üvegcső és hőmérővel ellátott skála akár 250 ° C-on Minden kapcsolat kell szűk ahhoz, hogy a keletkező gáz távozhat csak telefonon keresztül.
A csövet put 2 ml denaturált alkohollal és óvatosan, kis adagokban, adjunk hozzá 5 ml tömény kénsavat (csak szemüveg!). Amikor a keverék nagyon felmelegedett, és azonnal érezni a kellemes illat - ez áll etén, amíg egy kis összeget. Lehet hozzá másik fiolába 1-2 g tiszta finom homok a reakció gyorsítására. Azonban, ha ez nem megy.
Ahhoz, hogy a második cső öntsünk 5-10 ml 10% -os nátrium-karbonát-oldatot (nátrium-karbonát), és adjunk hozzá néhány csepp kálium-permanganát-oldatot. A megoldás állítólag intenzíven lila, de nem túl sötét. Ezt nevezik a Bayer reagens. (A hazai kémiai irodalomból ismert módszer szerkezetének meghatározására telítetlen vegyületek útján oxidációjával híg kálium-permanganát oldattal hívták Wagner reakciót. A reakciót fedezte fel EE Wagner 1887 és leírása a „Journal of the Russian Fiziko-Chemical Society” 1888 m . 20 o 72 -. Megjegyzés toll) ..
Most össze a készüléket, és az első cső kerül melegítjük Bunsen-égő, amíg a hőmérő merítjük keveréke alkohol és kénsav, nem fog megjelenni 150-170 ° C-on
Keresztül egy üvegcső gáznemű etén (most már tudjuk, hogy ez könnyű, kellemes illatú). Vezessük át a Bayer reagens. Hamarosan az oldat színtelenné nem válik, és ezzel egyidejűleg kell elkülöníteni barna pelyhek mangán-oxid (IV).
Ha kevés brómos vizet, hígíthatok vízzel arányban 1: 1, és a kapott barna folyadékot át skip etén. (Vigyázat brómgőz a szemet és a légzőrendszert). Színező brómos víz eltűnik. Ezután etén gyulladásra, még megjelent a hajlított üvegcső. Rágyújtott egy fénylő, enyhén füstös lánggal.
Telítetlen szénhidrogéneket, szemben a teljes, készségesen átmennek kémiai reakciók. Így, tapasztalataink etén oxidált oxigénnel kálium-permanganát, kálium-permanganát és így kinyert. Mint ahogy viselkednek, tekintettel a Bayer reagens és más telítetlen szénhidrogéneket. A reaktivitás a fenti vegyületek, mert a kettős vagy hármas kötést hasítjuk alkotnak egyszeres kötés. Így miatt a szabad vegyértékek kapcsolódnak atom vagy csoport, így oxigén- vagy brómatom.
Használata etén és acetilén (acetilén) az iparban annak a ténynek köszönhető, hogy ellentétben az alkánok, ezek rendelkeznek a magas reaktivitás. Ez neki köszönhetően alapján etén és acetilén lehet építeni a különféle szerves vegyületek.
A legtöbb szerves vegyületek és főleg szénből és hidrogénből.
Már ismeri szénhidrogének tartalmaznak csak ez a két elem. Más szerves vegyületek, amelyek közül sok bemutatjuk később, tartalmaz egy vagy több, más elemek, gyakran oxigén, halogének (klór, bróm, jód), a nitrogén és a kén.
A következő egyszerű kísérletek sok esetben megfelelő a kvalitatív meghatározására, a nitrogén-, kén- és halogének.
Annak kiderítésére, hogy van az anyagban, a nitrogén, minta melegítjük egy kémcsőben feleslegével nátronmész.
Ha nem, akkor lehet cserélni egy keveréket nátrium-hidroxid (nátrium-hidroxid) feleslegben oltatlan. Lássuk csak, hogy a tetején a cső nem marad tapadt mészrészecskék.
Dugja be a csövet egy darab vattát, és tedd egy csík megnedvesített vörös lakmuszpapír. Melegítsük fel a csövet egy Bunsen-égő (kis láng) - első gyengén, majd egyre.
Kék színeződés vizsgálati papír jelenlétét jelzi a nitrogén. A meghatározás azon a tényen alapul, hogy a tartalmazott anyagokra, a szerves kötött nitrogén, melegítés közben nátrium-karbonáttal (vagy még egy módszer - tömény kénsavval) sok esetben átalakíthatjuk az ammónia.
Sok esetben, a halogénatom a szerves vegyületek felhasználásával is kimutatható a Beilstein-próba. Vegye nem túl vékony rézdrót szigetelés nélkül, tisztítás és hajlítsa egyik végét a hurkon. A hurok erősíteni fogja a darab porózus kerámiák ( „egyetlen darab horzsakövet”).
Kalcinált ezen a végén a drót nem világító lángot zónában, míg a zöld szín a láng kialszik.
Ezután merítettünk a vizsgálati folyadék áthúzás, vagy tegye rá a szilárd mintában. Ha most újra, hogy a vezetéket nem világító lángot zónában, halogén jelenlétében detektáljuk zöld (jód) vagy kék-zöld (klór, bróm) láng festéssel.
Azonban ez a vizsgálat nagyon érzékeny. Ezért Halogén gyakran még abban az esetben, ha a vizsgálati anyag szennyezett kis mennyiségű halogént tartalmazó szennyeződéseket. Néhány vegyület (hangyasav és a benzoesav, és a különféle szervetlen anyagok) zavarják, mivel megfestettük zöld láng.
Kimutatására a kén általában kalcinált minta fémnátriummal. Amikor ez a kén válik szulfidot tartalmaznak, amely kimutatható nitroprusszid-nátrium. Fogjuk választani egy másik módja, hogy anélkül, hogy a távoli és veszélyes nátrium.
Spatulahegynyi mintát vesz a vizsgált anyag és elhelyezte egy kis porcelán csészében. Adjunk hozzá néhány vagy jobb tömény füstölgő salétromsav és erősen felmelegszik a csészét. Ezt kell tenni elszívókamrában vagy a szabadban. Amikor ezt a savat elpárologtatják. A maradékot ismét hozzá salétromsavat, és ismét bepároljuk. Oldható maradékot vízben és szűrjük az oldatot, ha szükséges. Ha a vizsgált anyag a mintában tartalmazott kén, majd összekeverjük a kapott oldatot egy bárium-klorid csapadék válik oldhatatlan bárium-szulfát.
Olvasóterem kunstkamery: mi van ott?