Móltömeg benzol (C6H6), és példák a általános képletű
A moláris tömege benzol
Benzol - egy komplex anyag szerves természetű. Progenitor homológ sor aromás szénhidrogének.
A szerkezet a benzol molekula ábrán látható. 1. Normál körülmények között egy színtelen folyadék egy adott édeskés szagú. Mérgező. Hozzájárul a rák kifejlődését. Benzol ég erősen füstös lánggal. Robbanó keverékeket képez levegővel. Vegyes különböző szerves oldószerekkel (éterek, benzin, stb ..).
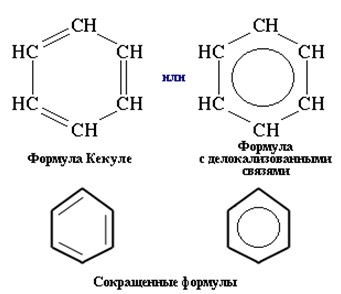
Ábra. 1. A szerkezet a benzol molekula.
Molekuláris képlet benzol - C6 H6. Mint ismeretes, a molekulatömege a molekula az összege a relatív atomi tömegek a atom alkotja a molekula (relatív atomtömeg értékeket vett Mendeleev Periódusos Táblázat egész számra kerekítve).
Úr (C6 H6) = 6 × 6 × 12 + 1 = 72 + 6 = 78.
Móltömeg (M) - a súlya 1 mol hatóanyagra vonatkoztatva. Könnyen azt mutatják, hogy a számértékek a moláris tömege, és a relatív molekulatömeg úr egyenlő, de az első érték az alábbi méretekkel rendelkezik [M] = g / mol, és egy második dimenzió:
Ez azt jelenti, hogy a molekulatömeg-benzol 78 g / mol.
Példák problémák megoldása
Az egyenlet a reakció magnézium oxigénnel interakció:
Mi kiszámítjuk az anyag mennyiségét a magnézium-oxid általános képletű:
n (MgO) = m (MgO) / M (MgO).
Ehhez az szükséges meghatározni a moláris tömege magnézium-oxid (értéke relatív atomtömeg vett Mendeleev periódusos, egészre kerekítve). Mint ismeretes, a moláris tömege a molekula az összege a relatív atomi tömegek a tartalmaznak a molekulában (M = úr):
M (MgO) = Ar (Mg) + Ar (O) = 24 + 16 = 40 g / mol.
Ezután, az összeg a magnézium-oxid anyag egyenlő:
n (MgO) = 2/40 = 0,05 mól.
Szerint n (O2) reakcióegyenlet: n (MgO) = 1. 2, akkor:
n (O2) = 1/2 × n (MgO) = 1/2 × 0,05 = 0,025 mol.
Találunk moltömegére oxigén (feltételezés, az oxigén a számítás a moláris tömeg, sőt ebben az esetben):
M (O2) = 2 × Ar (O) = 2 × 16 = 32 g / mol.
Mi határozza meg a tömeg az oxigén:
m (O2) = 0,025 × 32 = 0,8 g