5. fejezet hibridómatechnológia
5. FEJEZET hibridómatechnológia. monoklonális antitestek
A késő 60-as - a korai 70-es XX században. laboratóriumi módszerek klónozáshoz in vitro sejt-fejlesztettek. Ehhez hozza létre a szükséges táptalaj, anyagok laboratóriumi üvegedények és termosztátok inkubátorok, amely lehetővé tette, hogy szimulálja a feltételeket, a szervezet belső környezet megőrzése életképességének emlős sejtekben. 10-12 éves, sikerült klónozni csak tumorsejtek, mert képesek a tulajdonhoz korlátlan (kedvező külső feltételek a számukra) szakadék mitózisával. G. Keller és C. Milstein 1974-1975 gg. Használtuk a eljárás hibrid szomatikus sejtek, amelynek felhasználásával a tanulmány a citogenetikai lokalizációs szabályozó gének egy adott jelzés egy adott kromoszóma (a hibrid sejtek bocsátanak ki a legtöbb a kromoszómák, de nem az összes), a limfociták, hanem más célokra. G. Keller és C. Milstein kapott hibrid sejtek limfoid tumorok (myeloma) és a normál limfociták. Hibrid sejtek a kromoszóma részeként (és következésképpen a tulajdonságait) normál limfocita (a másik része kilökődik a kromoszómák a sejtek az első osztály, a genom még nem stabilizált) és egy részét - a daganat. Miután a sejtek szaporodnak örökölt myeloma képesek osztódni. Egyidejűleg mentek bioszintézis egyes termékek normál limfociták, az ilyen antitestek; A legfrissebb és a szükséges G. Keller és C. Milstein. Korlátlan osztódó sejtek „lehetővé teszi” magát klónozni, azaz fizikailag „leülni” egy (minden egyes, egy külön edényben) és azokból klónokat nyerjünk a sejtek - a leszármazottai egyetlen sejt. Az ilyen sejteket nevezzük hibridómák.
Limfociták hibridizációs állítjuk elő a lépből vagy a nyirokcsomókból előzőleg antigénnel immunizált egerek (gyakrabban - a vonal Balb / c). Mivel a tumor kletokpartnerov használnak speciálisan tenyésztett hibridóma mutáns egér mielóma sejtek (más néven plazmacitóma, hogy ebben az esetben az azonos) nyert transzplantált mielóma sejtvonal MOPC-21 Balb / c egerekben
tenyészetben tartjuk in vitro és 1921 G. Keller és Milstein alkalmazásával mutáns mielóma származó sejtek citogenetikai korábban szintén előállítására alkalmas hibrid emlőssejtek, hanem más célokra: a hibrid sejtek dobja legtöbb kromoszóma megmaradt citogenetikai korrigált lokalizációját bizonyos gének priznakkodiruyuschih bizonyos kromoszómák.
A szuszpenziót a limfoid sejteket az immunrendszer egerek összekeverünk egy kémcsőben minimális térfogatú tápközegben szuszpenziójával mielóma sejtek 1-2 percig, és hozzáadunk Egyesítést szer. Keller és Milstein először, ez a szer volt, mint a cytogeneticists, Sendai-vírus, de néhány hónap után az összes „gibridomschiki”, mint koaleszcens ágens használható szintetikus polimerek, - a polietilén-glikolok, amelyek molekulatömege 1540-6000 D. Miután 1-2 percig sejtszuszpenzió keverékét tartalmazó fuzionált limfoid sejtek, nem fuzionált mielóma hibrid sejteket 3 variánsok sejtek ( „a limfocita-limfocita”, „myeloma-myeloma”, „limfocita-mielóma”, amelyek a keresett sejtek csak hibridek „limfocita-myeloma”), mosott és tenyésztették a kiszámított térfogatát a HAT szelektív táptalajon. NAT jelenti «aminopterin timidin». Ezek a 3 komponenseket adagoljuk ismert koncentrációkban teljes táptalajban. Az első 7-10 nap tenyésztés, az említett keverék a tenyészetben lévő sejtek, a következő történik:
1) a nem fuzionált limfociták és hibridjei „limfocita-limfocita” elpusztulnak, mert a természetes törékenységét;
2) a nem fuzionált mielóma sejteket és a hibrid „myeloma-mielóma” halnak, hogy képtelen elvégzésére bioszintézisét DNS jelenlétében aminopterin - metabolikus mérget,
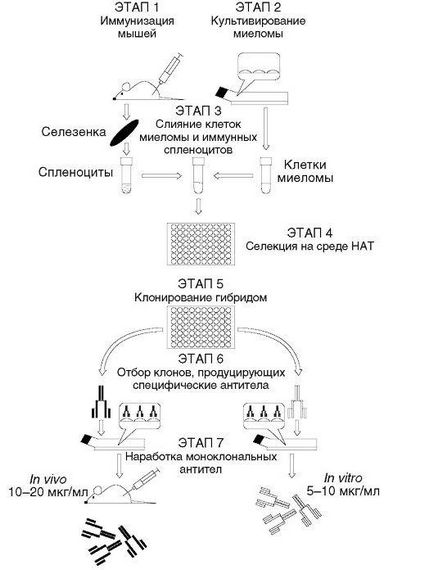
szelektíven blokkoló bioszintetikus enzimek de novo pirimidin bázisok az N5 N10-metilén-tetrahidrofolát; bioszintézisének purin bázisok hipoxantin ezekben a sejtekben is lehetetlen hiánya miatt GGFRT; 3) az egyetlen sejtek, amelyek képesek túlélni HAT média kívánatos, „limfocita-mielóma” hibrid sejtek: bioszintézisét purin bázisok nyújtott GGFRT gén, amely származik a normál limfociták, és a környezeti hipoxantin és bioszintézisét pirimidin bázisok végezzük sredovye timidin részvétele a timidin kináz. A fő szakaszai hibridóma technológia ábrán mutatjuk be. 5.1. Tól myeloma adatok hibrid sejtek öröklik az ingatlan korlátlan szaporodását. A normál immunrendszer B-limfociták - bioszintézise immunglobulinok.
Elterjedése «non-stop» lehetővé teszi, hogy a klón a hibrid sejtek, azaz a 1 diszperz is, és várjon egy cellát, hogy kedvező növekedési feltételek növekedni klón, azaz sok azonos sejteket (eltekintve spontán mutációk). Mely a kapott „limfocita-mielóma” hibrid sejtek termelnek antitestet, megtudni, kiválasztja a kutak megfelelő mintákat felülúszó immunoassay. Később a kiválasztott hibridóma rekloniruyut és ismételten kimenetre tömegkultúra - reaktorok in vitro vagy aszcitesz tumorok szingenikus egerek. A tenyészet felülúszókat vagy az aszcitesz folyadékokat izolált hibridóma monoklonális antitest tisztított formában.
Ha egy klón hibridóma sejtek antitesteket szintetizáló ezeket az ellenanyagokat nevezzük monoklonális. A tapasztalat azt mutatja, hogy az összes kiónozott hibridóma sejtek szintetizálják antitestek azonos - és specifitását az aktív hely, és az izotípus a nehéz lánc, azaz A monoklonális antitestek - nem csak Monoklonális terméket, hanem a készítmény az azonos antitestek. A késő 1970-es években már in vitro tenyésztjük, és klónozott T-sejtek, nem keresztezzük tumor sejtvonalban. Ez csak akkor vált lehetségessé, miután felfedezték a növekedési faktor a T-limfociták pedig később az IL-2. Ez klónozása T-limfocita alcsoportok felfedezéséhez vezetett a CD4 + T-limfociták, és hogy sok más felfedezés, beleértve azon HIV (elegendő, hogy tanulmányozza a számát gének és fehérjék a vírus is kiderülhet
Csak a T-limfocitákon, in vitro tenyésztett jelenlétében növekedési faktorok). B-limfociták, anélkül, átalakítja őket a hibridómákat lehet osztani (amely lehetővé teszi számukra, hogy klónozott) Fertőzéskor őket Epstein-Barr-vírus (átalakítja normál B-limfocitákat a tumorban a B-limfociták).
Így, által termelt monoklonális antitestek egyik klón a következők:
• rendkívül specifikusak, mivel egy adott antigén determináns;
• azonos izotípusú, idiotípus és a allotípus, valamint affinitást és fiziko-kémiai jellemzők.
Stabil hibridóma tenyészetek előállítására képes korlátlan számú monoklonális antitestek.
A monoklonális antitesteket már széles körben használják különböző területeken az orvostudomány. A mAb-alapú alkalmazás különböző területeken az a lehetőség, nagy mennyiségben való kinyerésére nagy affinitású specifikus antitestek:
1) az immunogén antigének, hisztokompatibilitási és meghatározzuk differenciálódását;
2) A differenciálódás, neoplasztikus és más sejtfelszíni antigének, amelyek mentesek a polimorfizmus és a nem-immunogén allogén rendszerekben, de felismerte, amikor xenogén immunizálás;
3) vírusos és bakteriális antigének;
4) egy izolált antigén determinánsokat különböző fehérjék, nukleinsavak és a cukrok.
Használata mAb lehetővé teszi, hogy meghatározza, és elkülönítünk egy szubpopuláció sejtek megkülönböztethetők az egyedi sejt-fejlődés lépésben, pontosabban gépelt szöveti pontosabban azonosítani a mikroorganizmusok, valamint több megbízható meghatározását immunológiai módszerek biológiailag fontos makromolekulát.
nagyszámú rendszerek diagnosztizálására különféle betegségek kifejlesztett gyógyászatban alapján Mab (fertőző betegségek, rák és mások.). Aktívan kifejlesztett és a kábítószer alapuló Mab, például rákellenes gyógyszerek, anti-citokin antitest (hatóanyag remikeyt et al.) Azonban, azt bizonyítják, hogy a rágcsáló Mab immunterápiára daganatos betegségek ad okot, hogy a különböző mellékhatások, és különböző intézkedéseket gyenge hatékonyságot.
Módosítása rágcsáló mAb (humanizált antitest Mab konjugátumok és a magas -. Radionuklidok, gyógyszerek, toxinok, stb) új lehetőségeket nyit meg a diagnózis és a kezelés a rák és más betegségek.