Osztályozás és nómenklatúra, eljárások előállítására karbonsavak
A karbonsav - egy osztály a szerves vegyületek, amely molekulák tartalmazhatnak egy vagy több funkciós karboxilcsoportokat -COOH csoport. IUPAC. kiválasztjuk mint az alapját a leghosszabb szénlánc tartalmazó -COOH csoportot, és hozzátéve, hogy a neve a megfelelő szénhidrogén végződő „OIC”, és a „sav”.
Például CH3-CH2-COOH - -propánsav, CH3-C (CH 3) 2-COOH - 2,2-dimetil-propánsav. A racionális hozzáadott végződő "karbonsav" és a „sav például, S5N9SOON -. Ciklopentánkarbonsav-, CH3-C (CH 3) 2-COOH - terc-butilkarbonovaya sav.
Attól függően, hogy a radikális kapcsolódik a karboxilcsoport következő karbonsavak: aromás
alifás (beleértve a telített és telítetlen), aliciklusos
heterociklikus. Száma szerint a karbonsav-csoportok lehetnek mono-, di- és több-bázisú.
karbonálást szerves fémvegyületek
Észterek hidrolízisét
21.Himicheskie tulajdonságok pridelnyh monokarbonsavak. A példaként az ecetsav. Nab Eq észterképzési reakcióban ecetsav és propanol2.
1. Disszociáció savak. Minden karbonsavak, a szervetlen savak, mint a, savas tulajdonságokkal rendelkezik, festés lakmusz piros. Ez annak köszönhető, hogy a disszociációs savak:
RCOOH <-> RCOO- + H +
2. sóinak kialakítása. Karbonsavakat könnyen vstu Payuta reakciót bázisokkal, bázikus oxidok és aktív fémek:
2RCOOH + Mg = (RCOO-) 2 Mg + H2
RCOOH + NaOH = RCOONa + H2O
2RCOOH + CaO = (RCOO-) 2Ca + H2O
Karbonsavak sói erősen hidrolizált, vizes oldatban, mint gyenge savak sói. Ásványi savak, mint például erősebb kiszorítják karbonsavak sóikból:
CH3COONa + HCl = CH3COOH + NaCl
Karbonsavak ellenállnak a koncentrált ásványi savak. Kivétel ez alól a hangyasav, amelyek, az intézkedés alapján koncentrált H2S04 lebomlott:
HCOOH --- H2SO4 ---> CO + H2O
4. Az intézkedés alapján halogének jelenlétében foszforossav képződött alfa-halogénezett savak:
CH3-CH2-COOH + Br2 -> SNVr-CH3-COOH + HBr
5. Az intézkedés alapján redukálószerek, például LiAlH4, savakat csökken primer alkoholok:
R-COOH -> R-CH 2-OH + H20
6. A telített savat egy egyenes szén-láncú nehéz oxidálni. Reagáltatva tercier szénatom az oxidációját hidroxi-savak:
(CH 3) 2 CH-COOH -> (CH 3) 2 C (OH) COOH
Észter-képződés.
1. CH3-CH (OH) CH 3 + SN3COOH = CH3-COO-CH (CH 3) 2
22. Kémiai tulajdonságok korlátozzák dikarbonsav. A példában az oxálsav. Írja egyenlet észter oxálsav képződését és propanol2.
Dikarbonsavak (vagy dikarbonsav) - karbonsav, amely két karboxilcsoportot -COOH, a HOOC-R-COOH, ahol R - bármilyen kétvegyértékű szerves csoport.
Oxálsav széles körben elterjedt a természetben formájában kalciumsók
Dikarbonsavak mutatnak az azonos kémiai tulajdonságokkal rendelkeznek, mint a monokarboxil - ezek a tulajdonságok jelenléte miatt a karboxil-csoportok:
disszociációs vizes oldatokban
az első szakaszban (KA1):
NOOC-X-COOH → NOOC-X-COO + H +
második szakasz (Ka2):
NOOC-X-COO- → OOC-X-COO + H +
észter oxálsav képződését és propanol2.
1.NOOS-COOH + CH 3 CH (OH) -CH3 (H2SO4) = HOOC-COO-CH (CH 3) 2 + H2O
2. HOOC-COO-CH (CH 3) 2 + CH 3-CH (OH) -CH3 (H2SO4) = (H3C) 2CH-OOC-COO-CH (CH 3) 2 + H2O
23. geometriai (cisz és transz) izoméria példáját fumársav. Írja egyenlet észterképzési reakcióban a fumársav és 2 propanol.
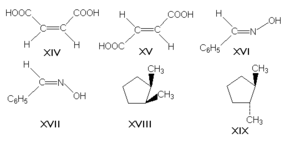
π-diasztereomerek, más néven geometriai izomerek különböznek különböző térbeli elrendezése a szubsztituensek viszonyítva a kettős kötés a (többnyire C = C és C = N) vagy a ciklus. Ezek közé tartozik, például, maleinsav és fumársav (XIV általános képletű és a XV, rendre), (E) - és (Z) -benzaldoksimy (XVI és XVII), cisz- és transz-1,2-dimetil-ciklopentán (XVIII és XIX)
észter képződés
HOOC-CH = CH-COOH + CH 3 CH (CH3) -OH ------> CH3-CH (CH 3) -OOS-CH = CH-COOH + H2O monoizopropilfumarat.
CH3-CH (CH 3) -OOS-CH = CH-COOH + CH 3 CH (CH3) -OH ------> CH3-CH (CH 3) -OOS-CH = CH-COO-CH (CH 3) - CH3 + H2O, diizopropil.