Cribs Kémia
Hidrolízis sók - reverzibilis folyamat. Számára, mint bármely más reverzibilis reakciók, azzal jellemezve, hogy az egyensúlyi állapot eltolható elve szerint a Le Chatelier. Például, ha a megsavanyított konyhasóoldattal NH4CI, az egyensúly balra tolódik, vagyis lassú hidrolízise:
Hígításkor az oldat egyensúlyi jobbra mozog, vagyis a hidrolízis só növekedését.
Ha a sót a gyenge oldhatatlan (vagy illékony) bázis és egy gyenge, illékony (vagy oldhatatlan) egy savval, a hidrolízis egy ilyen só megy a végére. Például, Fe 2 (C0 3) 3 az oldatban nem létezik, mivel a teljes hidrolízist:
A vezultate esik barna csapadék Fe (OH) 3 és a C0 2 gáz szabadul fel.
Ennek oka a hidrolízis sóinak a kation az offset víz disszociációs egyensúlyi hatása alatt egy só kationok felé hidrogén felhalmozódása kationok N.
Sók hidrolízisét okozza az anion egy eltolódás az egyensúlyi disszociációs víz hatása alatt a só anionok az anion oldalán felhalmozódásának OH -.
Ok sói hidrolízisével kation és anion.
Mivel a képződött sót egy gyenge bázis, és a gyenge sav, és a kationok, és a só anionok bomlanak víz:
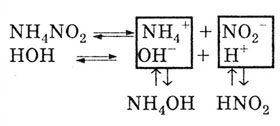
Ennek eredményeként a reakcióközegben, vagy semleges vagy enyhén savas vagy enyhén lúgos. Ez attól függ, a disszociációs mértéke a képződött gyenge savak és bázisok.
Feladat. Írja az egyenletet hidrolízis reakciók:
- a) ammónium-klorid;
- b) nátrium-acetát a molekulaion és redukált forma.
Határozza meg a reakcióközegben. Hogyan változtassuk meg a színét lakmusz a megoldást ezen sók?
Megoldás a) Ammónium-klorid NH4CI - képzett só gyenge bázisnak NH4OH és egy erős sav, sósav, hidrolizáljuk a kation. Rövid ionos egyenlet:
Írni molekuláris egyenlet ionokat hozzáadni, amely nem vesz részt a hidrolízis, de az oldatban. Ez kloridionokat:
a reakcióközeg savas. Lakmusz pirosra vált.
b) Nátrium-acetát CH 3 COONa - képezett só egy erős bázis és egy gyenge sav NaOH CH3COOH, hidrolizáljuk az anion. Ez a folyamat lehet kifejezni csökkentett ionos egyenlet:
Hozzáadása hiányzik kationok Na + molekuláris egyenletet kapjuk:
Reakció közeg lúgos, lakmusz - kék.