termo-oxidatív lebomlását
Bár a tiszta termodsstruktsiya határoló elengedhetetlen feldolgozása polimerek és azok használatát magas hőmérsékleten, hogy csekély hatása van a gyakorlatban a polimer termékek szobahőmérsékleten tempera-kerek, különösen, ha a polimert levegővel érintkeztetjük. Szinte az összes polimeráz-távú stabilitást úgy határozzák meg az árok oxidáció.
Oxidáció - Ez a polimer reakcióba lép az oxigénnel hőmérsékleten, ahol a termikus degradációs elhanyagolható. Egyszerű szénhidrogének Tanulmányok kimutatták, hogy a polimerek normál hőmérsékleten használat észrevehetően nem oxidált, és ez vezetett a koraérett és közhiedelemmel, hogy normális körülmények között a polimerek oldott ns destructor. Tulajdonképpen-oxidok Leniye egy nagy technológiai probléma, és csak egy kis számú polimerek feldolgozhatók és felhasználhatók anélkül stabilizáció. Az ok abban rejlik, hogy a szennyeződések és strukturális hibák polimerek, különösen-de alávetik kezelésnek.
Oxidáció - közötti reakció szilárd részlegesen cal kristályos polimer és a gáz. A fő különbség a termikus degradációs, hogy ezek a reakciók jelentkeznek lassan hetek vagy évek; A kimeneti illékony termékek lehetnek szinte észrevehetetlen. szükséges az oxigén diffúzióját a polimer oxidációja.
A körülmények, amelyek az oxidáció, lehet elég időt személyes, de van két fontos esetekben. Ezek közül az első - a gyártás Leniye-termékek, ahol a polimer a ömledék formájában, az oxigén koncentráció nagyon alacsony, a reakció gyorsan végbemegy, van egy erős nyíró stressz. A második esetben - ez a mindennapi használat izde-
Ly ha a polimer szilárd állapotban, a reakciók nagyon lassú, de tartja oxigenizáció és esetleges UV fény hatására, és at-mosfery m. P.
Oxidációs vezethet elvesztését a mechanikai tulajdonságok, és egy polimer anyag gyakran törékennyé válik nagyon alacsony szintű oxidációs. Ez tükröződik a megjelenését a termék készül belőle; vált gyakori jelenség elszíneződés, repedés, fényvesztésével, és sárgás.
A megértése alapjainak van kialakítva az oxidációs kémia klasszikus lépések perces Bolland és Ki [5-8] a oxidációja természetes gumi és a modell ol - finnek szénhidrogének Ezek a vizsgálatok azt mutatták, hogy az oxidációs láncreakciót tartalmaz ciklus:
IL + X -►I „+ HN Initiation
BG + 02- ^ I02 Folytatás láncok
Xfr + YANG -► IOON + és *
GYU2 (K) + (K *) -► inert termékek nyitott áramkör
Ha X - az elsődleges csoport, melynek eredetét megbeszéljük később.
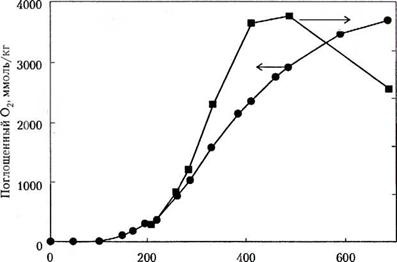
A termék a kezdeti ciklus polimer hidroperoxid 1YUON. Ő instabil, és elbomolhat a kialakulását új csoportok, amelyek kezdeményez egy új láncreakció. Így van egy láncreakció, amely regenerálja a saját kezdeményezője, és az eredményeket-Tat válik önálló gyorsulás. Egy tipikus minta indukciós időszakot lassú reakció, majd gyors oxidációt. Ez a műsor, de látható. 2.1, ami azt mutatja, az adatokat a felgyorsult öregedés PP. Bizonyos esetekben, például a PP, peroxidok képződését mehet gyorsabban, mint a bomlási (ez függ a hőmérséklet), úgy, hogy azok nakapli-vayutsya a polimerben. Más esetekben, peroxidok olyan instabil, hogy a versenyeket, esések után azonnal előfordulásuk.
A szakirodalom teszi sok feltételezések reakciók megindításáról, például:
Minden közvetlen reakció a polimer, mint például a független, és részvételével oxigén termodinamikailag nem indokolt hőmérsékleten vstre-tens a gyártására és üzemeltetésére (ezért tiszta modell vegyület-WIDE oxidált vonakodva). Jelenleg elfogadta, hogy a termo-cal megkezdése végezzük elsősorban bomlás
Nyomokban hidroperoxidcsoport felmerült az oxidáció során a gyártási szakaszban, bár fontos lehet, és sok más tényező.
Hidroperoxidok termikusan instabil, mert a gyenge kötés O-O. A legegyszerűbb monomolekuáris bomlás szünet kapcsolatokat 0-0 mintegy két-bályok csoportok:
1YUON-► SHE „+ OH *
Mint alkoxicsoport, és hidroxilgyökök nagyon reakcióképes és gyorsan elválasztjuk DK * H a polimer, amely során víz:
* 1yu gyök reagál ugyanolyan módon és így KOH. A poli-intézkedések is vezet megrepedése Exalt, mint látni fogjuk.
21100N-► IO + XFR + H20
Ismét gyökök LO és LO * ^ vannak kialakítva elválasztásával vagy törés.
A valós helyzet sokkal bonyolultabb. A szénhidrogének a hidrogénkötés poláris hidroperoxid társulás vezetett a bimolekuláris th bomlás:
Hidroperoxidok nagyon érzékeny a kis mennyiségben tallium ionok Me-több oxidációs állapotok (Pe, T1, Co, Mn, Cu, Cr).
Mindig jönnek a katalizátor vagy használt berendezések a pro-sét, és serkentik a gyors bomlása peroxid:
YOON + M + ------- + _ ►1YU OH + M2 +
BYUON + M2 + ------ ►ko2 + H + M +
A két reakció képező folytatása a ciklus, egyikük sokkal gyorsabb th jelentése alkilcsoport reakciót oxigénnel. Szinte az összes csoportok fordulnak elő a közönséges polimerek, ebben a reakcióban keletkezett-egy véletlenszerűen ütközések, és a zéró aktiválási energiája, úgy, hogy az alkilcsoportok élettartama nagyon kicsi, ha a polimer egy Kitty lorod. A második lépés - az elkülönítés a hidrogénatom a polimerből, hogy egy új csoport, és egy alkil-hidroperoxid - sokkal lassabb. A aktiválási energia függ disszociációs energia megtöri a kötések C-H. Ily módon az ilyen polimerek polipropilén, amely kapcsolatot biztosít a MULTI IN-oxidációs pont függ a reaktivitás kapcsolatát GW1. A fő oxidációs PP egy tercier C-H kötést. Hasonlóképpen, Nat gumi-ponti fő oxidációs egység egy része a tercier szénatom a kettős kötések nylon - a metilén-csoport a nitrogén oxidációja után folyadékok is várható, hogy továbbra is statisztikailag-cal. A szilárd fázisú gyökök mobilitás korlátozott lehet, és folytatjuk csak a helyi „oxidációs zóna”. Például, ismert, hogy az intramolekuláris folytattuk PP ad rövid hidroperoxidok szekvenciát reakcióvázlaton bemutatott 2.4.
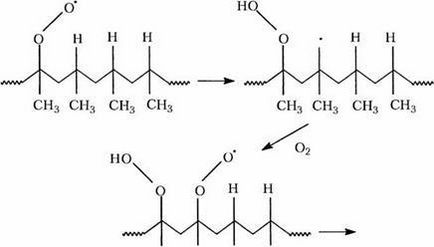
CH 3 CH 3 CH 3 CH 3
A PE és a gumi, ahol a mobilitás magasabb szekvenciák kevésbé gyakoriak, de szabálytalan peroxidok is előfordulhat. Jelenleg az eszköz értékű beszélgetés a megfelelőségét homogén kinetikai modellek leírására-CIÓ folytatódik oxidációs polimerek.
Megjegyezzük, hogy a relatív koncentrációja gyökök R * és függ a relatív sebessége a két lépést folyamatos, és ezért az oxigén koncentráció. A lakosság gyökök oxigenizáció feltételeknek kell uralni gyökök 1YU2”, de a gyártás során. ahol a radikális Concentra-rádió sokkal kisebb, a gyökök A * lehet sokkal több, ZNA-chenie; ez nagymértékben meghatározza a választott stabilizátorok.
Alkilperoksiradikaly általában viszonylag stabil, és nem lép mellékreakciókat. A polimer, oxigénezett alkil Rádhiká-ly gyorsan alakulnak alkilperoksiradikaly reagáltatva oxigénnel, így a részvétel más reakciók nem számít. A legfontosabb mellékhatások reakciók alkoxicsoport. A folyékony szénhidrogének fő reakció a szétválasztása hidrogénnel egy alkohol. A polimerek, ellentétben, versengő folyamat lehet időt-F - ryv hogy egy karbonilcsoportot képez, és egy alkilcsoport (reakcióvázlat 2,5).
Ez egy kulcsfontosságú reakció, hiszen egy nyitott áramkört. A kapott aldehid és keton reakcióképesebb az oxidációra, mint a polimer. A korai szakaszban zhisleniya melléktermékek túlnyomórészt aldehidek és ke - hangok, de az értéke a karbonsav növekszik a konverzió. Ha Kitty tételek és alkoholok képződött közelben, úgy tűnhet, és gyűrűs éterek
CH 3 CH 3 CH 3 CH 3 CH 3 CH 3 CH 3 CH 3
Skie laktonok. A formáció észtereket pedig karbonsavak és alkoholok nyújthat jelentős, ha nem elsöprő, a hozzájárulása a teljes koncentrációját az észtercsoportok a oxidált poliolefinek 9
Elvileg, a csillapítás kell adni két alkoxi-peroxid térhálósító, valamint a záróelem alkoxigyök az alkil-csoportot az éter kell adni térhálósodás. Nagyon nehéz beszerezni kísérleti bizonyíték mellett bármilyen ilyen reakciók, mert például dial-észterek és nehéz ellenőrizni. Azonban, nem kétséges, hogy az idő-ryv lánc uralja a telített szénhidrogén polimerek
Az alkoxicsoport játssza a legfontosabb, mert a nagy felületű reagenst és képes túlélni oxigén jelenlétében, azaz a reakció-rés, illetve az áramkörök és a legtöbb stabil oxidációs termékek. Így, az oxidációs telített polimerek telítési körülmények között Kis-
• llllll CHO SN2'LLLLLL
Lorodom ad egy kis szünetet. Ezzel szemben, a nagy koncentrációjú telítetlen gumik-TION C = C kötés vezet az a tény, hogy a támadás a C = C össze lehet hasonlítani a folytatása és szakadás.
Ennek eredményeként, a telítetlen gumik mindig fordul elő varrás EPO - ksidirovanie és a kialakulását ciklusos peroxidok. Növelése térhálósűrűsége megnöveli gumi keménységét.
Ha az oxigén koncentrációja alacsony, mint ahogy az a műanyag készít-TION szakaszban, az R * elég stabilak ahhoz, hogy reagáljanak függetlenül. Akkor lesz közötti verseny rekombinációs térhálósító és (3-break kifejezés hozzájárulására koncentrálva reakciók függ a polimer, például a feldolgozó a PP helyezése-Nick diszkontinuitások, és PE -. Crosslink [10].