08 adiabatikus index
Work №8 (virtuális)
meghatározására fajhő aránya állandó nyomáson, hogy a fajhő állandó térfogaton levegő által adiabatikus tágulása
A cél a munka -, hogy tanulmányozza az ideális gáztörvény és az alapvető rendelkezések a klasszikus elmélet a hő kapacitást; meghatározzuk Poisson - aránya fajhő állandó nyomáson fajhő Cp állandó térfogaton, CV adiabatikus expanzió (Clement - Desormes).
A hőmennyiség korlátozza, amelyet be kell jelenteni, hogy egy mól az anyag hogy növelje annak hőmérséklet 1 K, az úgynevezett moláris hőkapacitás.
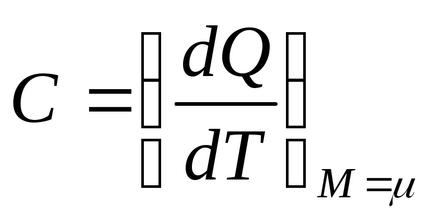
ahol Q - hőmennyiség jut a rendszer, T - abszolút hőmérséklet, M - tömege a gáz, - tömege egy mól gáz.
Mivel az elmélet és a tapasztalat, a hő kapacitása függ a feltételeket, amelyek mellett a gáz melegítjük, azaz a természet a termodinamikai folyamatot.
Hőkapacitása gáz állandó nyomáson (Cp) nagyobb, mint a hőkapacitása állandó térfogaton (CV). Ez könnyű megmutatni minőség alapján az első főtétele: a szám teplaQ. szolgáltatott a rendszer, hogy növelje a belső energia és sistemyU rabotyA ez pontozási rendszer a külső szervekkel.
Ha a gáz melegítjük állandó térfogaton, a műveletet nem hajtunk végre, és az összes a hőbevitel, hogy növelje az árrés a belső energia U, azaz csak növeli a gáz hőmérsékletét. Ha a gáz melegítjük állandó nyomáson, az kitágul, és termel munkát igényel további hőáram. Így, hogy növelje a gáz hőmérsékletét egy bizonyos értéket a izobár folyamat során egy nagyobb mennyiségű hőt, mint amikor izochor.
Amint következik az elmélet
ahol R- egyetemes gázállandó.
Az arány = Cp / CV belép a Poisson-egyenlet leírja az adiabatikus folyamat, azaz, folyamat fut, anélkül hőcsere a környezet (Q = 0):
Ott IV1 - a nyomás és a gáz térfogatát az első állam, p2 u nyomás és a gáz mennyisége a második állapotban.
Komplett szigetelő gázt a környezetet nem lehet végrehajtani. Azonban, ha az állam a gáz paraméterei nagyon gyorsan változnak, a folyamat lehet tekinteni körülbelül adiabatikus. A gyakorlatban, adiabatikus folyamatot hajtunk végre bizonyos hőerőgépek (például dízelmotorok); hangterjedés gázokban (gyors periodikus változása a nyomás a kistérségek tér) is zajlik adiabatikus.
beállítás áramkör látható az 1. ábrán A beállítás áll egy üvegtartály 1, a 2 tartályt a sűrített levegő és a U alakú folyékony manométer 3. Van még két daru - a bemeneti szelep 4 szolgáló bemeneti gáz az 1 edénybe a 2 tartály és a kimeneti szelep 5 csatlakoztatásához a hajó a légkörbe.
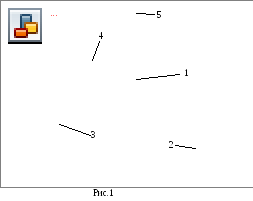
Következtetés dolgozó formula.
Tekintsük a módszer Clement - Desormes. Töltsük levegőt egy üvegedénybe 1 (lásd. Ábra) és zárja a szelepet 4. A gyors összenyomását a levegő hőmérséklete emelkedik. Ezért, miután a terminációs bemeneti különbség a manométer-folyadék szintje fokozatosan csökkenni fog, amíg a hőmérséklet a tartály belsejében egyenlővé válik a környezeti hőmérséklet. Nevezzük légkondicionáló az edényben, miután a hőmérséklet kiegyenlítés 1. feltétel paraméterek állapot 1: V1 - az egységnyi térfogatú levegő tömegét; T1 - levegő hőmérséklete; P1 - a nyomás az edényben.
Mintegy tkroem kran5 és amint a nyomás a légköri nyomás, zárja be. Mivel bővítése igen gyorsan játszódik le, akkor a folyamat közel adiabatikus és így a hőmérséklet a t2. Eltolhatóegység levegő tömege válik egyenlővé V2. A levegő maradt a hajó mozog az állam 2 V2 paramétereket. t2. p2 (p2 -atmosfernoe nyomás). Mivel a T2 hőmérséklet kisebb, mint a külső, a levegő a tartály fokozatosan felmelegítjük (utáni következmény hőcsere a környezettel), hogy a környezeti levegő hőmérséklete t1. Ez isochorically fűtési fordul elő, mert a szelep zárva van. Levegő nyomás az edényben növekszik, mint a légköri, és a nyomásmérő felmerül különbség h2 szinteket. azaz levegő megy állapotban 3 V2 paramétereket. t1. p3.
Így van három állam a gáz a következő paraméterekkel:
6) kiszámítjuk minden egyes mérés, amelyet a képlet (7); az átlag

7) a mérési hiba ebben az esetben (a meghatározott érték újrahasználható) kell kiszámítani, mint az átlagos n kvadratikus mérési sorozat:
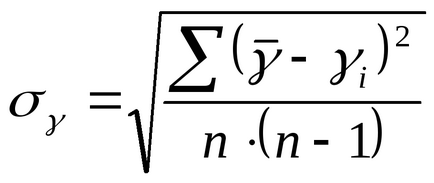
8), hogy a végső eredményt.
1. Mi a fajhője, moláris hőkapacitás, fajhő? Hogyan kapcsolódnak? Mi az a dimenzió a hőkapacitás? Mi határozza meg a moláris hő?
2. Miért Cp> CV szempontjából az első főtétele?
3. Mi a nevezett folyamat adiabatikus? Mi egyenlet adiabatikus folyamat? Döntetlen a adiabatikus p-V koordinátákat.
4. Melyek a termodinamikai folyamatok zajlanak ebben a munkában? Döntetlen ezen eljárások p-T koordinátákat, V-T, p-V.
5. Miért nyomás mérésére kell végezni után azonnal átfedésben (kisütés) a levegőbe, és egy idő után?