alkének 1
Szénhidrogének a molekulában mellett egyszerű σ-kötések szén - szén és a szén - hidrogén: szén-szén π-natív kommunikációs nevezik telítetlen. Mivel a kialakulását π-kapcsolat elvesztése formálisan ekvivalens egy mól-pled két hidrogénatom, a telítetlen szénhidrogéneket tartalmaznak 2n hidrogén atomok kisebb, mint a határérték, ahol n - száma π -kötéseken:
Sorozat, amelynek tagjai különböznek egymástól (2H) n. izologicheskim felhívta következő. Így a fenti séma olyan izologami hexán, hexén, hexadiének, hexinilcsoport és hexatrién t. D.
Szénhidrogének, amelyek egy π-kötés (.. Azaz, kettős kötés) nevezzük alkének (olefinek) vagy az első kifejezés a sorozat - etilén, etilénesen szénhidrogének. Az általános képlet a homológ sorozat C N2l.
Összhangban az IUPAC-szabályok, ha építési Hosting Project-ny alkének leghosszabb szénlánc egy kettős kötést tartalmazó, nevet kap a megfelelő alkán, ahol -én végződő helyébe -én. Ez a lánc számozva, hogy a szénatomok részt vesz a kialakulását egy kettős kötés, kapott száma a lehető legkisebb legyen:
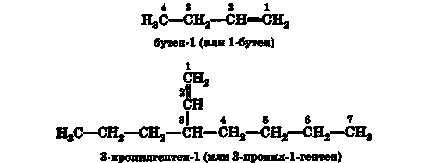
Gyökök említett és számozását esetében alkánok.
Mert alkének viszonylag egyszerű szerkezetet hagyjuk, hogy több mint csak egy név. Tehát, néhány, a leggyakoribb az úgynevezett alkének, hozzátéve, az utótag -én, hogy a nevét, a szénhidrogén-csoport, hogy az ugyanazon szénvázhoz:
Szénhidrogén származó gyökök alkének Ray -enil utótag. A számozás kezdődik radikális szénatom szabad vegyértéke. Ahhoz azonban, hogy a legegyszerűbb Alkenilcsoportokra helyett szisztematikus-nek nevét használhatják a triviális:
A hidrogénatomok közvetlenül kapcsolódnak nenasy-schennymi szénatom képezi a kettős kötés gyakran nevezik vinilnymi hidrogénatom,
Amellett, hogy a szénváz izoméria, körében alkének is helyzeti izomerek a kettős kötés. Általánosságban, az ilyen típusú izomériát - helyettes helyzeti izomer (funkció) - figyelhető meg minden olyan esetben, ahol a mol-Kul vannak olyan funkciós csoportok. A alkán C4 H10 két szerkezeti izomer:
Az alkén C4 H8 (butén) három izomer:
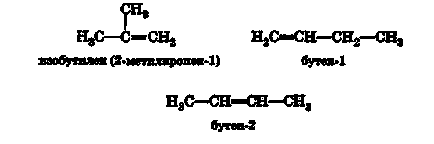
Butén-1 és butén-2 a helyzeti izomereket a funkció-TION (ebben az esetben a szerepe végez kettős kötés).
Térbeli izomerek különböznek a térbeli elrendezése a szubsztituensek egymáshoz képest, és az úgynevezett cisz-izomerjei, kivéve, ha a szubsztituensek az egyik oldalán helyezkedik el, a kettős kötés, és a transz-izomerek, ha ellentétes oldalain:
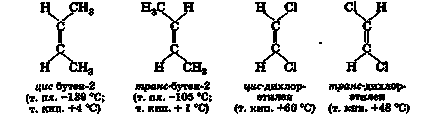
3. A szerkezet a kettős kötés
Az energia különbség a molekula egy kettős kötéssel C = C 611 kJ / mól; mivel az energia σ-kötés a C-C 339 kJ / mol, az energia különbség π -bond csak 611-339 = 272 kJ / mól. π elektronok könnyebben befolyásolhatók σ elektronok, például a polarizáló hatások bármely oldószer vagy támadó reagensek. Ez annak köszönhető, hogy a különbség a szimmetria az eloszlás az elektron felhő-ment σ- és π-elektronok. Maximális átfedő p pályák, és így a minimális-szabad energia a molekula végrehajtott csak a lapos TUP enii vinil-fragmenst és egy rövidített C-C egyenlő távolság 0,134nm, azaz sokkal kisebb, mint egy verseny-távolság közötti szénatomot tartalmaz, egy közvetlen kötés (0,154 nm). A turn „fele” a molekula-telno egymáshoz képest egy kettős kötés tengelye, az átfedési foka pályák csökken, mivel a kiadások energia. Viem-Ennek az a következménye, hogy nincs szabad rotáció a tengelye a kettős kötés, és a létezését geometriai izomer lehet megfelelő szubsztitúció a szénatomok.
4. Fizikai tulajdonságok
Az alkánok, alacsonyabb homológjait, sorozat egyszerű alkének normál körülmények között - a gázokat, és a C5 - az alacsony forráspontú folyadék.
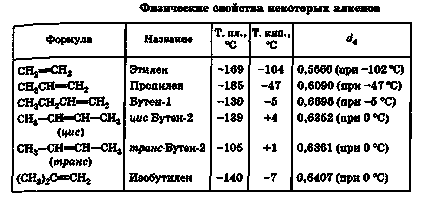
Minden alkének az alkánok gyakorlatilag oldhatatlanok vízben és oldhatók más szerves-oldódnak Lyakh kivéve metil-alkohol; mindannyian egy férfi Shui sűrű, mint a víz.
5. Kémiai tulajdonságok
Ha figyelembe vesszük reaktivitása a komplex vagy-szerves vegyületek az általános elvet. A fájdalom-shinstve részt vevő reakciókat nem „inert” szénhidrogéncsoport, és a rendelkezésre álló funkciós csoportok és a környezet a közeli-nyak. Ez természetes is, mivel a legtöbb kötvények kevésbé erős, mint a C-C és a C-H, és ezen túlmenően, a kommunikáció a funkció-közi csoport és közel a leginkább polarizált.
Ez természetes, hogy elvárják, hogy az alkén reakciók mennek végbe a kettős kötés, ami szintén tekinthető a funkciós csoport távú, és ezért adjunction-CIÓ reakciókat, szubsztitúciós reakciókat és nem kizárólag a korábban dis megjelenésű alkánok.
hidrogén mellett alkének keletkezéséhez vezet alkánok:
Amellett a hidrogénnek az etilénre a vegyületek a-katalizátor távollétében történik csak nagy ütemben-struktúrák, amelynél gyakran kezdődik lebontása szerves-ing anyagok. Jelentősen könnyebb a hozzáadott hidrogén mennyisége jelenlétében katalízis tori. Katalizátorok platinacsoportbeli fémek egy finoman eloszlatott formában, platina maga és különösen a palládium, de - még normál hőmérsékleten. Big Prac-kritikus érték felfedezése volt Sabatier, akik alkalmazzák egy speciálisan előállított finomra zúzott nikkel hőmérsékleten 150-300 ° C, és a sok papír, amíg találni magát a sokoldalú ez a katalizátor a különböző redukciós reakciók.
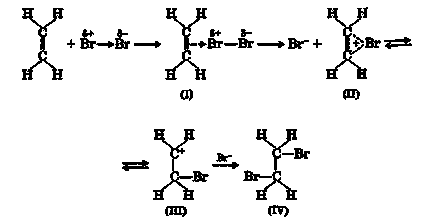
Halogénatom kapcsolódik alkének alkotnak digalogenoproizvodnyh tartalmaz halogénatomokat szomszédos szénatomokhoz;
Az első lépésben ennek a reakciónak van közötti kölcsönhatás π-elektronok a kettős kötés, és egy elektrofil halogén részecske alkotnak egy π-komplexet (I). További π-komplex átrendeződés be ónium (bromonievy) ion (II) halogénatommal oschepleniem anion egyensúlyban a karbokation (III). Ezután anion megtámadja a ónium ion adduktumot alakítunk ki (IV):